CDMO服務介紹
醫療器械注冊人制度(MAH)全面實施,即允許醫療器械注冊人(注冊證持有人)通過委托合規的生產平臺的方式獲得產品注冊審批上市,從而優化了資源配置,加快創新醫療器械產品上市進程。
瑞旭集團基于醫療器械注冊人制度打造了合規的專業研發生產服務平臺-瑞旭醫療器械產業轉化CDMO平臺,致力于為進口醫療器械國產化、科研成果產業轉化、政府引導項目轉化、研發生產資源整合項目及初創期器械項目提供法規咨詢、技術轉化、樣品生產、檢測驗證、臨床評價(試驗)、質量體系及注冊申報(認證)等全產業鏈技術服務。幫助創新醫療器械企業減少研發生產運營成本、縮短產品上市周期、提升項目轉化成功率、提高產品注冊通過率,高效推進醫療器械的產業化。
醫療器械產業化全流程技術服務
瑞旭集團通過整合原有醫療器械檢驗檢測、質量體系、臨床前動物實驗、臨床試驗、注冊申報等業務,將服務鏈向上游延伸,將醫療器械研發和生產外包服務納入到瑞旭集團醫療器械技術服務體系,致力于為國內外醫療器械企業提供從研發生產到臨床注冊全產業技術服務。
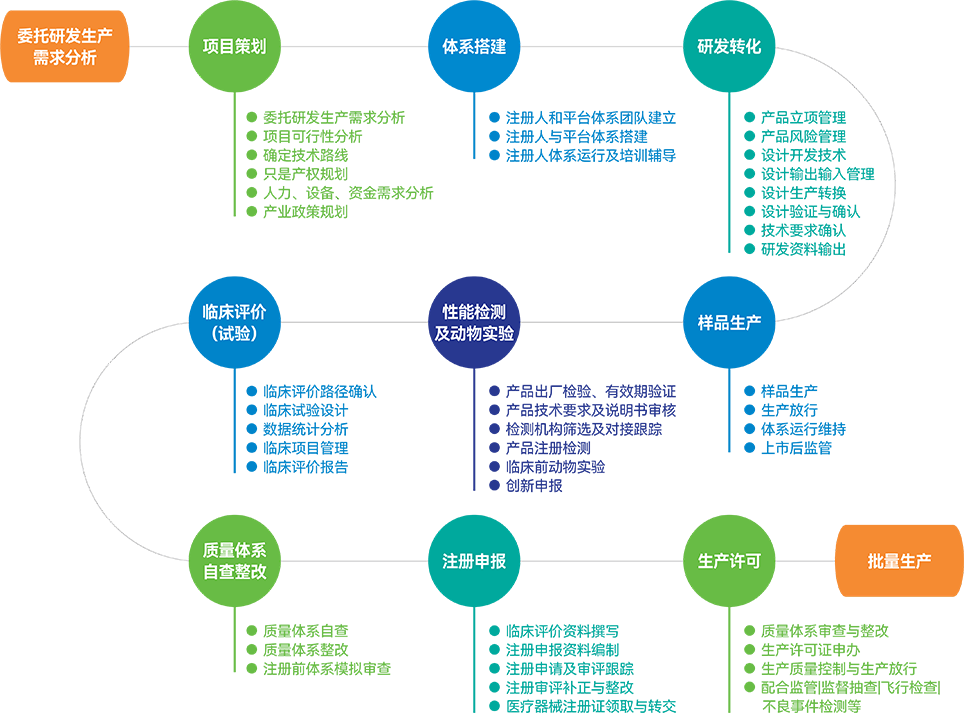
CDMO服務模式
從概念到產品產業化合規上市

CDMO服務領域
進口醫療器械本地化生產
進口醫療器械國產化替代
高校及科研院所的醫療器械技術成果產業化轉化
政府引導的創新醫療器械項目產業化
注冊人制度下研發生產資源重新整合的項目
其它有需求的創新醫療器械產業化及市場準入
CDMO服務內容

CDMO服務優勢
專業的研發生產平臺
瑞旭CDMO平臺配置有專業研發生產平臺,其中9個無菌生產車間共計4600㎡,非無菌生產車間3個,配置結構設計實驗室、有源器械研發實驗室、醫用耗材研發實驗室、理化實驗室、微生物及無菌實驗室。可滿足各類醫療器械的研發和生產。

成熟的技術及運營管理團隊
瑞旭CDMO平臺配備醫療器械產業化項目管理、研發、生產、檢驗、質量體系、臨床、注冊等專業技術團隊,其中核心團隊90%在醫療器械行業具有10年以上從業經驗,涉及消化、泌尿、婦科、骨科、肝膽外科、整形外科、神經外科、呼吸科等領域器械產品的研發、生產、體系、臨床和注冊成功經驗。

豐富醫療器械研發生產經驗
平臺擁有自主研發和生產的多項創新醫療器械產品,已經成功通過審查并獲得醫療器械注冊證和生產許可證。

完善的產業政策和渠道資源
平臺與科技政策咨詢平臺、創新醫療器械孵化器、產業基金、科研機構等多渠道建立合作,為醫療器械注冊人提供公司注冊、技術轉化、專利申報、項目申報、投融資咨詢、專業輔導、人才培養、項目孵化等配套服務。
聯系我們
杭州瑞旭科技集團有限公司
北 京:010-6398 4062 15010201703
杭 州:0571-8720 6527 13588404338
郵 箱:md@jianzaoshiwang.cn
總部地址:杭州市濱江區秋溢路288號東冠高新科技園1號樓11層
CDMO地址:杭州市余杭區瓶窯鎮嶺上路2號(萊恩瑟特醫療園區內)
