近日,歐盟委員會正式發布法規(EU) 2023/464文件,修訂了法規(EC) No 440/2008的附件,該附件是作為REACH法規配套的測試方法。此次更新,引入了大量的最新的OECD體外測試方法以及移除了不少舊的測試方法,諸如兩代生殖毒性試驗(OECD 416)和UDS試驗 (OECD486),有力推動了體外測試方法在歐盟的應用。根據本次更新,結合REACH法規測試要求,對本次涉及到的毒理學測試方法重要的變化進行總結:
1. 嚴重眼損傷/眼刺激
正式引入OECD 467-嚴重眼損傷和眼刺激的確定方法,采用該方法后,可以采用體外方法即可對物質做出合適的分類,大部分情況下無需引入體內方法。下圖僅顯示OECD 467方法中的一種測試策略,實際測試過程中,需要根據物質的液體/固體,水溶解性以及表面張力情況,主要通過OECD 492+OECD437,結合水溶解度、蒸汽壓、表面張力、正辛醇水分配系數等理化性質,可以做出非此類/類別1/類別2的區分。或者通過OECD491+OECD437的組合,做出非此類/類別1/類別2的區分。
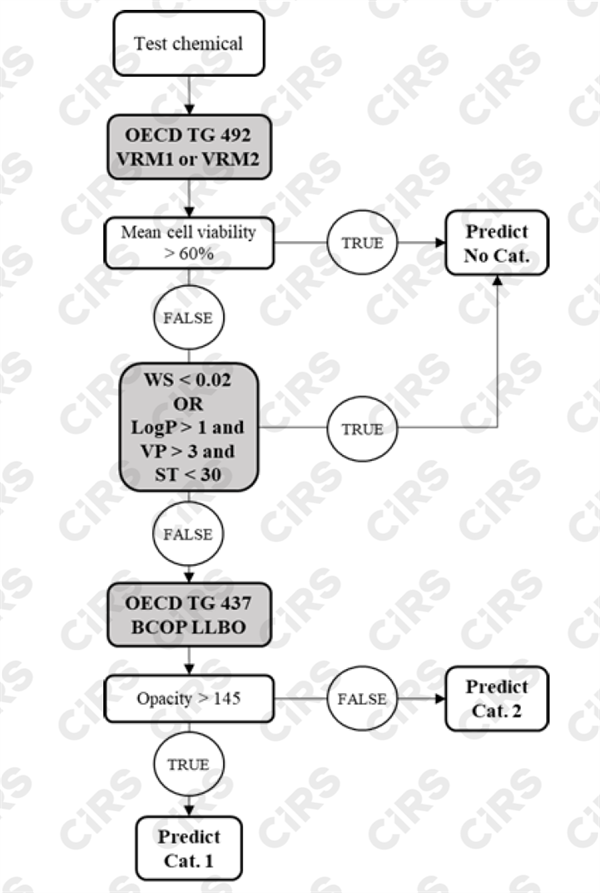
2. 皮膚致敏性
正式引入了OECD497-皮膚致敏性的確定方法,通過2個體外實驗方法(OECD 442C+OECD 442E)再加一個QSAR結果,如果體外實驗結果比較理想,結合QSAR結果,即可根據下圖做出合適的分類,如果體外實驗結果或者QSAR結果不太理想,也有一定可能性對物質完成皮膚致敏性分類,通過這些方法可以有效降低LLNA的測試需求。
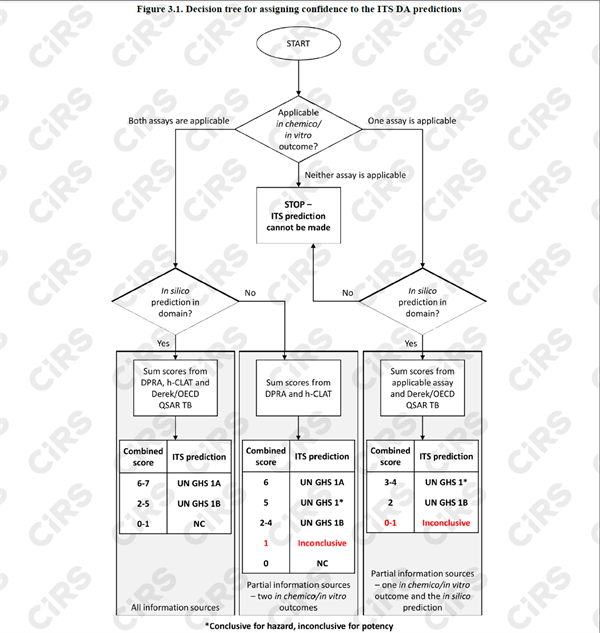
3. 致突變性
正式引入兩種比較新的體內基因方法,包括OECD 488-轉基因嚙齒動物體細胞和生殖細胞基因突變以及OECD 470-哺乳動物紅細胞Pig-a基因突變測定,也給體內基因突變的實驗設計更多選擇。同時移除了UDS方法,目前在歐洲REACH法規卷宗評估要求開展的體內基因突變實驗中,基本上會要求在Comet或轉基因方法2選1。
4. 生殖毒性/發育毒性
正式移除兩代生殖毒性試驗(OECD 416),統一用擴展一代生殖毒性試驗(OECD 443)代替,早在之前的REACH法規要求里,就已經統一用OECD 443取代了,由于該實驗費用高昂,有歐洲實驗室報價高達100萬歐元,對面臨卷宗評估的高噸位注冊人造成巨大壓力。
5. 內分泌干擾特性
新增若干新的內分泌干擾特性體外方法,比如OECD 455-利用穩定轉染細胞系檢測雌激素受體激動劑的體外轉錄激活試驗、OECD456-R295R細胞系類固醇生成試驗、OECD 45-利用穩定轉染細胞系檢測雄激素受體激動劑的體外轉錄激活試驗以及OECD493-人重組雌激素受體親和力體外試驗等。體內方法包括OECD 440-嚙齒類動物子宮增重試驗(UT試驗)和OECD441-大鼠中的Hershberger試驗(H試驗)。由于目前歐盟CLP法規已完成修訂,正式引入內分泌干擾特性分類,預計未來內分泌干擾試驗有可能成為考察物質特性的一個重要組成部分。
涉及到其他毒理,生態毒理的試驗方法由于不是常見的測試方法,對試驗的選擇影響不大,所以就不一一贅述了。
專家點評:
此次測試方法的更新,可以看到歐盟在推進體外測試方法,尤其是皮膚腐蝕/刺激,嚴重眼損傷/刺激以及皮膚致敏性方面是全球領先的,這些體外測試的方法應用也將逐步擴展到其他國家的化學品登記注冊中,從而更好推動全球替代方法的應用。同時我們也注意到近期歐盟在更新CLP法規,新引入內分泌干擾特性分類,此次內分泌干擾特性的體外和體內測試方法的公布,有可能未來成為研究物質相關內分泌干擾特性的試驗組合,需要引起企業關注。
新加入的體內基因突變測試方法包括OECD 488和OECD 470,也給企業更多的試驗選擇,但由于這些方法比較新,包括價格方面也相對較高,導致實驗室的選擇面臨較大困難,也對實驗室提出了更高的要求。兩代生殖毒性測試,在較早的環節里已經被擴展一代生殖毒性測試所取代,對歐盟REACH注冊的影響已經不存在,對于要開展相關測試的注冊人經濟壓力較大(OECD 443單項測試費用相當高)。
綜上所述,企業在開展REACH注冊要求的相關節點時,應根據最新的指南,結合合適的方法,從而避免測試不滿足相關法規要求。
相關推薦:
