1、消毒產品介紹
消毒產品定義:指專門用于殺滅和清除傳播媒介上的病原微生物,以化學、物理或生物方式預防控制感染性疾病或傳染性疾病的一類特殊的健康相關產品。
作用方式:化學、物理、生物方式殺滅或清除病原微生物。
使用場所:人體外部環境:醫療器械、皮膚、黏膜、餐飲具、瓜果蔬菜、水、環境、物體表面、空氣、污物等。
防治對象:病原微生物,包括金黃色葡萄球菌、大腸桿菌、白色念珠菌、銅綠假單胞菌、細菌芽胞、龜分枝桿菌、白色葡萄球菌、黑曲霉菌、脊髓灰質炎病毒等。
消毒產品類別:
- 消毒劑(含氯消毒劑、過氧化物類消毒劑、醛類消毒劑、醇類消毒劑、含碘消毒劑、酚類消毒劑、環氧乙烷、雙胍類消毒劑和季銨鹽類消毒劑);
- 消毒器械(包括生物指示劑、化學指示劑及滅菌包裝物);
- 衛生用品(一次性衛生用品+抗抑菌制劑)。
風險等級:
- 第 I 類:較高風險,需嚴格管理以保證安全、有效的消毒產品(包括用于醫療器械的高水平消毒劑和消毒器械、滅菌劑和滅菌器械,皮膚、黏膜消毒劑,生物指示物、滅菌效果化學指示物等);
- 第 II 類:中度風險,需要加強管理以保證安全、有效的消毒產品(包括除第一類產品外的消毒劑、消毒器械、化學指示物,以及帶有滅菌標識的滅菌物品包裝物、抗(抑)菌制劑等);
- 第 III 類:風險程度較低,實行常規管理可以保證安全、有效的除抗(抑)菌制劑外的衛生用品(是除抗(抑)菌制劑外的衛生用品,如婦女經期衛生用品、尿布等排泄物衛生用品、其他的一次性衛生用品等)。
2、消毒產品監管
監管部門
國家衛健委 | 各地衛生監督機構 | 市場監督局 | 標委會 | 海關及CIQ | CDC | 應急管理部 |
負責全國消毒產品監督管理工作 | 負責本轄區消毒產品的審批、備案以及監督抽檢工作 | 上市消毒產品展開抽查、消毒產品營業執照頒發 | 消毒產品標準立項、制定、審查和發布 | 進出口消毒產品檢驗檢疫及關稅征收 | 新消毒產品的技術評審并負責組織制定國家公共衛生技術方案和指南 | 危險化學品生產許可、經營許可、登記等 |
法律法規
- 《中華人民共和國傳染病防治法》
- 《消毒管理辦法》
- 《消毒產品分類目錄》
- 《消毒技術規范》
- 《消毒產品衛生安全評價規定》
- 《消毒產品生產企業衛生規范》
- 《消毒產品衛生安全評價技術要求》
- 消毒產品相關衛生標準
消毒產品生產企業的衛生監督內容
當地衛生監督部門或機構主要對消毒產品生產企業進行以下衛生監督:
- 消毒產品及生產企業衛生許可資質,在國內從事消毒產品生產、分裝的單位和個人,必須按照相關規定要求申領消毒產品生產企業衛生許可證一企一生產場所一證,一個集團或公司擁有多個生產場所的,應分別申請衛生許可證。企業生產列入《危險化學品目錄》中的消毒產品成品或者中間產品, 還應依照規定取得危險化學品安全生產許可證;
- 生產條件(生產皮膚黏膜消毒劑&抗抑菌制劑&衛生用品需要凈化車間、生產戊二醛車間需通風設施、生產乙醇車間需防爆設施),生產過程(是否執行標準操作規程和管理制度,是否添加國家規定禁用的物質);
- 使用原材料衛生質量;
- 消毒產品和物料倉儲條件;
- 消毒產品從業人員配備和管理情況;
- 消毒產品衛生質量:出廠檢驗;
- 衛生安全評價報告+說明書標簽。
3、消毒產品衛生安全評價
2014年,為進一步深化衛生行政審批制度改革,規范消毒產品的生產經營行為,保障用于傳染病防治的消毒產品的有效性、安全性,依據《中華人民共和國傳染病防治法》、《消毒管理辦法》和有關規定,制定了《消毒產品衛生安全評價規定》,后又在2018年發布WS 628-2018《消毒產品衛生安全評價技術要求》,其中提出產品責任單位在第一類和第二類(消毒劑、消毒器械、抗抑菌制劑)消毒產品首次上市前需要對產品有效性和衛生安全性進行綜合評價,形成《消毒產品衛生安全評價報告》,并對評價結果負責。消毒產品責任單位在第一類和第二類消毒產品首次上市前需要進行衛生安全評價,可將有關衛生安全評價報告錄入全國信息服務平臺進行備案。
全國信息服務平臺于2018年10月8日上線運行,主要是為全國消毒產品責任單位提供消毒產品衛生安全評價網上備案服務,為社會監督和信息查詢、社會信用體系建設、監督機構開展事中事后監督執法提供規范統一的信息服務,網址為:點擊查看
消毒產品安全評價&備案流程
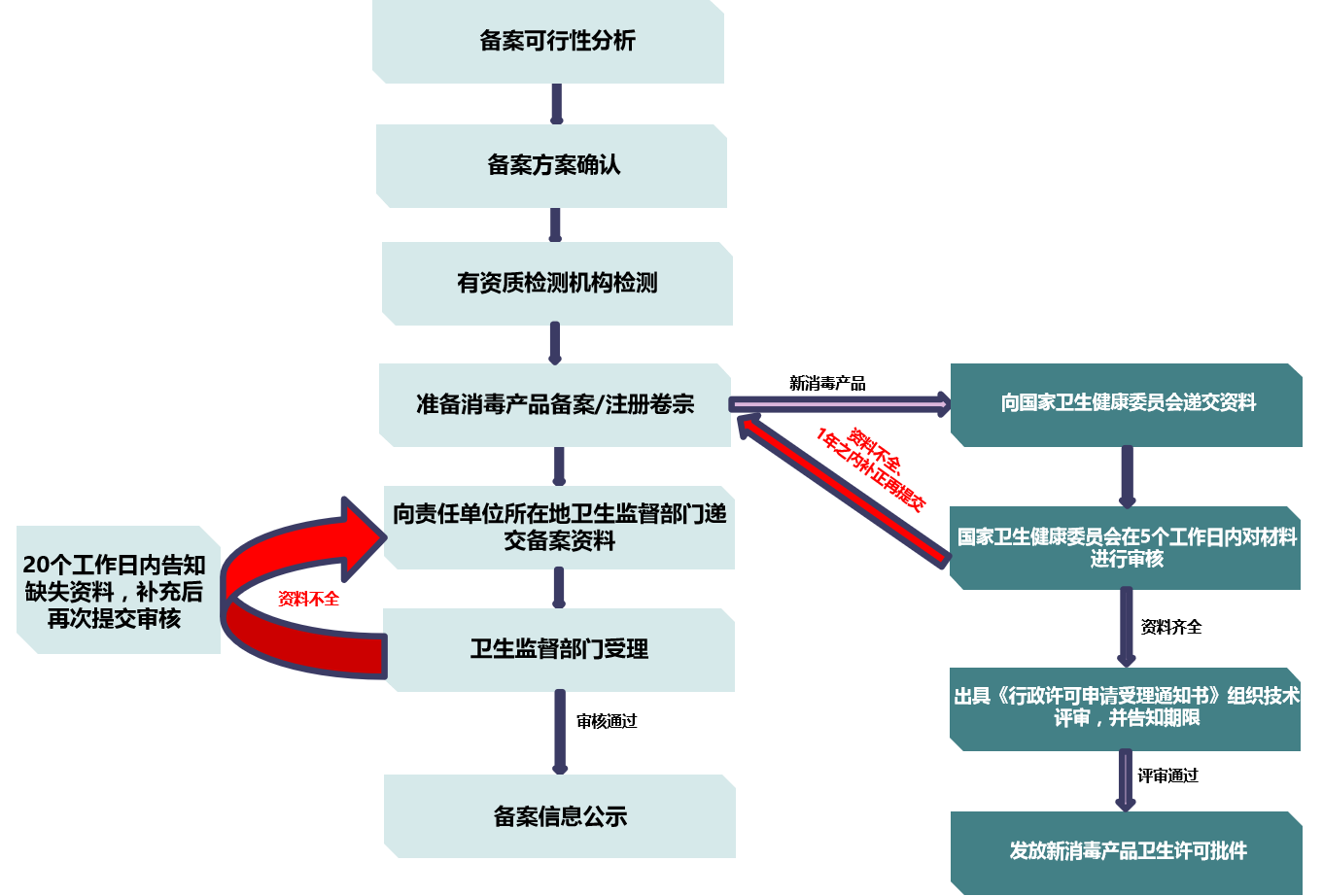
消毒產品衛生安全評價備案,需準備以下資料:
- 封面;
- 備案登記表、安全評價基本情況表;
- 市售標簽(銘牌)、市售說明書;
- 檢驗報告(含結論);
- 國產產品備案企業標準或進口產品質量標準;
- 國產產品生產企業衛生許可證;
- 進口產品生產國(地區)允許生產銷售的證明文件(公證)及報關單;
- 進口產品在華責任單位授權書(公證);
- 消毒劑、抗(抑)菌制劑產品配方;
- 消毒器械元器件、結構圖;
- 其他(產品照片、委托加工合同、商標文件等)。
檢測要求(有CMA資質)
檢測項目 | 檢測內容 |
理化試驗 | 有效成分含量檢測、pH值、穩定性、Pb、As、Hg、金屬腐蝕性 |
毒理學試驗 | 急性經口毒理試驗、一(多)次完整皮膚刺激試驗、眼刺激試驗、致突變試驗 |
功效試驗 | 微生物殺滅試驗、微生物抑菌試驗、(模擬)現場試驗 |
其他 | 微生物污染指標(GB 27951)、微生物指標(GB 15979) |
消毒產品標簽說明書通用要求
國家衛生健康委員會等相關部門制定了強制性衛生標準—GB 38598-2020 《消毒產品標簽說明書通用要求》,對標簽說明書要求作進一步的補充和完善,該標準于2020年11月17日發布,2021年12月1日實施。
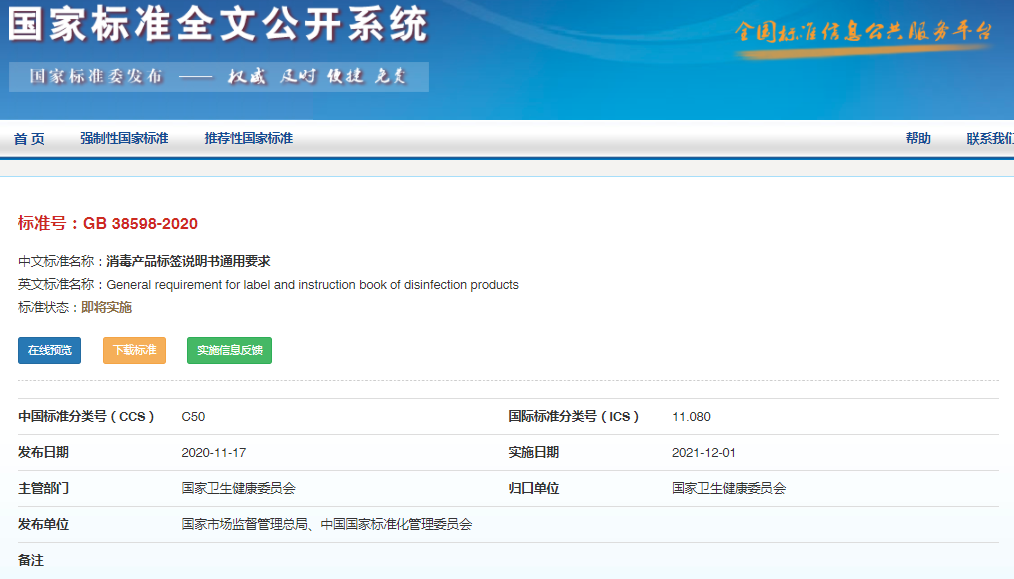
該標準對消毒產品的標簽說明書內容列出各項要求,以消毒劑、抗(抑)菌制劑為例,在申請消毒備案時要注意標簽說明書內容的以下幾點:
消毒劑
定義 | 用于殺滅傳播媒介上的微生物使其達到消毒或滅菌要求的制劑 |
最小銷售包裝特別注意事項 | 使用范圍(用于黏膜的消毒劑應標注“僅限醫療衛生機構診療用”內容) |
標簽、說明書不應標注內容 | a) 抗炎、消炎、治療疾病、減輕或緩解疾病臨床癥狀、描述或解釋疾病癥狀、預防性病、殺精子、避孕; b) 用于人體足部、眼睛、指甲、腋部、頭皮、頭發、鼻黏膜、肛腸部位; c) X天為一療程,或遵醫囑;防止復發;有利于傷口愈合;輔助配合藥物治療。 |
產品名稱示例 | XX®皮膚黏膜消毒液;XXTM戊二醛消毒液;XX牌三氯異氰尿酸消毒片;XX®碘伏消毒液;XX牌消毒液(多用途或多種有效殺菌成分的) |
抗(抑)菌制劑
定義 | 抗菌制劑:直接接觸人體完整皮膚或黏膜的,具有一定殺菌作用的制劑 |
抑菌制劑:直接接觸人體完整皮膚或黏膜的,具有一定抑菌作用的制劑 | |
最小銷售包裝特別注意事項 | 抗(抑)菌制劑還應標注有效成分及其含量、使用范圍(用于陰部黏膜的應標注“不應用于性生活中對疾病的預防”) |
標簽、說明書不應標注內容 | d) 抗炎、消炎、治療疾病、減輕或緩解疾病癥狀預防性病; e) 適用于破損皮膚、破損黏膜、傷口等; f) 高效、消毒、滅菌、除菌、殺精子、避孕; g) 用于人體足部、眼睛、指甲、腋部、頭發、頭皮、鼻黏膜、肛腸部位; h) X天為一療程,或遵醫囑;防止復發;有利于傷口愈合;輔助配合藥物治療。 |
產品名稱示例 | XX牌抗菌洗手液;XX®口腔抑菌噴劑 |
4、消毒產品進出口法規要求
法律法規
- 《進出口商品檢驗法》及其實施條例
- 《危險化學品安全管理條例》(國務院令第591號)
- 其他法律法規(《反恐怖主義法》等)
- 《關于進出口危險化學品及其他包裝檢驗監管有關問題的公告》(質檢總局2012年第30號公告)
- 地方政府相關條例(《上海市危險化學品安全管理辦法》等)
受理主體
- 進口:進口化學品的收貨人或者其代理人
- 出口:出口化學品的收貨人或者其代理人
檢驗范圍
- 列入國家《危險化學品名錄》內的進口危險化學品實施檢驗監管
- 列入法定檢驗目錄內的進出口化學品(醫用消毒劑)
消毒產品進口要求
- 確定產品在華責任單位;
- 進行衛生安全評價&備案(I類、II類消毒產品),檢測(III類消毒產品);
- 符合消毒產品標簽,SDS和GHS標簽;
- 確定HS code(380894項下);
- 按要求提供報檢材料;
- 進口商進行危險化學品登記、危險化學品經營許可證;
- 國內運輸合規。
進出口報檢材料
- 進口危險化學品經營企業符合性聲明;
- 出口危險化學品生產企業符合性聲明;
- 《出境危險貨物包裝容器性能檢驗結果單》(散裝貨物除外);
- 危險特性分類鑒別報告;
- 中文安全數據單、中文危險公示標簽樣本;
- 對需要添加抑制劑或穩定劑的產品,應提供實際添加抑制劑或穩定劑的名稱、數量等情況說明;
- 出口屬于危險貨物的消毒劑的生產企業還應向所在地海關申請出口危險貨物包裝使用鑒定。
屬于危險化學品、危險貨物的消毒劑
- 醇類消毒產品(乙醇(體積比>24%)消毒凝膠、異丙醇消毒液、酒精濕巾);
- 氧化劑類消毒產品(含有次氯酸鈉、次氯酸的消毒產品、過氧乙酸(含量>8%));
- 季銨鹽類消毒劑(高濃度季銨鹽(含量>5%)危險貨物);
- 復合碘產品。
危險貨物在中國的運輸
危險貨物在中國運輸,如采用不同的運輸方式,按照不同的標準執行。
公路 | 《道路危險貨物運輸管理規定》 |
空運 | 《民用航空危險物品運輸》 |
鐵路 | 《鐵路危險貨物運輸安全監督管理規定》 |
海運 | 參照IMDG操作 |
內河 | 《中華人民共和國內河交通安全管理條例》 |
少量危險化學品在中國運輸
“危險化學品”禁止普通快遞運輸:
根據危險化學品安全管理條例-2011,第六十四條:任何單位和個人不得交寄危險化學品或者在郵件、快件內夾帶危險化學品,不得將危險化學品匿報或者謊報為普通物品交寄。郵政企業、快遞企業不得收寄危險化學品。
例外數量(EQ)&有限數量(LQ):是指危險貨物在移交運輸時,如數量較少,且包裝滿足一定要求,即可免除運輸時的部分合規要求(例如,承運人資質,包裝性能測試)。
參考法規:《危險貨物道路運輸規則》(JT/T617-2018);GB28644.1-2012 危險貨物例外數量和包裝要求;GB28644.2-2012 危險貨物有限數量和包裝要求;危險貨物道路運輸安全管理辦法。
危險貨物–例外數量和有限數量運輸
危險貨物必須是包裝類Ⅱ或Ⅲ;包裝類Ⅰ的危險貨物不得限量;必須利用組合包裝(內包裝置于外包裝之內)。
聯合國編號 | 中文名稱和說明 | 英文名稱和說明 | 類別或項別 | 包裝類別 | 有限數量 |
1212 | 異丁醇 | ISOBUTANOL | 3 | III | 5L |
1219 | 異丙醇 | ISOPROPANOL | 3 | II | 1L |
1230 | 乙醇 | METHANOL | 3 | II | 1L |
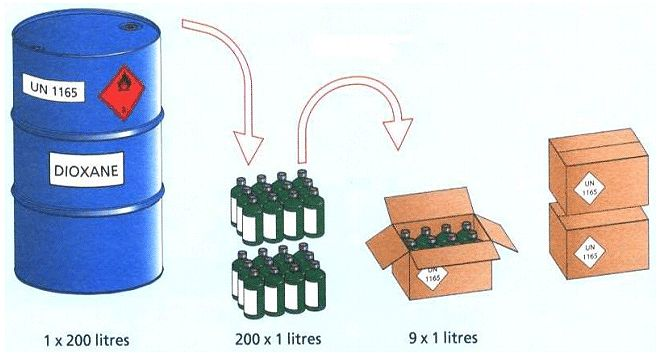
限量的原則是把大包件分解成小包件,然后將小包件置于外包裝內。雙層包裝保護產品和可能的小滲漏。包括:吸附材料、襯墊等保護內容器的部件。
消毒抑菌產品及驅蚊產品受不同的法規管理,對于產品配方、安全測試、標簽、登記備案和委托加工都有自己獨特的監管要求。
瑞旭集團將于4月12日舉辦線上法規培訓課《中國消毒抑菌產品及驅蚊產品合規培訓》,誠邀您參加。本次培訓免費,將幫您了解消毒抑菌產品及驅蚊產品在中國的管理法規,以及新產品研發上市需要知道的注意事項。
會議時間
語言 | 日期 | 北京時間 | 演講者 |
中文 | 2022年4月12日 | 9:00– 9:40 AM | 中國消毒抑菌產品研發上市合規要點 王方 女士 瑞旭集團日化事業部消毒劑法規技術專家 |
9:40-10:20AM | 中國驅蚊產品研發上市合規要點 丁平 女士 瑞旭集團農化事業部總經理 |
主辦方
- 杭州瑞旭科技集團有限公司(CIRS)
會議軟件
- 小鵝通
會議費用
- 免費

相關推薦:
- 電商平臺消毒產品入駐要求分析
- 區分化妝品和消毒產品-勿將消毒產品當作化妝品進行銷售宣傳
- 國家藥監局發布關于1批次化妝品檢出禁用原料的通告(2021年第54號)
- GB 38598-2020《消毒產品標簽說明書通用要求》2021年12月1日實施
我們的服務:
