 為進一步規范重組膠原蛋白創面敷料等醫療器械的管理,國家藥監局器審中心組織制定了《重組膠原蛋白創面敷料注冊審查指導原則》等2項醫療器械產品注冊審查指導原則(見附件),現予發布。
為進一步規范重組膠原蛋白創面敷料等醫療器械的管理,國家藥監局器審中心組織制定了《重組膠原蛋白創面敷料注冊審查指導原則》等2項醫療器械產品注冊審查指導原則(見附件),現予發布。
特此通告。
附件:1.重組膠原蛋白創面敷料注冊審查指導原則( 下載 )
2.重組人源化膠原蛋白原材料評價指導原則( 下載 )
國家藥品監督管理局
醫療器械技術審評中心
2023年5月22日
【附件1】
重組膠原蛋白創面敷料注冊審查指導原則
本指導原則旨在指導注冊申請人準備及撰寫重組膠原蛋白創面敷料注冊申報資料,同時也為技術審評部門審查注冊申報資料提供參考。
本指導原則是對重組膠原蛋白創面敷料產品的一般要求,注冊申請人應依據產品的具體特性確定其中內容是否適用,若不適用,需具體闡述理由及相應的科學依據,并依據產品的具體特性對注冊申報資料的內容進行充實和細化。
本指導原則是供注冊申請人和技術審評人員使用的指導性文件,但不包括注冊審批所涉及的行政事項,亦不作為法規強制執行。如果有能夠滿足相關法規要求的其他方法,也可以采用,但需要提供詳細的研究資料和驗證資料。需在遵循相關法規和強制性標準的前提下使用本指導原則。
本指導原則是在現行法規、標準體系以及當前認知水平下制定的,隨著法規和標準的不斷完善,以及科學技術的不斷發展,本指導原則相關內容也將適時進行調整。
一、適用范圍
本指導原則適用于按第二類醫療器械管理的重組膠原蛋白創面敷料,其結構組成中含有重組膠原蛋白成分(不包括動物組織提取的膠原蛋白成分),用于非慢性創面及其周圍皮膚的護理。產品通常為凝膠、液體、敷貼、膏狀等型式,包括一次性使用的產品和開封后多次使用的產品,以無菌形式或非無菌形式提供。產品中所含成分不具有藥理學作用,不可被人體吸收。對產品分類和屬性不明確的,需申請產品的分類和屬性界定。
二、注冊審查要點
(一)監管信息
注冊申請人應提供申請表、既往溝通記錄(如不適用,應當明確聲明申報產品沒有既往申報和/或申報前溝通)、關聯文件(如主文檔授權信)及其他管理信息等。
1.申請表
1.1產品名稱
產品名稱應符合《醫療器械通用名稱命名規則》等相關法規、規范性文件的要求。產品名稱的材料部分統一為“重組膠原蛋白”,如重組膠原蛋白凝膠敷料、重組膠原蛋白創面敷貼等。除非有充分資料證明重組膠原蛋白原材料的結構特征等能夠給申報產品功能帶來額外獲益,產品名稱不區分具體材料特征。
1.2管理類別、分類編碼
申報產品中所含的重組膠原蛋白(不包括動物組織提取的膠原蛋白成分)等成分不具有藥理學作用,不可被人體吸收時,按第二類醫療器械管理,參考《醫療器械分類目錄》中分類編碼為14注輸、護理和防護器械-10創面敷料的第二類醫療器械相關描述。根據不同的產品型式,二級產品類別可為-01創面敷貼、-04凝膠敷料、-08液體、膏狀敷料等。
1.3注冊單元劃分的原則和實例
申報產品的注冊單元原則上以產品的技術原理、主要結構組成、性能指標和適用范圍為劃分依據,同時應滿足《醫療器械注冊單元劃分指導原則》相關要求。例如:
1.3.1凝膠型、液體型、敷貼型等產品,主要組成成分相同但配比不同,性能指標存在差異而影響產品安全有效性時,建議劃分為不同的注冊單元。
1.3.2凝膠型、液體型等產品,主要組成成分和配比相同,包裝材質不同(包裝對產品性能無影響)時,如低硼硅西林瓶和聚對苯二甲酸乙二醇酯(PET)噴瓶,建議劃分為同一個注冊單元。
1.4型號規格
應明確申報產品的型號規格。
1.5結構及組成
結構及組成中組分名稱應規范。產品所含成分可能涉及很多種類,但所含成分不應具有藥理學作用,不可被人體吸收。產品結構及組成原則上不體現重組膠原蛋白原材料的結構特征、氨基酸序列等相關信息(除非有充分資料證明重組膠原蛋白原材料的結構特征等能夠給申報產品功能帶來額外獲益)。
2.產品列表
應明確列出擬申報產品的型號、規格、結構及組成、附件,以及每個規格型號的標識和描述說明。
(二)綜述資料
1.產品描述
1.1工作原理
應描述申報產品的工作原理。如通過在創面表面形成保護層,起物理屏障作用。用于非慢性創面及其周圍皮膚的護理。
1.2結構組成
申報產品含重組膠原蛋白成分、成膜成分或高分子增稠成分、保濕潤滑成分、調節劑、乳化劑、防腐成分、緩沖劑、溶劑、基質載體等。產品中除重組膠原蛋白外,其他常見的組成成分有:聚乙烯醇、聚乙二醇、卡波姆、黃原膠、海藻酸鈉、羧甲基纖維素鈉、甘油、丙二醇、海藻糖、聚乙烯吡咯烷酮、三乙醇胺、油酸山梨坦(司盤80) 、鯨蠟硬脂醇、尼泊金甲酯鈉、尼泊金丙酯鈉、苯氧乙醇、羥苯甲酯、醋酸鹽緩沖劑、磷酸鹽緩沖劑、注射用水、純化水、無紡布貼等。產品通常為凝膠、液體、敷貼、膏狀等型式,一次性使用或開封后多次使用,無菌形式或非無菌形式提供。
1.3型號規格
對于存在多種型號規格的申報產品,應當明確各型號規格的區別。應當采用對比表或帶有說明性文字的圖片、圖表,描述各種型號規格的結構組成、功能、產品特征和技術參數等內容。應清晰、準確表述產品的全部型號/規格,型號/規格可以以裝量或尺寸等形式表述,例如:5mL、10g、15mL/瓶、20g/支、25g/貼等,不得出現“依據客戶需求可提供定制型號”。不得出現誤導或超出申報產品描述以及預期用途范疇的表述內容。
1.4包裝說明
說明申報產品組成的包裝信息,以無菌形式提供的醫療器械,應當說明其無菌屏障系統的信息;以非無菌形式提供的醫療器械,應當說明保持其微生物指標的包裝信息。說明如何確保最終使用者可清晰地辨識包裝的完整性。
1.5研發歷程
闡述申報產品的研發背景和目的。如有參考的同類產品或前代產品(如有),應當提供同類產品或前代產品的信息,并說明選擇其作為研發參考的原因。
1.6與同類和/或前代產品的參考和比較
列表比較說明申報產品與同類產品和/或前代產品(如有)在工作原理、結構組成、制造材料、性能指標、作用方式、適用范圍等方面的異同。
2.適用范圍和禁忌證
2.1適用范圍
2.1.1應當描述申報產品的適用范圍,明確預期用途。如通過在創面表面形成保護層,起物理屏障作用。用于非慢性創面及其周圍皮膚的護理。如產品宣稱其他的適用范圍,應與臨床評價結論一致,應有充分的臨床數據支持。
2.1.2明確目標用戶及其操作或使用申報產品應當具備的技能/知識/培訓。明確申報產品為一次性使用或開封后多次使用。如適用,明確與申報產品聯合使用實現預期用途的其他產品的詳細信息。
對于已獲得批準的部件或配合使用的附件,應當提供注冊證編號和國家藥監局官方網站公布的注冊證信息。
2.2預期使用環境
應明確申報產品使用場所要求,如醫療機構、家庭等,明確使用環境要求,如需要無菌/非無菌操作的非慢性創面護理等。
2.3適用人群
應詳述申報產品的適用人群。
2.4禁忌證
應說明申報產品臨床應用的禁忌證,應當明確說明申報產品不適宜應用的特定的人群或特定情況等信息,如:對原材料過敏者禁用,對不明確過敏者慎用等。如適用,通過風險/受益評估后,針對某些疾病、情況或特定的人群(如兒童、老年人、孕婦及哺乳期婦女、過敏體質人群),認為不推薦使用該產品,應當明確說明。
3.申報產品上市歷史
如適用,應當提交申報產品的上市情況、不良事件和召回、銷售不良事件及召回率。
(三)非臨床資料
1.產品風險管理資料
應依據GB/T 42062提供產品風險管理報告。注冊申請人應重點說明:申報產品的研制階段已對有關可能的危害及產生的風險進行了估計和評價,針對性地實施了降低風險的技術和管理方面的措施。產品性能測試對上述措施的有效性進行了部分驗證,達到了通用和專用標準的要求。注冊申請人對所有剩余風險進行了評價,全部達到可接受的水平。產品風險分析資料應為注冊申請人關于產品安全性的承諾提供支持。應對申報產品的可能危害進行判定并列出清單(見附件表1)。
2.醫療器械安全和性能基本原則清單
說明申報產品符合《醫療器械安全和性能基本原則清單》各項適用要求所采用的方法,以及證明其符合性的文件。對于《醫療器械安全和性能基本原則清單》中不適用的各項要求,應當說明理由。
3.產品技術要求及檢驗報告
3.1產品技術要求
產品技術要求的制定應符合《醫療器械產品技術要求編寫指導原則》的相關法規要求。本條款給出需要考慮的產品主要技術指標,如有其他指標,建議注冊申請人結合YY/T 1627等適用標準、產品設計特點及臨床應用進行制定。注冊申請人如不采用的條款(包括國家標準、行業標準要求),應當說明理由。
3.1.1產品型號/規格及其劃分說明
應說明申報產品的型號/規格,明確產品型號/規格的劃分說明。
3.1.2性能指標
申報產品的性能指標建議包含以下幾點(包括但不限于此):外觀、裝量(或尺寸、質量)、重組膠原蛋白的鑒別、重組膠原蛋白的含量、粘度/黏度(如適用)、化學性能(如酸堿度、重金屬等)、無菌(或微生物指標),如有配合使用的附件(如噴瓶、滴管等)應制定相應要求等。
注冊申請人如宣稱其他技術參數和功能,應在產品技術要求中予以規定,符合《醫療器械產品技術要求編寫指導原則》的相關法規要求。
3.1.3檢驗方法
申報產品的檢驗方法應根據性能指標制定,優先采用已頒布的標準或公認的檢驗方法。
考慮到產品的成分、配比可能對檢驗結果產生影響,因此產品技術要求中采用的具體檢驗方法應經過驗證,以保證檢驗結果的可靠性。比如重組膠原蛋白的鑒別和含量的檢驗方法,應結合產品實際情況,采用適宜的方法。
3.2產品檢驗報告
可提交注冊申請人出具的自檢報告或委托有資質的醫療器械檢驗機構出具的檢驗報告。若提交自檢報告,應按照《醫療器械自檢管理規定》的要求提供相關資料。
3.3同一注冊單元內注冊檢驗典型性產品確定原則及示例
同一注冊單元中所檢驗產品應能夠代表注冊單元內其他產品安全性和有效性。代表產品的確定可以通過比較同一注冊單元內所有產品的主要原材料、生產工藝、技術結構、性能指標和預期用途等資料,說明其能夠代表注冊單元內其他產品的安全性和有效性。必要時提交不同型號規格產品的差異性檢測報告。
4.研究資料
根據申報產品適用范圍和技術特征,提供非臨床研究綜述,逐項描述所開展的研究,概述研究方法和研究結論。根據非臨床研究綜述,提供相應的研究資料,各項研究可通過實驗室研究、模型研究、文獻研究等方式開展,一般應當包含研究方案、研究報告。采用建模研究的,應當提供產品建模研究資料。
4.1性能研究
應當提供產品化學/材料表征、物理、性能指標及檢驗方法的確定依據、設計輸入來源以及臨床意義,所采用的標準或方法、采用的原因及理論基礎。
申報資料中應明確各種原材料的名稱、重組膠原蛋白原材料的生產工藝(如適用)、質量控制指標及要求等,說明原材料的功能特點或選擇依據。
對于首次用于醫療器械方面的新材料,應提供該材料適合用于符合預期用途的相關研究資料。
如有配合使用的附件(如噴瓶、滴管等)應制定相應要求,考慮附件與產品的適宜性等。
4.2生物學特性研究
申報產品接觸使用者的非慢性創面及其周圍皮膚,屬于表面接觸器械,接觸時間結合產品的使用方法確定。
申請人如進行生物學試驗,應按GB/T 16886.1選擇適用的試驗項目,試驗項目的選擇應結合產品預期接觸的部位以及產品累積使用的接觸時間,根據現行版GB/T 16886.1,考慮細胞毒性、致敏反應、皮內反應項目等。
申請人如開展申報產品與市售產品的等同性比較的生物相容性評價,應按照《醫療器械生物學評價和審查指南》,提供資料證明申報產品與已上市產品具有等同性。
4.3滅菌(除菌)工藝研究
以無菌形式提供的產品,應提交產品包裝及滅菌(除菌)方法選擇的依據,經過確認并進行常規控制。應考慮選用的滅菌(除菌)工藝是否會對重組膠原蛋白產生影響。注冊申請人應開展以下方面的研究:
4.3.1產品與滅菌(除菌)過程的適應性:應考察滅菌(除菌)方法等工藝過程對于產品的影響。
4.3.2包裝與滅菌(除菌)過程的適應性。
4.3.3如適用,應明確滅菌工藝(方法和參數)和無菌保證水平(SAL),無菌保證水平(SAL)應達到10 -6 ,提供滅菌確認報告。可根據適用情況選擇滅菌方式:
如采用濕熱滅菌,參照GB 18278.1標準的要求開展研究;
如采用輻射滅菌,參照GB 18280.1、GB 18280.2、GB/T 18280.3等標準的要求開展研究。
4.3.4若申報產品不能耐受終端滅菌工藝,需提供依據及不能耐受的驗證資料。
如適用,應明確采用的除菌工藝,如過濾除菌等。應明確除菌工藝(方法和參數)和保證水平,提供確認報告。
4.4穩定性研究
4.4.1貨架有效期
應提供貨架有效期研究資料,證明在貨架有效期內,產品可以保持性能功能滿足使用要求。注冊申請人需在試驗方案中設定檢測項目、檢測方法及判定標準。檢測項目包括產品自身性能檢測和包裝系統性能檢測兩方面。實時穩定性試驗結果是驗證產品貨架有效期的直接證據。當加速穩定性試驗結果與其不一致時,應以實時穩定性試驗結果為準。
對于非無菌形式提供的產品,開封后可以多次使用時,應對其開封后穩定性進行研究。為確認產品開封后,在實際使用環境下,經過一段時期仍然能夠滿足使用要求的最長存放時間,建議通過分析評價后選擇合適的檢測項目(如微生物指標等),提供研究報告。
產品以無菌和非無菌兩種形式提供時,應分別進行有效期的研究。
4.4.2包裝研究
應提供包裝研究資料,證明在生產企業規定的運輸貯存條件下,運輸和貯存過程中的環境條件(例如:震動、振動、溫度、濕度、光線的波動)不會對產品的性能造成不利影響。
注冊申請人應提交最終成品包裝的初始完整性和維持完整性的驗證資料。對于在加速穩定性試驗中可能導致產品變性而不適于選擇加速穩定性試驗研究其包裝的情況,應以實時穩定性試驗進行驗證。
包裝研究資料應包括封口試驗以及包裝材料對滅菌的適應性研究。可依據GB/T 19633系列標準對包裝進行分析研究和評價。
4.5證明產品安全性、有效性的其他研究資料
應提供申報產品不可被人體吸收的相關研究資料。如選擇或設計可以模擬臨床使用方式的試驗。
應提供申報產品中重組膠原蛋白成分的質量控制相關資料。建議參照YY/T 1849標準及其他相關標準的要求(如今后有適用的其他標準發布,應參照執行),提供原材料相關質控資料。
申報產品如宣稱形成物理阻隔的保護層或具有成膜效果,應提供適用于申報產品的成膜性研究測試資料。
4.6其他資料
對于符合《免于臨床評價醫療器械目錄》的產品, 注冊申請人可根據產品型式選擇對應的目錄產品免于進行臨床評價。
如無菌形式提供的重組膠原蛋白凝膠、液體、敷貼、膏狀型產品等,符合《免于臨床評價醫療器械目錄》中相應產品的描述時,申報產品可按照《列入免于臨床評價醫療器械目錄產品對比說明技術指導原則》提供相應資料,從基本原理、結構組成、性能、安全性、適用范圍等方面,證明產品的安全有效性。
(四)臨床評價資料
對于不符合《免于臨床評價醫療器械目錄》的產品,應按照《醫療器械注冊與備案管理辦法》《醫療器械臨床評價技術指導原則》《醫療器械臨床試驗質量管理規范》等要求提交臨床評價資料。
1.同品種臨床評價路徑
在滿足注冊法規要求的前提下,可按照《醫療器械臨床評價等同性論證技術指導原則》進行境內已上市同品種產品的對比、分析、評價,并按照《醫療器械注冊申報臨床評價報告技術指導原則》要求的項目和格式出具評價報告。
2.臨床試驗路徑
臨床試驗需按照《醫療器械臨床試驗質量管理規范》開展,提交完整的臨床試驗資料。臨床試驗的設計可參考《醫療器械臨床試驗設計指導原則》,根據注冊申請人宣稱的申報產品適用范圍開展。
(五)產品說明書和標簽樣稿
產品說明書和標簽的編寫應符合《醫療器械說明書和標簽管理規定》、YY/T 0466.1、YY/T 1627和相關法規、規章、規范性文件、強制性標準的要求。說明書中關于產品性能特征的描述不應超過注冊申請人提交的研究資料及產品技術要求,不得含有未經驗證的夸大宣傳的相關描述。申報產品的說明書和標簽原則上不體現重組膠原蛋白原材料的結構特征、氨基酸序列等相關信息(除非有充分資料證明重組膠原蛋白原材料的結構特征等能夠給申報產品功能帶來額外獲益)。應注意以下內容:
1.產品的結構組成及性能指標應與產品技術要求內容一致。
2.無菌形式提供的產品應當注明滅菌方式或除菌工藝、“無菌”等字樣或符號;非無菌形式提供的產品應當注明微生物指標、“不適用于無菌操作的非慢性創面護理 ”、“非無菌”字樣或符號,防止臨床誤操作。
3.注明產品主要原材料,應有對材料過敏者禁止使用的提示。
4.使用前檢查包裝是否完好,如有破損,禁止使用。
5.應標明產品的貨架有效期,嚴禁使用超過貨架有效期的產品。
6.產品應注明建議使用時間和使用方法。如產品可多次使用,應當明確提示使用者該產品開封后應如何保存以及限定時間內使用完畢。
7.使用中若有紅腫、疼痛或瘙癢等不適癥狀,請立即停止使用并清洗干凈,必要時向醫生咨詢或及時就醫。
8.明確針對產品特點的特殊注意事項、警示信息、可能的不良事件及處理措施等。如創面感染的患者不宜使用等。
三、參考文獻
[1]中華人民共和國國務院.醫療器械監督管理條例:中華人民共和國國務院令第739號[Z].
[2]國家市場監督管理總局.醫療器械注冊與備案管理辦法:國家市場監督管理總局令第47號[Z].
[3]國家藥品監督管理局.醫療器械注冊申報資料要求和批準證明文件格式:國家藥監局公告2021年第121號[Z].
[4]國家食品藥品監督管理局.醫療器械注冊單元劃分指導原則:總局通告2017年第187號[Z].
[5]國家食品藥品監督管理局.醫療器械分類目錄:國家食品藥品監督管理總局公告2017年第104號[Z].
[6]國家藥品監督管理局.重組膠原蛋白類醫療產品分類界定原則:國家藥監局通告2021年第27號[Z].
[7]國家藥品監督管理局.醫療器械安全和性能基本原則清單:國家藥監局公告2021年第121號[Z].
[8]國家藥品監督管理局.醫療器械產品技術要求編寫指導原則:國家藥監局公告2022年第8號[Z].
[9]國家藥品監督管理局.醫醫療器械注冊自檢管理規定:國家藥監局公告2021年第126號[Z].
[10]國家食品藥品監督管理局.醫療器械生物學評價和審查指南:國家食品藥品監督管理局通知2007年345號[Z].
[11]國家藥品監督管理局.列入免于臨床評價醫療器械目錄產品對比說明技術指導原則:國家藥監局通告2021年第73號 [Z].
[12]國家藥品監督管理局.免于臨床評價醫療器械目錄:國家藥監局通告2021年第71號[Z].
[13]國家藥品監督管理局.醫療器械臨床評價技術指導原則:國家藥監局通告2021年第73號[Z].
[14]國家食品藥品監督管理局.醫療器械說明書和標簽管理規定:國家食品藥品監督管理總局令第6號[Z].
[15]GB 15979,一次性使用衛生用品衛生標準[S].
[16]GB 18278.1,醫療保健產品滅菌 濕熱 第1部分 醫療器械滅菌過程的開發、確認和常規控制要求[S].
[17]GB 18280.1,醫療保健產品滅菌 輻射 第1部分醫療器械滅菌過程的開發、確認和常規控制要求[S].
[18]GB 18280.2,醫療保健產品滅菌 輻射 第2部分:建立滅菌劑量[S].
[19]GB/T 14233.1,醫用輸液、輸血、注射器具檢驗方法 第1部分:化學分析方法[S].
[20]GB/T 14233.2,醫用輸液、輸血、注射器具檢驗方法 第2部分:生物學試驗方法[S].
[21]GB/T 16886.1,醫療器械生物學評價 第1部分:風險管理過程中的評價與試驗[S].
[22]GB/T 16886.5,醫療器械生物學評價 第5部分:體外細胞毒性試驗[S].
[23]GB/T 16886.10,醫療器械生物學評價 第10部分:刺激與皮膚致敏試驗[S].
[24] GB/T 18280.3,醫療保健產品滅菌 輻射 第3部分:劑量測量指南[S].
[25]GB/T 19633.1,最終滅菌醫療器械包裝 第1部分:材料、無菌屏障系統和包裝系統的要求[S].
[26]GB/T 19633.2,最終滅菌醫療器械包裝 第2部分:成形、密封和裝配過程的確認的要求[S].
[27]GB/T 42062,醫療器械風險管理對醫療器械的應用[S].
[28]GB/T 42061,醫療器械質量管理體系用于法規的要求[S].
[29]YY/T 0466.1,醫療器械用于醫療器械標簽、標記和提供信息的符號 第1部分: 通用要求[S].
[30]YY/T 0681.1,無菌醫療器械包裝試驗方法第1部分:加速老化試驗指南[S].
[31]YY/T 0698.2,最終滅菌醫療器械包裝材料 第2部分:滅菌包裹材料要求和試驗方法[S].
[32]YY/T 1627,急性創面用敷貼、創貼通用要求[S].
[33]YY/T 1849,重組膠原蛋白[S].
[34]中華人民共和國藥典(2020版)[S].
附表
產品主要危險(源)
|
危險(源) |
可預見的事件序列 |
危險(源)的形成因素 |
可能的后果 |
|
生物學 危險(源) |
生物污染 |
生產環境控制不好。包裝破損或使用時不規范造成生物污染;產品沒有達到無菌或微生物指標的要求;開封后多次使用的產品未按開封后穩定性要求使用 |
引起交叉感染 |
|
不正確的配方(化學成分) |
未按照工藝要求配料 |
造成毒性危害 |
|
|
加工工藝 |
加工工藝控制不嚴格,后處理工藝控制不嚴格 |
引入有害物質,引起患者感染或造成毒性危害 |
|
|
環境污染 |
生產環境污染產品,如外來的粉塵、微生物、其他雜質等 |
引起交叉感染 |
|
|
儲存(如溫度、濕度)或運行偏離預定的環境條件 |
產品老化、無菌有效期縮短或開封后性能不能達到使用要求
|
||
|
生物相容性 |
采用不合格或不合格原輔材料 |
引起使用者接觸部位的過敏或刺激 |
|
|
操作 危險(源) |
由不熟練/未經培訓的人員使用 |
操作不熟練、操作失誤 |
無法保證使用的安全性,導致無法達到滿意的使用效果 |
|
使用產品時未按照說明書中操作方法使用 |
錯誤涂覆、貼敷或操作過程中破壞產品的完整性;未采取相應的護理或固定措施 |
無法保證使用的安全性,導致無法達到滿意的使用效果 |
|
|
忽視說明書中禁忌證、警示信息等內容 |
使用過程中出現過敏或刺激;超出產品的最長使用時間;開封后多次使用的產品再次使用前,未經過充分有效的驗證、未按開封后穩定性要求使用、未在規定時間內使用 |
引起使用者接觸部位的過敏或刺激 |
|
|
在限定環境下未正確選用合適的產品 |
引起交叉感染 |
||
|
信息 危險(源)
|
不正確的標簽 |
標記錯誤或不清晰、不全面,沒有按照要求標記 |
錯誤使用;儲存錯誤;產品辨別錯誤 |
|
不正確的說明書;說明書上的注意事項、禁忌證不全 |
缺少詳細的使用方法、必要的警告說明;使用前未檢查產品包裝狀態;未標示使用后的處理方法(如一次性使用產品用后按醫療廢物處理、開封后多次使用的產品應注明推薦開封后儲存條件或使用時間、使用要求);未正確區分一次性使用產品和開封后多次使用產品 |
錯誤操作;無法保證使用安全有效性 |
|
|
對醫療器械壽命終止缺少適當的決定 |
未標識產品有效期或開封后多次使用(如適用) |
使用超出有效期的產品或超出最長開封穩定性時間的產品,或因成分性能變化而導致無法達到滿意的使用效果;或引起交叉感染 |
|
|
不適當的產品包裝(產品污染和/或降低性能) |
生產、運輸和儲存過程中導致包裝破損;包裝封口不嚴密;包裝材料選擇不適當;使用前未檢查產品包裝密封狀態 |
產品使用效果和有效期無法得到保證 |
|
|
一次性使用產品重復使用時危害性警告不適當 |
一次性使用產品的標識不全或不易識別 |
引起交叉感染 |
|
|
開封后多次使用產品使用時危害性警告不適當 |
開封后多次使用產品,未說明保證產品開封穩定性的儲存條件、沒有標識推薦再次使用的操作方法和要求;開封后多次使用產品的標識不全或不易識別 |
達不到使用效果使用效果,引起交叉感染 |
|
|
由于廢物和/或醫療器械處置的污染 |
使用后的產品沒有按照要求銷毀 |
造成環境污染或者細菌的交叉感染 |
【附件2】
重組人源化膠原蛋白原材料評價指導原則
本指導原則旨在指導注冊申請人對醫療器械所用重組人源化膠原蛋白原材料進行充分的研究,并整理形成產品注冊申報資料,同時也為技術審評部門對重組人源化膠原蛋白制成的產品注冊申報資料包括所引用主文檔相關內容的技術審評提供參考。
本指導原則系對醫療器械用重組人源化膠原蛋白原材料的一般要求,適用于人膠原蛋白的所有型別,注冊申請人需依據具體醫療器械產品的特性對產品注冊申報資料涉及的原材料相關內容進行充實和細化,并依據產品的具體特性確定本指導原則相關內容的適用性。本指導原則不直接涉及重組人源化膠原蛋白原材料制成的醫療器械終產品的安全性或有效性評價,具體產品的評價請參考相應的產品注冊審查指導原則。
本指導原則是對注冊申請人和技術審評人員的指導性文件,但不包括注冊審批所涉及的行政事項,亦不作為法規強制執行,如果有能夠滿足相關法規要求的其他方法,也可以采用,但是需要提供詳細的研究資料和驗證資料;需在遵循相關法規和強制性標準的前提下使用本指導原則。
本指導原則是在現行法規和標準體系以及當前認知水平下制定的,隨著法規和標準的不斷完善,以及科學技術的不斷發展,本指導原則相關內容也將進行適時的調整。
近年來,隨著基因重組、蛋白質組學等基礎理論、技術手段和臨床醫療探索研究的不斷發展,重組膠原蛋白日益成為重要的生物材料,為相關醫療器械的研發提供了新的思路與方法。重組人源化膠原蛋白是由DNA重組技術制備的人膠原蛋白特定型別基因編碼的全長或部分氨基酸序列片段,或是含人膠原蛋白功能片段的組合。
重組人源化膠原蛋白僅是重組膠原蛋白的一類,材料特性并不能完全決定最終產品的安全性和有效性。本指導原則中的“原材料”是指用于生產制造醫療器械用的重組人源化膠原蛋白材料。除特別說明外,本指導原則中的“材料”等同于“原材料”。
重組人源化膠原蛋白是通過基因工程生產的蛋白,工程細胞構建過程、生產用細胞的質量控制及常規生產過程控制是該原材料生產工藝及風險評價的基礎,此方面主要的驗證資料,可參考本指導原則的資料性附件作為原材料研究資料的補充,但不作為產品注冊申報資料的必要內容。結合重組人源化膠原蛋白的特點,該資料性附件修改引用了國家藥監局藥審中心《重組制品生產用哺乳動物細胞質量控制技術評價一般原則》《體外基因修飾系統藥學研究與評價技術指導原則》等生物制品指導原則的相關內容。
(一)
為了確保重組人源化膠原蛋白原材料質量可控,重組人源化膠原蛋白需參考相關行業標準進行必要的鑒別、純度和雜質等分析,可采用不同的分析方法對原材料的分子量、等電點、氨基酸序列、各種翻譯后修飾(如脫酰胺化、氧化、糖譜/糖基化修飾、脯氨酸羥基化等)進行充分鑒定,并進行相應的檢測,以確認終產物具有擬宣稱的原材料構象、聚集狀態、降解狀態及膠原蛋白高級結構。
材料理化特性分析需按照醫療器械制備工藝和特點,結合其風險控制要求進行相關研究,建議對如下常規理化項目進行研究,例如氨基酸序列、蛋白空間結構、劑型(如溶液、凍干粉、凝膠、纖維、海綿等)、膠原蛋白型別等特異性性能,同時結合醫療器械特點,完善理化性能指標要求。
需根據不同的預期用途及使用部位、不同生產工藝、預期使用效果和最終醫療器械的狀態,選擇適用的指標;根據膠原蛋白原材料是否經過交聯或化學修飾,宜提供交聯劑或修飾劑的殘留量、降解性能等的研究,提供相應的研究報告。
性能指標的建立及驗證取決于膠原蛋白原材料性質和用途、生產和純化工藝及生產工藝的經驗等多種因素。新的分析技術及對現有技術的改進正在不斷進行,適當時需使用這些新的技術。因現有技術原因而產生偏差的需進行合理性解釋說明。
首先需明確氨基酸序列的選擇依據,如為特定氨基酸序列片段組成的,還需明確片段重復次數及依據。需采用綜合的方法測定目標膠原蛋白原材料的氨基酸序列,并與其基因序列對應的理論氨基酸序列進行比較驗證。肽段覆蓋率的檢測結果需為100%覆蓋,末端氨基酸序列檢測結果需與理論序列完全一致。可按照《重組人源化膠原蛋白》行業標準的要求,直接使用供試品檢測,并選擇適宜的酶解條件進行水解,酶解后選擇不小于5個連續氨基酸的片段為基本的序列單元進行覆蓋分析。
如適用,目標膠原蛋白材料的理論氨基酸序列需包括二硫鍵連接方式。氨基酸序列測定還需考慮可能存在的N端甲硫氨酸(如大腸桿菌來源的膠原蛋白原材料),信號肽或前導序列。
使用各種水解法和分析手段測定氨基酸的組成,并與目的蛋白基因序列推導的氨基酸組成或天然異構體比較。如需要時需考慮分子量的大小。多數情況下,氨基酸組成分析對肽段和小蛋白可提供有價值的結構資料,但對大蛋白一般意義較小。在多數情況下,氨基酸定量分析數據可用于確定蛋白含量。
氨基酸末端分析用于鑒別N-端和C-端氨基酸的性質和同質性。用氨基酸序列分析儀或質譜法測定N端和/或C端氨基酸序列,其結果需符合理論預測。
若發現目的膠原蛋白材料的末端氨基酸發生改變時,需使用適當的分析手段判定變異體的相應變異數量。需將這些氨基酸末端序列與來自目的膠原蛋白基因序列推導的氨基酸末端序列進行比較。
按照《中華人民共和國藥典》 四部 通則 肽圖檢查法 第一法 胰蛋白酶裂解-反相高效液相色譜法進行測定,建立膠原蛋白原材料標準肽圖。
推薦利用四極桿飛行時間串聯質譜儀(Q-TOF MS)建立標準肽圖,作為膠原蛋白材料的指紋圖譜,用于材料的批間一致性和穩定性評價,以及材料特異性的鑒別。
需用合適的酶或化學試劑使所選的材料片段產生不連續多肽,應用高效液相色譜法(HPLC)或其他適當的方法分析該多肽片段。盡量應用氨基酸組成分析技術,N-末端測序或質譜法鑒別多肽片段。至少對材料成品放行來說,經驗證的肽譜分析經常是確證目的材料結構/鑒別的適當方法。具體分析方法可參考《重組膠原蛋白肽圖指紋圖譜分析》行業標準。
分子量
對申報醫療器械所用膠原蛋白材料可參照《中華人民共和國藥典》高效液相色譜法、“電泳法”的“第五法 SDS-聚丙烯酰胺凝膠電泳法”、基質輔助激光解析電離飛行時間質譜方法建立分子量及分布檢測方法,也可以運用其他適當技術測定分子量,如分子排阻色譜法等。需通過至少一種合理的、經驗證的方法證明其實際分子量與理論預測一致。
高效液相色譜法目標蛋白的出峰保留時間需與參比品一致;高分辨質譜法分子量需與參比品一致;SDS-聚丙烯酰胺凝膠電泳法分子量電泳條帶位置需與參比品一致。同時,需就參比品的選擇提供合理性依據。
按照《中華人民共和國藥典》 四部通則 電泳法第六法(等電聚焦電泳法)或0542毛細管電泳法進行檢測,等電點需在標示范圍內,也可以運用其他適當的方法測定。
如果目的膠原蛋白材料的基因序列存在半胱氨酸殘基時,需盡可能確定巰基和/或二硫鍵的數量和位置。使用方法包括肽譜分析(還原和非還原條件下)、質譜測定法或其他適當的方法。
多數情況下,可取目的膠原蛋白材料于UV/可見光波長處測定消光系數(或克分子吸光度)。消光系數的測定為使用UV/可見光或分光光度計檢測已知蛋白含量的溶液,蛋白含量應用氨基酸組成分析技術或定氮法等方法測定。
應用PAGE電泳、等電聚焦、SDS-PAGE電泳、免疫印跡、毛細管電泳法或其他適當的方法,獲得目的膠原蛋白材料的一致性,同一性和純度的電泳圖譜和數據。
色譜圖譜
應用分子篩色譜、反相液相色譜、離子交換液相色譜、親和色譜或其他適當方法,獲得目的膠原蛋白材料的一致性、同一性和純度的色譜圖譜和數據。
.結構表征
脯氨酸羥基化
若在設計時進行脯氨酸羥基化,需按YY/T 1849《重組膠原蛋白》中的要求進行分析,并規定標示值。
鑒于高級結構與重組人源化膠原蛋白表現出的性能和功能密切相關,若材料擬宣稱具有相應的高級結構,采用多種方法對高級結構進行研究分析,包括以下列舉的方法及其他結構表征方法,如冷凍電鏡、蛋白質晶體結構等方法。
1三螺旋結構分析
可采用圓二色譜在特定常規試驗條件下的檢測重組人源化膠原蛋白的CD光譜特征。若采用特定的非常規條件檢測,則檢測結果僅反映膠原蛋白材料在該條件下可(否)具有形成類似膠原蛋白三螺旋結構的CD光譜特征能力;此時需分析并闡述所檢測樣品是否代表“原材料樣品”,還是“原材料樣品”的特定處理(后續加工)樣品。同時建議進行最低檢出限分析,其結果需與生理性膠原蛋白相近(相差不超過一個數量級)。可采用X射線晶體學技術或冷凍電鏡技術在原子結構水平考證膠原蛋白材料或其包含的特定氨基酸序列的三螺旋結構特性,計算有結構信息的序列占整個蛋白序列的百分比;可采用差示掃描量熱法檢測膠原蛋白材料結構變化的熱效應輔助說明膠原蛋白的高級結構特征;可采用紅外光譜進行結構分析,其非特征區(如:酰胺a、b)和特征區(如:酰胺I、酰胺II、酰胺III)的特征峰位置需與參比品一致;可采用拉曼光譜,其拉曼光譜圖需與參比品一致;也可應用其它紫外或可見光吸收光譜法、核磁共振(NMR)等適當的方法檢測。
表征
若材料預期形成纖維/網狀結構時,宜使用掃描電子顯微鏡(SEM)、透射電子顯微鏡(TEM)或原子力顯微鏡(AFM)等方法觀察膠原蛋白材料形成膠原纖維束/多孔網狀結構等,需明確兩種方法具體的制樣和觀察測定過程。與此相關的膠原分子自組裝和聚合能力分析,可參考相關國內外相關標準進行研究。
.純度
關于純度的要求可根據醫療器械終產品的用途和用法而確定。存在二硫鍵時重組人源化膠原蛋白可能會形成寡聚體,且其電泳分子量大小需成倍增加,寡聚體需視為重組人源化膠原蛋白而非雜質。
.含量
需建立重組人源化膠原蛋白含量檢測方法,含量以質量/重量或質量/體積表示。含量檢測可通過液相色譜法(HPLC)、凱氏定氮法、特征多肽法等。
.雜質、污染物和添加劑
對膠原蛋白材料工藝相關雜質以及外源污染物等進行研究,如:細胞基質來源、細胞培養來源和下游工藝。需對潛在的工藝相關雜質(如宿主細胞蛋白質、宿主細胞DNA、細胞培養殘留物、下游工藝的殘留物等)進行鑒別、評估,并進行定性和/或定量分析,并采用適宜的方法評價其對生物學功能的影響。工藝相關雜質來源于生產工藝,可分三大類:來源于細胞基質、培養基和下游工藝。細菌內毒素、微生物限度和無菌性,是常規的污染物控制要求。
來源于細胞基質的雜質包括源于宿主生物體的蛋白/多肽;核酸(宿主細胞/載體/總DNA);多糖及病毒。對于宿主細胞蛋白,一般需用能檢測出較寬范圍蛋白雜質的靈敏的免疫檢測方法。需用不含目的基因的生物體粗提物,即不含膠原蛋白編碼基因的生產用細胞,制備上述試驗使用的多克隆抗體。可通過對膠原蛋白材料的直接分析方法(如雜交技術法)檢測宿主細胞的DNA水平,和/或通過標記試驗(實驗室規模)檢測證實通過純化工藝能去除核酸。對于有意導入的病毒,需驗證生產工藝中去除/滅活病毒的能力。
按照《中華人民共和國藥典》“外源性DNA殘留量測定法”的“熒光染色法”或“定量PCR法”進行測定,“熒光染色法”的樣品加標回收率需滿足70%~130%;“定量PCR法”的樣品加標回收率需滿足50%~150%,需規定殘留限量。如果樣品中外源性DNA殘留量低于“熒光染色法”的檢測限,則需采用“定量PCR法”進行測定。
需根據醫療器械產品的預期臨床用途、使用量等,確定含重組人源化膠原蛋白的材料臨床最大使用量的外源性DNA殘留量限值。推薦參考生物制品外源性DNA殘留限量要求,結合殘留DNA宿主類型及其風險程度設定每人每次最大使用量限值。
建議參考生物制品中大腸桿菌或酵母菌表達的基因工程重組生物制品的外源性DNA殘留量限度。
大腸桿菌蛋白質殘留量
按照《中華人民共和國藥典》“大腸埃希菌菌體蛋白質殘留量測定法”或采用經驗證的酶聯免疫試劑盒進行測定。
酵母蛋白質殘留量
按照《中華人民共和國藥典》“酵母工程菌菌體蛋白質殘留量測定法”或采用經驗證的酶聯免疫試劑盒進行測定。
CHO細胞蛋白質殘留量
采用經驗證的酶聯免疫試劑盒進行測定。
促炎性污染物(肽聚糖)
采用經驗證的方法或經驗證的市售細菌肽聚糖檢測試劑盒(ELISA)檢測殘留肽聚糖,需根據其致熱反應風險規定可接受的限量要求。
5.1.4碳水化合物結構
根據細胞基質等因素,必要時需考慮測定糖蛋白中碳水化合物的含量(中性糖、氨基糖、唾液酸)。此外,盡可能分析碳水化合物的結構、寡糖形態(長鏈狀)和多肽的糖基化位點。
來源于培養基的雜質包括誘導劑(多核苷酸,病毒)、抗生素、血清及其他培養基組分。需根據工藝中采用的表達體系和使用的抗生素類型,采用經驗證的方法測定殘余抗生素含量/活性,殘余抗生素含量需符合《重組人源化膠原蛋白》行業標準等相關標準,不應有殘余抗生素活性。
殘余抗生素含量的測定按照YY/T 1849《重組膠原蛋白》中描述的方法或其他經驗證的方法進行檢測,殘余抗生素活性按照《中華人民共和國藥典》 四部通則 生物活性測定法中抗生素微生物檢定法或《中華人民共和國藥典》 四部通則 抗生素殘留量檢查法進行檢測。
來源于下游工藝產生的雜質一般包括酶、化學/生化處理試劑(如溴化氰、胍、氧化劑和還原劑)、無機鹽(如重金屬、砷、非有色金屬離子)、溶劑、載體/配體(如單克隆抗體),及其他可濾過的物質。需結合實際情況制定相關理化指標。
如果使用了防腐劑、凍干保護劑等添加劑,需給出其限量要求和檢測方法。
需符合以下規定。
重金屬元素
對工藝中添加的重金屬元素,需符合規定限值。
重金屬含量
重金屬總量(以Pb計)需符合YY/T 1888《重組人源化膠原蛋白》行業標準等相關標準中的限值。
微量元素含量
微量元素含量:砷(As)、汞(Hg)、鉛(Pb)、鉻(Cr)、鎘(Cd)、銅(Cu)、鉬(Mo)、鐵(Fe)、鎳(Ni)需符合YY/T 1888《重組人源化膠原蛋白》等相關標準中的要求。
細菌內毒素相關限量要求需考慮醫療器械終產品與人體的接觸方式。
若重組人源化膠原蛋白材料以微生物限度控制狀態提供,按照《中華人民共和國藥典》 四部通則 非無菌產品微生物限度檢查:微生物計數法和非無菌產品微生物限度檢查:控制菌檢查法進行檢測,結果需符合相關要求。
若重組人源化膠原蛋白材料以無菌狀態提供,按照《中華人民共和國藥典》 四部通則 無菌檢查法進行檢測,結果需無菌。
需對重組人源化膠原蛋白材料的各種分子變異體進行分離、鑒別和分析。如變異體的功能與目標產物一致時可不做雜質考慮。需考慮在生產和/或貯存期間膠原蛋白材料降解產物是否顯著增加及其與免疫原性的相關性。以下為最常見的目的膠原蛋白材料的分子變異體,并列出了相應的檢測方法。
1化學修飾類型
各種非預期的翻譯后修飾是導致重組蛋白異質性的重要質量問題,如:脫酰胺化、氧化、糖譜/糖基化修飾等和其他可能的N端、C端修飾(如乙酰化、酰胺化或者由于外肽酶導致的部分降解以及C端加工、N端焦谷氨酸等),以及各種其他異質性(如異構化、碎片化、二硫鍵錯配、N-連接和O-連接的寡糖、聚集等)。適用時,需按YY/T 1849《重組膠原蛋白》中的要求,參照《重組膠原蛋白肽圖指紋圖譜分析》行業標準等相關標準進行分析。需考慮脫酰胺、異構化、錯配二硫鍵連接和氧化形式的分離和鑒別。對這些變異體的分離和鑒別,可采用層析法、電泳法(如毛細管電泳)、質譜法和/或光譜法(如圓二色譜)。需注意在修飾不會引起或只引起較小的分子量變化及結構變化的情況下,這些方法可能無法鑒別。此時,需要結合功能性試驗,評價所發生的修飾是否影響預期的功能和使用。
降解物和聚合體:聚合體包括二聚體和多聚體,可用分子篩層析法(如SE-HPLC)進行定量;需建立成品中非預期降解物的判定標準,并對穩定性試驗產生的降解產物進行監測。
.熱穩定性
如果重組人源化膠原蛋白是多聚體,可采用差示掃描量熱分析(DSC)進行解聚溫度分析。可參考《中華人民共和國藥典》 四部。
如果是單鏈的蛋白肽,可參考《中華人民共和國藥典》 四部,人免疫球蛋白3.3.2.4熱穩定性試驗,將供試品置(57±0.5)℃水浴中保溫4h后,用可見異物檢查裝置,肉眼觀察需無凝膠化或絮狀物。
它理化指標
膠原蛋白材料其它性能指標宜根據醫療器械終產品特性及相關通用要求制定,在適用時,需對相關性能指標檢測方法使用的參比品進行性能研究,對照品技術參數需明確且性能穩定。用于理化測定等方面的參比品,需進行必要的分析鑒定,包括但不限于:
用肉眼直接觀測,需為白色/淡黃色/無色透明液體或凝膠,或白色/類白色凍干粉或海綿狀固體。
注:隨著行業發展,可能存在其他外觀要求,需根據原材料具體形態規定外觀要求。
按照《中華人民共和國藥典》 四部通則 可見異物檢查法第一法(燈檢法)進行檢測,需無明顯異物。
需根據供試品的溶解特性,對供試品在水、稀酸或中性鹽溶液中的溶解程度進行表征和闡述。
7.4水分
適用時(如凍干樣品),需明確水分含量。除另有規定外,取供試品約1g~2g,按照《中華人民共和國藥典》“水分測定法”第二法(烘干法)測定,或取供試品約10mg按照《中華人民共和國藥典》“熱分析法”熱重法(TG)測定,升溫程序:從室溫以10℃/min速率升溫至105℃,保持60min。減失重量需符合所標示范圍。規定仲裁方法為水分測定法。
除另有規定外,取1.0-2.0g,按照《中華人民共和國藥典》 四部通則 熾灼殘渣檢查法進行檢測。
液體和凝膠樣品直接取樣,固體樣品用生理鹽水稀釋為1mg/mL,按照《中華人民共和國藥典》 四部通則“pH值測定法”進行檢測,需符合所標示值的±1.0。
適用時,液體和凝膠樣品直接取樣,固體樣品用生理鹽水稀釋為1mg/mL按照《中華人民共和國藥典》 四部通則 滲透壓摩爾濃度測定法進行檢測,滲透壓摩爾濃度范圍需符合相關標準要求。
取供試品按照《中華人民共和國藥典》“黏度測定法”的“旋轉黏度計測定法”測定,需要詳細描述試驗條件,動力黏度值需符合所標示范圍。
根據供試品性狀(溶液、凝膠、凍干海綿或凍干粉末等)和裝量的不同確定裝量的允差要求。例如:20g(mL)以下,單個裝量不低于標示裝量的93%;20g(mL)至50g(mL),單個裝量不低于標示裝量的95%;50g(mL)以上,單個裝量不低于標示裝量的97%;平均裝量不低于標示裝量。
8.降解特性及產物
需對膠原蛋白材料降解特性進行研究,可采用凝膠滲透色譜(GPC)測定降解產物的分子量分布及分子量,水解/酶解產物可使用氨基酸分析儀、高效液相色譜或其他適宜的方法測定。
9.生物學功能評價
重組膠原蛋白的生物學功能是指以重組膠原蛋白生物學特性相關屬性為基礎的生物學作用,對聲稱的生物學功能宜進行定性定量分析。膠原是細胞外基質的主要成分,重組人源化膠原蛋白作為重組膠原蛋白的一種,其主要生物學功能也同樣是為細胞提供支架和良好的微環境,如促進細胞黏附、增殖、生長、分化等。因此,可通過評價細胞-膠原蛋白相互作用來評價重組人源化膠原蛋白的生物學功能。細胞增殖、分化、黏附性、遷移或移行評價方法可參考YY/T 1849《重組膠原蛋白》。
由于膠原類材料在分子組成、微結構、物理性能方面可能差異顯著,需檢測材料與細胞之間相互作用及其引導細胞基礎響應的性能。細胞響應的參數包括細胞形態、面積和體積,均可通過二維(2D)或三維(3D)圖像技術可視化評價,還包括存活率、增殖率、程序化凋亡以及遷移。
鼓勵對重組人源化膠原蛋白對細胞的作用機理進行研究。例如,抗體阻斷試驗可用來確定細胞表面的何種受體參與了與膠原的作用,如整合素或盤狀結構域受體(DDRs)。此外,細胞骨架成分(如肌動蛋白)的協同作用也可用來評價細胞與基質間的粘附與收縮解離。有多種在單細胞或多細胞水平上評價細胞引導的收縮解離的方法,包括自由漂浮組織構建物的尺寸隨時間的變化、施加在培養-力學監測系統上力的大小,以及單個細胞在膠原網絡的應力和形變等。
其它適用于干細胞和祖細胞類型的細胞-膠原相互作用的功能性檢測包括細胞株的定向分化,特定干細胞或祖細胞的增殖,或組織形態發生(始于內皮祖細胞的血管形成)。按照《中華人民共和國藥典》 四部 進行成纖維細胞生長因子生物學活性測定,對膠原蛋白肽-細胞相互作用評價,反映膠原蛋白肽與成纖維細胞增殖的構效關系。
按照《中華人民共和國藥典》 四部 生物活性測定法對試驗結果進行統計學分析,包括對驗證指標結果的繪圖和統計學分析,以及判斷其是否符合可接受標準等。常規的統計學方法一般要求數據之間相互獨立,并呈近似正態分布和方差齊性,通常采用相對效價的對數轉換值進行數據分析。當無法滿足上述統計學要求時,也可考慮采用其他適宜的替代方法進行數據分析。
上述關于膠原—細胞相互作用的功能性測定也可作為醫療器械產品標準化和質量控制的方法。三維支架材料中細胞活性評價方法可參考YY/T 1562《組織工程醫療器械產品 生物材料支架 細胞活性試驗指南》。
(二) 安全性研究
臨床前安全性評價包括臨床前安全性試驗,其目的主要是確定新膠原蛋白材料是否會在人體引起未能預料的不良反應,免疫學安全性研究是重組人源化膠原蛋白材料生物安全性研究資料的主體。但是,用傳統生物試驗方法來評價重組人源化膠原蛋白往往有困難,并受多種因素的影響。例如高度的種屬特異性,人的蛋白質對人的生物學活性遠高于對動物的活性,而且人的蛋白質氨基酸序列,常常與來自其它種系的蛋白質不同,例如糖基。因而由基因工程技術所制備的蛋白質或肽類往往會在人體以外的其它宿主中產生免疫應答,其生物學效應有所改變,并可能因形成免疫復合物而導致有毒性反應,而這樣產生的毒性反應與人體安全性顯然無關。
另外,由于重組人源化膠原蛋白功能、生產工藝或者膠原蛋白材料穩定性等要求,對膠原蛋白材料進行修飾或者改構,需提供與未修飾或者改構材料比較的研究資料。以簡化生產工藝為目的而引入的額外多肽片段如His-tag,在最終的材料成品中需符合相關行業標準的要求。
基于部分人膠原蛋白核酸序列進行編輯組合而重組的蛋白質產物,特別是長期反復使用時,可能引起人體預測不到的免疫原性。因此,不能完全排除其免疫原性風險,宜增加免疫學研究。重組人源化膠原蛋白作為醫療器械用原材料,可采用適宜方法進行免疫學評價。若用動物進行免疫學試驗,可能因為動物模型與臨床應用之間存在種屬差異,帶來對評價試驗結果或評價試驗數據使用上的局限,需要根據臨床評價獲得的免疫學評價數據及動物模型獲得的免疫評價數據進行綜合評價分析。
患者對蛋白質類材料產生免疫應答的風險將隨醫療器械產品變化而變化。建議采用基于風險的方法來評價和減輕與影響人源化膠原蛋白安全性和有效性相關的免疫應答。人源化膠原免疫原主要源自生產過程中殘留的可致免疫原性的各種因子,包括殘留的各種雜蛋白(包括DNA轉錄過程中可能產生的異種蛋白)、殘留的大腸桿菌及酵母菌外源性DNA、材料致熱原、生產過程中菌體產生的細菌內毒素、DAMPs以及人源膠原特異性免疫等等。
為降低人源化膠原蛋白材料的免疫原性風險,一般需在材料設計及生產工藝中采取相應處理措施以降低其免疫原性,如宿主細胞選擇,蛋白提取、蛋白純化。注冊申請人需對其降低材料免疫原性的有效性進行驗證,并提供驗證試驗性數據或相關研究資料。注冊申請人需提供免疫原性檢測范例的理論依據,需使用經完全驗證的檢測法對來自關鍵性研究的樣品進行檢測,并提供支持該檢測法的全面驗證的數據。
雜蛋白的檢測可參考YY/T 1453《組織工程醫療器械產品 I型膠原蛋白表征方法》,外源性DNA檢測可參考YY/T 0606.25《組織工程醫療產品 第25部分 動物源性生物材料DNA殘留量測定法:熒光染色法》。膠原蛋白材料的免疫原檢驗可通過流式細胞術(FCM)或酶聯免疫吸附法(ELISA)測定,檢測試驗宜考慮,但不限于淋巴細胞增殖試驗(YY/T 0606.15《組織工程醫療產品 第15部分 評價基質及支架免疫反應的試驗方法:淋巴細胞增殖試驗》)、細胞遷移試驗(YY/T 0606.20《組織工程醫療產品 第20部分:評價基質及支架免疫反應的試驗方法:細胞遷移試驗》),采用非標方法時需進行方法學驗證。
免疫原性檢測可設計為檢測不期望的生物或生理結果的抗體,重組人源化膠原蛋白抗體可能降低效果或者引起過敏等反應。抗體檢測的免疫原試驗可參考《中華人民共和國藥典》,選擇適宜的方法進行,包括橋聯或均相酶免疫法、放射免疫沉淀試驗等,并進行相關的方法開發和試驗驗證。試驗過程中,可根據滴度試驗和中和活性試驗進一步對ADA進行分析,還可進行額外的抗體特征分析,包括抗體分型、抗原表位鑒定及交叉反應評價。
篩選檢測法(也稱為結合抗體(BAb)檢測法)用于檢測與材料結合的所有抗體。使用確證性檢測法建立BAb對材料的特異性,使用滴定和中和檢測法進一步表征重組人源化膠原蛋白抗體。使用滴定檢測法表征抗體應答的量級,抗體對安全性和有效性的影響可能與其滴度和持續性而不是發生率相關。中和檢測法評估抗體干擾材料-靶標相互作用的能力。中和抗體(NAb)是BAb的亞類,ADA對安全性和有效性的影響可能與NAb活性而不是抗體發生率相關。類似地,在一些情況下可能重要的是確定NAb滴度。用于檢測抗體的首選檢測法應當是檢測低親和力和高親和力抗體的高靈敏度篩選檢測法。注冊申請人在開發檢測方法以確認重組人源化膠原蛋白特異性抗體結合時,需選擇合適的確證性檢測法以防止抗體假陽性數據,這些假陽性數據會混淆抗體對安全性和有效性影響的分析。
注冊申請人需提供支持該檢測法的全面驗證的數據。驗證包括證明用于給定樣品中抗體的定量測量的特定檢測法對于預期用途是可靠和可重現的。抗體檢測法有助于評價材料的免疫原性,然而抗體的檢測依賴于檢測法的關鍵操作參數(如靈敏度、專屬性),一般來說,建議注冊申請人開發針對靈敏度、專屬性、選擇性、精確度、重復性和穩定性進行優化后的檢測法。
其他的免疫原評價及生物學性能及生物相容性評價等建議做醫療器械終產品的檢測,因為加工工藝不同最終產品性能不同,例如有些交聯工藝可能會封閉某些免疫原反應簇等等。
當擬生產醫療器械免疫原性風險與已上市產品無可比性,且無充分的文獻數據評價其免疫原性,需進行免疫毒理學試驗研究。通過免疫毒理學試驗,對炎癥反應、免疫抑制、免疫刺激、超敏反應以及自身免疫進行確證評價,評估免疫系統改變導致的潛在人體不良健康作用。
免疫毒理學可通過流式細胞術(FCM)、酶聯免疫吸附法(ELISA)、組織病理切片等方法測定,試驗方法可考慮結合生物學試驗、體外T淋巴細胞轉化試驗(YY/T 1465.1《醫療器械免疫原性評價方法 第1部分 體外T淋巴細胞轉化試驗》)等,注冊申請人需對選用檢測方法的適用性進行評價,采用非標方法時需進行方法學驗證。
可參考GB/T 16886.20《醫療器械免疫毒理學試驗原則和方法》選擇性進行功能性或非功能性免疫毒理學試驗,通過嚙齒動物試驗方式檢測和評價物質的不良作用。目前主要研究方法是將醫療器械/材料植入小鼠/模式小鼠,然后研究器械/材料整個降解周期內機體的體液和細胞的免疫應答,以及局部組織的免疫反應。功能性檢測測定細胞和/或器官活性,例如淋巴細胞對有絲分裂原或特異性抗原的增殖反應、細胞毒性和特異性抗體的形成;非功能性檢測涵蓋形態學方面和/或定量的術語、淋巴組織變化程度、淋巴細胞數目和免疫球蛋白水平或其他免疫功能標志物。
(三)
作為制備醫療器械產品的原材料,需參照GB/T 16886.1的要求對重組人源化膠原蛋白原材料進行必要的生物學評價,尤其通過膠原蛋白材料到醫療器械終產品的加工工藝分析發現,兩者之間的生物學風險相近時。如預期用于植入產品的原材料,還需評估樣品是否為內源性凝血系統激活物。若醫療器械終產品與膠原蛋白材料的使用方法不一致,需考慮生物學補充研究。
根據GB/T 42062《醫療器械 風險管理對醫療器械的應用》描述的風險管理過程進行生物學風險評定,識別材料、添加劑、加工助劑和其他潛在可瀝濾物中的危害,接觸劑量等因素,繪制基于風險管理的生物學評價流程圖。
如果醫療器械產品以非滅菌的方式提供,可將樣品滅菌后用于生物學評價試驗,需考慮滅菌方式及滅菌對重組人源化膠原蛋白的影響。
可能需要評價的生物學風險評定終點包括但不限于:
細胞毒性
致敏性
注射膠原、膠原止血劑等具有潛在生物可降解性材料,或體內植入材料以及材料制備過程中新增了化學成分和制造加工助劑、裝配粘合劑/溶劑殘留物,以及成品中可能存在滅菌殘留物或滅菌過程所致的反應性產物時,需進行遲發型超敏反應試驗。
皮膚刺激性
皮內反應
注射膠原、膠原止血劑等具有潛在生物可降解性材料或體內植入材料以及材料制備過程中新增化學成分和制造加工助劑、裝配粘合劑/溶劑殘留物以及滅菌殘留物或滅菌過程所致的反應性產物可能存在于成品時需進行皮內刺激試驗。
材料介導的致熱性
全身毒性
溶血性
血管修復材料、創傷和燒傷修復材料、膠原止血劑、心臟瓣膜等與循環血液接觸的外部接入材料和大部分植入材料以及全部植入血管系統材料需進行溶血試驗。
植入反應
皮下植入(膠原支架、血管修復材料、創傷和燒傷修復材料、膠原止血劑等可降解/可吸收材料或需植入生物材料等需進行皮下組織植入試驗進行評價);肌肉植入;骨植入。
9.遺傳毒性。
(四)
重組人源化膠原蛋白生產過程中間體如涉及到貯存,則需開展相應的穩定性研究。采用擬貯存階段樣品的代表性批次開展研究,一般包括貯存、運輸(如適用)和使用穩定性研究等。研究開展前,需統籌制定穩定性研究方案,關注各穩定性研究所用樣品、直接接觸性容器/材料、檢測時間點、檢測條件和分析檢項等。
研究中需對能夠反映質量變化的敏感特征進行研究,如含量、完整性、純度、微生物安全性和生物學特性等。需依據相應的醫療器械產品的貯存運輸條件開展研究,涵蓋設定的各項條件,如溫度、光照、反復凍融(冷凍貯存時)、振搖等方面。根據實際使用情況,開展使用中的穩定性研究,例如復溶或解凍、與復溶稀釋劑的相容性研究等。研究中需采用與實際使用相同材質的直接接觸性容器/材料。
如涉及貯存,需對直接接觸的包裝容器開展相應的包材相容性研究。根據相容性研究結果,結合穩定性研究,選擇合理的包裝容器。
另外,對制備工藝中與樣品接觸的容器和一次性使用材料(如貯存袋、過濾膜、層析介質、管路等),需開展風險評估和/或相應的相容性研究。
[1]中華人民共和國國務院.醫療器械監督管理條例:中華人民共和國國務院令第739號[Z].
[2]國家市場監督管理總局.醫療器械注冊與備案管理辦法:國家市場監督管理總局令第47號[Z].
[3]國家藥典委員會.中華人民共和國藥典:三部[M].北京:中國醫藥科技出版社,2020.
[4]YY/T 0954,無源外科植入物 I型膠原蛋白植入劑[S].
[5]YY/T 1453,組織工程醫療器械產品 I型膠原蛋白表征方法[S].
[6]YY/T 0606.25,組織工程醫療產品 第25部分 動物源性生物材料DNA殘留量測定法:熒光染色法[S].
[7]YY/T 1849,重組膠原蛋白[S].
[8]YY/T 1888,重組人源化膠原蛋白[S].
[9]YY/T1562,組織工程醫療器械產品生物材料支架 細胞活性試驗指南[S].
[10]GB/T 16886.1,醫療器械生物學評價 第1部分:風險管理過程中的評價與試驗[S].
[11]國家藥品監督管理局藥品審評中心.治療用生物制品非臨床安全性技術審評一般原則:2007年[Z].
[12]國家藥品監督管理局藥品審評中心.人用重組DNA制品質量控制技術指導原則:2003年[Z].
[13]國家藥品監督管理局藥品審評中心.特異性人免疫球蛋白藥學研究與評價技術指導原則:國家藥監局藥審中心通告2022年第27號[Z].
[14]國家藥品監督管理局藥品審評中心.重組制品生產用哺乳動物細胞質量控制技術評價一般原則:2007年[Z].
[15]國家藥品監督管理局藥品審評中心.體外基因修飾系統藥學研究與評價技術指導原則:國家藥監局藥審中心通告2022年第29號[Z].
[16]國家藥品監督管理局.重組膠原蛋白生物材料命名指導原則:國家藥監局通告2021年第21號[Z].
[17]U.S. Food and Drug Administration. Guidance for Industry: For the Submission of Chemistry, Manufacturing, and Controls Information for a Therapeutic Recombinant DNA-Derived Product or a Monoclonal Antibody product for in vivo use [EB]. 1996-08.
[18]U.S. Food and Drug Administration. Guidance for Industry: Immunogenicity Testing of Therapeutic Protein Products —Developing and Validating Assays for Anti-Drug Antibody Detection [EB]. 2019-01.
[19]European Medicines Agency. Guideline on similar biological medicinal products containing biotechnology-derived proteins as active substance: non-clinical and clinical issues [EB]. 2014-12-18.
[20]MEYER M. Processing of collagen based biomaterials and the resulting materials properties[J]. Biomedical engineering online, 2019, 18(1): 24-24.
[21]Rezvani Ghomi E, Nourbakhsh N, Akbari Kenari M, et al. Collagen‐based biomaterials for biomedical applications[J]. Journal of biomedical materials research. Part B, Applied biomaterials, 2021, 109(12): 1986-1999.
[22]Gentile, Ferreira, A. M, et al. Collagen for bone tissue regeneration[J]. Acta Biomater, 2012 Sep, 8(9):3191-3200.
[23]Schor SL. Cell proliferation and migration on collagen substrata in vitro[J]. J Cell Sci, 1980 Feb, 41:159-175.
[24]Somaiah C, Kumar A, Mawrie D, et al. Collagen Promotes Higher Adhesion, Survival and Proliferation of Mesenchymal Stem Cells[J]. PLoS One, 2015 Dec 14, 10(12): e0145068.
[25]Luparello C, Sirchia R. Type V collagen regulates the expression of apoptotic and stress response genes by breast cancer cells[J]. J Cell Physiol, 2005 Feb, 202(2): 411-421.
[26]Urlaub, G., Kas, E., Carothers, A. M., et al. Deletion of the diploid dihydrofolate-reductase locus from cultured mammalian-cells[J]. Cell, 1983, 33: 405-412.
[27]Cregg J. M., Vedvick T. S., Raschke W. C.. Recent advances in the expression of foreign genes in Pichia pastoris[J]. Biotechnology, 1993 Aug, 11(8): 905-910.
[28]Jeong, H., Barbe, V., Lee, C. H., et al. Genome Sequences of Escherichia coli B strains REL606 and BL21(DE3) [J]. Journal of Molecular Biology, 2009, 394(4): 644–652.
[29]Gussow D., Clackson T. Direct clone characterization from plaques and colonies by the polymerase chain-reaction[J]. Nucleic Acids Research, 1989, 17: 4000.
[30]Kubista M, Andrade JM, Bengtsson M, et al. The real-time polymerase chain reaction[J]. Molecular aspects of medicine, 2006, 27: 95-125.
[31]Cereghino, J. L., Cregg, J. M. Heterologous protein expression in the methylotrophic yeast Pichia pastoris[J]. Fems Microbiology Reviews, 2000, 24: 45-66.
[32]Cereghino, G. P. L., Cereghino, J. L., Ilgen, C., et al. Production of recombinant proteins in fermenter cultures of the yeast Pichia pastoris[J]. Current Opinion in Biotechnology, 2002, 13: 329-332.
[33]Hollenberg, C. P., Gellissen, G. Production of recombinant proteins by methylotrophic yeasts[J]. Current Opinion in Biotechnology, 1997, 8: 554-560.
[34]Barker, J. Material change[J]. Nature, 1988, 333: 310.
Gräslund Susanne, Nordlund Pär, Weigelt Johan, et al. Protein production and purification [J]. Nature Methods, 2008, 5(2): 135-146.
附件:重組人源化膠原蛋白原材料制造過程控制
附件
重組人源化膠原蛋白原材料制造過程控制
制造過程控制主要涉及工程細胞構建過程、生產用細胞的質量控制及常規生產過程控制。本附件特別關注了較為復雜的動物細胞生產體系,細菌與酵母的生產過程控制需首先符合中國藥典第三部中《生物制品生產檢定用菌毒種管理及質量控制》的要求。植物與昆蟲體系制造重組人源化膠原蛋白,可參考本附件中適用的內容并制定相應的控制要素。
一、重組工程細胞構建及生產用細胞的質量控制
重組人源化膠原蛋白屬于采用重組DNA技術,對編碼所需人膠原蛋白的基因進行遺傳修飾,利用質粒等載體將目的基因導入適當的宿主細胞,表達并翻譯成蛋白質,經過提取和純化等步驟制備而成的重組膠原蛋白之一。
(一)工程細胞的構建
1.宿主細胞的選擇、來源、歷史和一般特性
經過全面檢測的種子細胞是實現重組人源化膠原蛋白材料生產的前提和基礎。生產用種子細胞需具有共同的始祖細胞,保持相同的遺傳和生物學特征,在特定的培養環境和條件下持續穩定表達攜帶的外源目的基因。建議詳細闡述共同始祖細胞的判定標準。只有經過研究確定細胞在擴增培養和生產過程中的變化,才能夠有效控制風險性因素,滿足生產的持續需求,使膠原蛋白材料質量保持一致。
本附件中的宿主細胞主要涵蓋來自于人或動物的細胞系或者微生物細胞,動物來源的細胞系可來自所有后生動物,包括體外永生化的傳代細胞系以及有限傳代的二倍體細胞。微生物的來源包括細菌、真菌、酵母和其他單細胞生物。在宿主細胞選擇、重組工程細胞構建以及生產細胞的培養擴增和監控過程中,不僅要關注細胞的適用性、目的產物表達生產能力,同時還需重視伴隨細胞培養產生的內源性病毒、宿主細胞殘余蛋白和DNA、致腫瘤成分等潛在的風險性因素對重組人源化膠原蛋白材料帶來的安全性影響。在早期研究階段,需同步開展庫細胞、生產培養過程細胞、生產終末細胞的全面檢定和控制。針對哺乳動物細胞,需進行病毒和/或致瘤性成分的去除/滅活工藝的驗證。
需選擇來源、背景十分清楚的適宜宿主細胞,明確存在的內源性病毒和/或致瘤性等影響膠原蛋白材料安全性的因素,并結合膠原蛋白材料純化的程度、細胞培養和生產過程中風險性成分的去除/滅活能力及殘留量控制水平,以及臨床應用適應證和用法用量等特點綜合分析,經利弊權衡后確定與特定膠原蛋白材料相適應的宿主細胞。盡可能選擇致瘤性試驗陰性和低增殖代次水平的宿主細胞。對于改良的傳代細胞、全新構建的轉化細胞,甚至腫瘤細胞等,由于前期研究、背景資料和致瘤性風險等積累的認識有限,其開發應用將引入新的安全性隱患,需要慎重權衡利弊,確保遺傳背景清晰,在開展充分研究的基礎上嚴格控制其潛在的風險性。
用于構建重組工程細胞的宿主細胞其來源和培養歷史需足夠清楚,可溯源有關的背景資料。例如最初分離建立株/系的機構,在不同機構內引進和傳代經過,既往進行過的檢測分析項目和確證研究結果,細胞保存狀態,經體外傳代培養已達到的增殖代次/水平及傳代過程中所用過的人源或動物源性材料等。需提供宿主細胞來源的相關資料和證明性文件,說明是否曾進行過遺傳操作引入了外源基因序列,描述已進行過的研究檢定項目例如細胞鑒定、內源和外源性因子檢測等的結果及引進時進行的復核檢定結果。對于微生物細胞而言,需提供產生細胞系的物種、株和已知的遺傳和表型特征。如可能,還需提供其致病性、毒素產物和其他生物危害方面的資料。需說明所用細胞基質的細胞來源(實驗室制備或來源于菌種庫),引證科學文獻上的相關參考資料。直接從實驗室獲得的資料是首選的,如果沒有這些資料,也可以利用文獻。
需闡述宿主細胞的基本特征,如形態、培養和生長一般特征、培養條件和培養液要求,新構建的動物細胞系需檢測致瘤性特征。對宿主系統(原核、真核、哺乳細胞等)的特性、遺傳背景、基因型、表型、抗性、質粒轉化條件特征都需有詳細的文獻或實驗資料。基本特征信息舉例如表1。
表1 宿主細胞基本特征信息表(舉例)
|
細胞株名稱 |
Chinese Hamster Ovary (CHO) |
Pichia pastoris |
Escherichia coli |
|
出品公司 |
Sigma |
Invitrogen |
Invitrogen |
|
宿主系統類型 |
中國倉鼠卵巢細胞 |
畢赤酵母GS115 |
大腸桿菌 BL21(DE3) |
|
生長條件 |
36.5℃,有氧 |
28℃,有氧 |
37℃,兼性厭氧 |
|
質粒轉化條件 |
電轉 |
電轉 |
電轉 |
|
基因型 |
Wild type |
His4 |
F-ompT hsdSB(rB-mB-)gal dcm rne131(DE3) |
2.宿主細胞鑒定
宿主細胞(原核、真核、哺乳細胞等)污染和營養缺陷表型(或基因敲除)、過表達及導入外源基因等鑒定檢測方法都需有詳細的文獻或實驗資料。舉例如表2。
表2 宿主細胞鑒定項目(舉例)
|
檢測項目 |
檢測方法 |
質量標準 |
|
污染 |
平板劃線,顯微鏡檢測、支原體檢測試劑盒 |
無污染 |
|
營養缺陷表型鑒定 |
營養缺陷平板生長鑒定 |
不生長 |
|
甲醇利用性 |
含甲醇的平板生長鑒定 |
符合菌株表型 |
|
導入外源基因鑒定 |
PCR擴增,產物測序 |
符合菌株基因型 |
|
過表達基因鑒定 |
qPCR檢測過表達基因轉錄水平 |
符合菌株表型 |
3.重組工程細胞克隆構建過程、篩選及相關鑒定
工程細胞的構建一般包括基因獲得、質粒構建和表達體系構建三個階段。舉例如圖1。
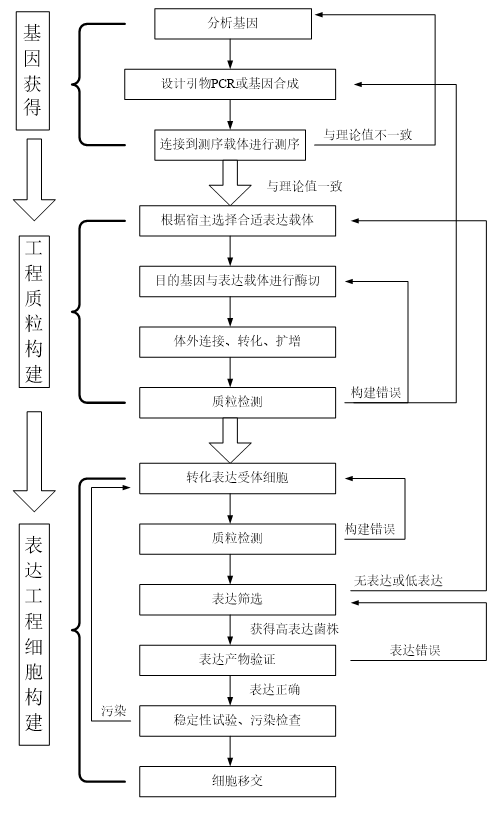
圖1 工程細胞構建一般流程
目前可采用多種表達載體、宿主細胞、基因導入方法和篩選標記等進行工程細胞的構建和篩選,構建成功的標志是工程細胞能夠穩定、高效地表達結構正確且具有生物活性的目的產物,包括共表達的產物。因此,需盡可能提供關于重組工程細胞構建和鑒定的詳細資料,重點描述的內容舉例如表3。
表3 工程細胞鑒定項目(舉例)
|
檢測項目 |
檢測方法 |
質量標準 |
|
工程質粒線性化 |
核酸電泳法 |
單一條帶,大小正確 |
|
線性質粒純化 |
紫外分光光度掃描 |
DNA濃度不低于100ng/μL;OD260/280=1.8~2.0 |
|
轉化表達受體細胞 |
平板篩選,PCR擴增產物測序 |
測序結果正確 |
|
表達鑒定 |
SDS-PAGE電泳考馬斯亮藍染色法 |
分子量符合預期 |
|
免疫印跡法 |
分子量符合預期 |
|
|
水解氨基酸測定 |
氨基酸組成正確 |
|
|
表達篩選 |
SDS-PAGE/Western bloting/酶聯免疫吸附法(酵母除外) |
按表達量前5%選擇 |
3.1目的基因來源及插入目的基因的設計
需包括最初獲得目的基因序列的來源和背景方面的資料,包括但不限于用于制備目的基因cDNA的方法,以及必要的初步序列分析。
需根據人膠原蛋白的氨基酸序列和學術研究,檢索公開數據庫,如美國國立生物技術信息中心(National Center for Biotechnology Information,簡稱NCBI)生物信息數據庫(http://www.ncbi.nlm.nih.gov/)、公開發表的蛋白質學術論文等,獲取人膠原蛋白的氨基酸序列及其對應的核酸序列,包括全長人氨基酸序列、片段人氨基酸序列、片段重復人氨基酸序列等。衡量目的基因質量時至少需考量下述項目:
表4 衡量目的基因質量的項目(舉例)
|
檢查項目 |
檢測方法 |
質量標準 |
|
目標序列 |
DNA測序 |
測序結果正確 |
|
限制性酶切 |
核酸電泳法 |
插入片段大小正確,無預期外片段 |
|
DNA質量 |
紫外分光光度掃描 |
OD260/280=1.8~2.0 |
根據所選的核酸序列及質粒進行插入目的基因的設計,明確插入位點、標簽序列或分泌表達信號肽。將目的插入序列翻譯成氨基酸序列,需提供該序列與人膠原蛋白氨基酸序列比對圖。帶有非膠原蛋白設計與修飾(標簽、抗性等),則需提供具體序列及修飾位點,最終產物的膠原蛋白序列與修飾需符合相關行業標準的要求。
3.2載體選擇與重組質粒的構建
需詳述表達載體構建或改建的過程,對構建成功的表達載體需進行必要的鑒定,并提供相關試驗資料如構建中所用位點的酶切圖譜等。根據設計的重組人源化膠原蛋白氨基酸導入宿主細胞的不同,選擇合適的質粒以滿足目標克隆的構建,并提供質粒的完整序列信息。舉例如下:
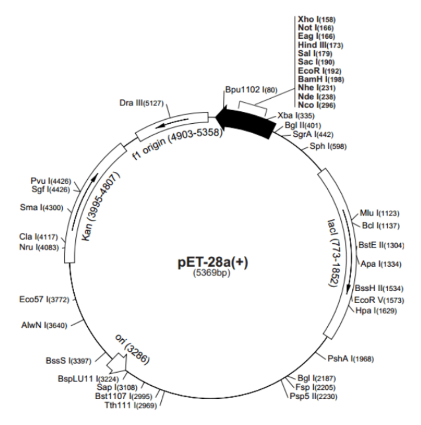
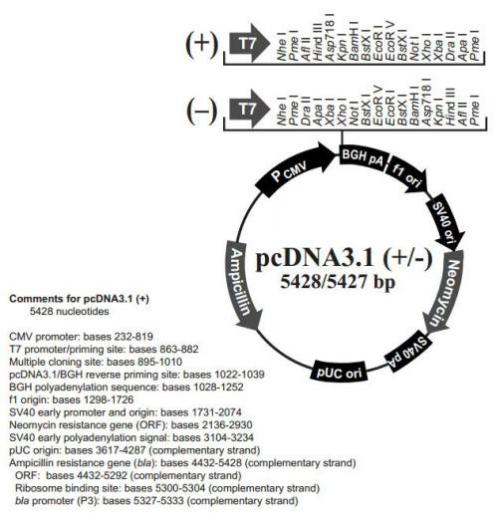
圖2 完整的質粒信息示例
需提供有關表達載體詳細資料,包括基因的來源、克隆和鑒定,表達載體的構建、結構和遺傳特性。需說明表達載體組成成分以及主要元件的來源和功能,包括插入基因和側翼區序列、復制子、啟動子、增強子、抗性標記以及主要的酶切位點等。提供至少包括構建中所用位點的酶切圖譜。
將目的基因序列插入質粒中時,為保證重組質粒構建正確,需提供重組質粒至少含目的插入基因完整開放讀碼框的測序報告,并提供測序序列與設計序列的比對結果,二者需一致。需提供插入基因和表達載體兩側端控制區的核苷酸序列。所有與表達有關的序列均需詳細敘述。主要質量控制參數舉例:
表5 目的基因序列插入質粒過程中的主要質控參數(舉例)
|
檢查項目 |
檢測方法 |
質量標準 |
|
限制性酶切驗證 |
核酸電泳法 |
插入片段大小正確,無預期外片段 |
|
目標序列 |
DNA測序 |
測序結果正確 |
|
DNA質量 |
紫外分光光度掃描 |
OD260/280=1.8~2.0 |
需明確質粒與菌種/細胞的儲存條件,例如質粒溶液為-20℃,甘油菌為≤-60℃,等等。
3.3載體引入宿主細胞的方法及重組工程細胞的篩選
需詳細說明載體引入宿主細胞的方法和操作過程,重組工程細胞的篩選原理、條件和標準,以及采用何種方法增加基因拷貝數等。闡述外源基因引入宿主細胞后產生的變化,符合篩選標準的候選細胞可能為多個細胞株,但擬用于建庫的細胞株需為經研究比較后確定的單一細胞克隆。
3.3.1載體引入宿主細胞的方法
非病毒載體類基因修飾系統可通過物理、化學或生物轉導方式遞送進入細胞。進入目的細胞后,通過轉錄、剪切、翻譯等方式發揮作用。
外源基因導入受體細胞有多種方法,宿主細胞類型不同,載體不同,導入方法也有差異。舉例如大腸桿菌屬于原核生物,常用的是熱擊轉化方法,將重組表達載體DNA分子轉化至感受態細胞。酵母生長較迅速且細胞分散,常用的酵母細胞轉化方法包括氯化鋰、電穿孔、基因槍和玻璃珠方法。這些方法常用于釀酒酵母,但也可用于其他真菌轉化,如酵母(例如粟酒裂殖酵母、白色念珠菌和畢赤酵母)和絲狀真菌(例如曲霉屬菌種)。將外源DNA導入哺乳動物細胞的轉染方法包括磷酸鈣轉染法、DEAE葡聚糖轉染法、原生質體融合、電穿孔、脂質體和胞核微注射法等,各種轉染方法的作用機制、轉染效率和優缺點各不相同。
若采用基因編輯系統,建議對靶向序列、目的基因序列和基因編輯用酶等的序列和比例等進行優化。通過特定細胞中的基因編輯效果確認基因編輯用酶和靶向序列的特異性,篩選最佳的靶向結合序列(如sgRNA序列),并采取措施降低基因脫靶、插入突變的概率及對目的細胞基因組穩定性的不良影響。對于轉座子系統,建議考慮整合位點的特異性和分布趨勢,以及轉座子在基因組中的移動(genomicmobilization)等特征,進行轉座子序列、轉座酶及相應調控元件的優化,合理設置轉座序列/轉座酶的比例、序列分布等。
3.3.2重組工程細胞的篩選
需檢測重組后細胞基本性狀的改變,比較研究插入外源基因后細胞致瘤性特征的改變。需說明表達載體在宿主細胞內的狀態(是否整合到染色體)并采用適宜的方法測定其拷貝數,需提供宿主和載體結合后的遺傳穩定性資料。說明啟動和控制目的基因在宿主細胞中表達所采用的方法,并進行初步的表達產物鑒別和表達水平檢測。
對于選定的工程細胞株需進行充分的目的基因全序列確認,以保證用于編碼和表達目的產物的基因在初始核酸序列上的正確性。需詳細敘述在生產過程中,啟動和控制克隆基因在宿主細胞中的表達所采用的方法及表達水平。
3.4合成表達系統構建過程中關鍵質量控制
此過程的質量研究通常包括鑒別、結構特征、理化特性、生物學活性、純度和雜質分析等,建議采用多個代表性批次開展研究。
3.4.1鑒別和序列確認
鑒別研究中,可采用限制性內切酶進行酶切,對酶切產物進行電泳分析,觀察是否存在特征性的帶型;也可以用PCR方法進行擴增,分析片段大小是否與理論大小一致等方法。序列確認研究中,建議開展全序列測定,重點關注目的基因和調控元件的序列正確性。
3.4.2結構
建議采用適用的方法對結構完整性和大小均一性進行研究。如對于DNA,可關注其是否存在單鏈、雙鏈、線性/開環、環狀和超螺旋等多種結構形式,以及可能的高級結構等。
3.4.3理化特性
建議開展分子量、核酸濃度/含量、修飾位點及比例(如有)、物理特性(如pH、滲透壓)等方面的研究。
3.4.4生物學活性
根據作用機制,生物學活性研究通常包括對基因修飾效率、目的基因表達的水平、表達產物的功能或體外模擬生理功能的測定等。建議首選定量檢測方法,如可通過目的基因或基因編輯產物的表達量和功能進行分析,關注表達產物是否與預計一致或蛋白表達/基因是否被抑制、空間結構是否符合設計(如多聚體)等。當采用體外轉染檢測細胞的方法時,需關注選擇的檢測細胞是否具有代表性和合理性。
3.4.5其他特性研究
對于使用基因編輯工具酶的修飾系統,質量研究中建議持續關注對應細胞中修飾系統的殘留情況,采用生物信息學工具分析靶細胞基因組結構變化、單點和小規模基因突變以及外源DNA在基因組中的插入位置、拷貝數等,監控基因編輯用酶的細胞內持續表達時間,考察脫靶效應及相應的安全性影響等。對于制備過程中使用的酶類試劑,建議重點關注酶的功能活性,例如需關注所用DNA聚合酶的保真度和活性,消化酶的酶解作用、酶的非特異性消化條件等,同時需要關注酶的純度、生產過程中引入的雜質等。對于核苷酸、5’-帽或帽類似物等原材料,其整體的質量需符合制備的要求,建議關注鑒別、濃度、純度和雜質等。制備過程建議避免使用氯化銫、溴化乙錠、氯仿等毒性物質,避免使用動物源胰蛋白胨、核酸酶等可能引入外源因子等風險的原材料。對于用作遞送系統的材料,其制備涉及的關鍵原材料(脂質、陽離子聚合物等)需進行充分的篩選和質量控制。
(二)生產用細胞的質量控制
連續傳代細胞生產重組人源化膠原蛋白材料的最大優點是使每批膠原蛋白材料都有一個經過檢定的共同起源細胞,因此建立細胞庫的目的就是為了保證生產的可持續性和膠原蛋白材料質量的穩定。重組人源化膠原蛋白材料的生產必須建立在有良好的細胞庫管理基礎上,載體細胞可以是細菌、酵母或其他真核細胞,已通過篩選、育種、復蘇等程序驗證建立細胞庫而實現工程化,具有穩定的遺傳表達和相應的質量控制體系。本部分以針對動物細胞庫的管理為例,進行相關闡釋。
需建立細胞庫系統(細菌、酵母、哺乳細胞等其他)保存管理的相應制度及文件,保證細胞庫符合相關標準要求,保障細胞庫的穩定性,需對細胞庫進行質量檢測,包括質粒核酸序列、拷貝數、丟失率檢測;雜菌檢測(計數、菌落形態觀察、菌種鑒定)等;需提供細胞庫檢測報告。
1.細胞庫建立
細胞庫可為三級即原始細胞庫、主細胞庫(MCB)和工作細胞庫(WCB);也可采用主細胞庫和工作細胞庫組成的兩級細胞庫;在某些特殊情況下,也可使用主細胞庫一級庫。用于建庫的初始工程細胞株需為經過克隆選擇而形成的均一細胞群體,必要時須經與實際生產過程所用培養基和培養條件相一致的適應性培養。
2.建庫細胞的管理
在制備工作細胞庫過程中不得進行單克隆篩選,以避免由于個別基因突變引起工作細胞庫中細胞群體性的遺傳特性改變;為了保證細胞庫中每個容器中的內容物完全一致,如培養細胞采用幾個器皿的,需將所有培養皿中的細胞混合成單批后再分裝。
在細胞庫的建庫期間需采取適宜的預防措施,以確保細胞不被污染(包括微生物污染和實驗室中其他類型細胞的交叉污染等)。各級種子庫的細胞需按照特定的要求經過全面檢定合格后方可使用(具體要求參見本文細胞庫檢定)。
動物細胞庫建庫的具體過程、方法和管理需符合中國藥典要求。
3.細胞庫檢定
正確的起始細胞是實現良好生產的前提和基礎。檢定的目的是為了確認經過初步篩選建庫的細胞符合預期設計要求,攜帶有穩定的目的基因,能夠持續表達有功能活性的目的產物,沒有微生物污染和混雜其它細胞,能夠直接擴增儲備或者應用于生產。
對于原始庫細胞和/或主庫細胞,通常需要進行一次全面系統的研究檢定,包括遺傳學、生物學和微生物學,以便從源頭開始嚴格控制起始細胞的一致性和防止污染。經過傳代穩定性研究的主細胞到工作細胞,只經過簡單的傳代、擴增,可以適當簡化檢定項目,重點檢測外源因子污染和防止混入了其它細胞。保存的數目和傳代水平需保證生產用細胞的持續穩定供應。
3.1細胞鑒定
要進行目的蛋白表達穩定性分析,即確證表達產物的蛋白質序列與預期相符。
表6 目的蛋白表達穩定性分析(舉例)
|
檢查項目 |
檢測方法 |
質量標準 |
|
表達穩定性 |
SDS-PAGE電泳考染法 |
與供試品一致 |
|
含量 |
紫外分光光度掃描 |
不低于初始工程菌 |
|
污染檢測 |
顯微鏡檢測、支原體檢測試劑盒 |
無污染 |
3.1.1細胞種屬的鑒定
需驗明細胞的種屬來源,分析細胞的同一性,排除與其它細胞的交叉污染。鑒別試驗可利用細胞的表型或遺傳型特征,通常對MCB作鑒別試驗,而對每個WCB僅作有限的鑒別試驗。
目前常用的方法有細胞生長特征和培養形態學檢查、種屬特異性抗原檢測、染色體核型分析、同工酶分析、限制性內切酶分析、基因多態性分析等。需結合具體細胞固有的特性進行適宜的組合和選擇,以實現正確鑒別為目的。
真核細胞用于生產時,細胞的鑒別標志,如特異性同功酶或免疫學或遺傳學特征,對鑒別所建立的種子是有用的。有關所用傳代細胞的致癌性需有詳細報告。如采用微生物培養物為種子,則需敘述其特異表型特征。
3.1.2致瘤性試驗
對于動物細胞,需檢測分析目的基因引入細胞后的致瘤性特征,對于陽性細胞,需研究確定致瘤性改變對膠原蛋白材料帶來的安全性風險。種子批不應含有外源致癌因子。
3.1.3目的基因和表達框架分析
目的基因和表達框架的確證是種子庫細胞檢定的重要組成部分,對于表達正確的目的產物具有先決性意義。常用的方法包括:通過PCR擴增樣本DNA來進行DNA序列分析;通過限制性內切酶譜和Southern雜交來檢測基因的完整性,確定目的基因的拷貝數,并檢測是否有任何序列插入或缺失等。
基因序列分析資料需包括試驗方案和步驟、原始的測序圖、測得序列以及翻譯后的氨基酸序列,同時需將實際測得序列與理論序列進行對比。清楚標注兩者之間的異同。一般情況下,在原始種子階段需確證克隆基因的DNA序列。但在某些情況下,例如傳代細胞基因組中插入多拷貝基因。在此階段不適合對克隆基因作DNA序列分析。在此情況下,可采用總細胞DNA的雜交印染分析,或作mRNA的序列分析。對最終膠原蛋白材料的特征鑒定需特別注意。
為保證膠原蛋白材料結構的正確和穩定,基因序列分析需貫穿于重組工程細胞的篩選和鑒定、細胞庫的建立和檢定以及生產細胞培養監控的全過程。
3.1.4表達產物檢測
需檢測分析目的產物的表達量和生物活性。活性測定需選擇與其預期用途相對應并能夠定量的方法。活性測定方法學研究可貫穿于重組人源化膠原蛋白原材料研究的始終,并經相關驗證分析。
3.2微生物污染檢測
3.2.1細菌、真菌和支原體檢查
對于動物細胞庫,需對MCB、WCB和EPC(生產終末期細胞)進行全面檢查,對生產培養過程中的細胞進行監測。在進行支原體檢查時,需注意同時進行培養法和指示細胞法兩種方法,或經驗證的qPCR法。必要時可采用掃描電鏡法檢查細胞是否受到特殊微生物的污染。在設計檢測微生物細胞庫中外源微生物因子和外源細胞污染的特異性試驗方法時,需考慮以下問題:建庫細胞的性質、科技文獻中報道的可能存在的污染、用于細胞培養的細胞來源、方法和材料以及存在于建庫實驗室中的其他生物等。
3.2.2病毒因子的檢查
包括細胞來源宿主動物潛在的內源性病毒和由于操作帶入的外源性病毒的檢查。對細胞進行病毒檢查的種類和方法,需根據細胞的種屬和組織來源、傳代歷史和細胞特性選擇。
3.2.1.1體外試驗
需將MCB、WCB和EPC細胞活細胞或細胞裂解產物接種到盡可能多的病毒易感的指示細胞上。可以根據細胞來源,傳代史和細胞培養基的原料使用情況來選擇適宜的指示細胞。檢測結果需為陰性。
3.2.1.2體內試驗
通過接種乳鼠、成年小鼠、雞胚、豚鼠、家兔或其它敏感動物來檢測細胞培養物中潛伏性病毒。通常要對MCB、EPC進行體內試驗。
3.2.1.3種屬特異性病毒的檢定
通過抗體產生試驗來檢測可能存在于MCB細胞中的種屬特異性病毒,如嚙齒類動物來源的細胞需進行小鼠、倉鼠或大鼠的抗體生成試驗。嚴格控制對于人類有危害的鼠源性病毒。
3.2.1.4逆轉錄病毒的檢測
逆轉錄病毒的試驗需包括感染性試驗、逆轉錄酶(RT)檢測和電鏡技術檢查。需采用上述方法對MCB和EPC細胞進行逆轉錄病毒的檢測。
3.2.1.4.1感染性試驗
需根據細胞的特性及可能存在的逆轉錄病毒種類選擇適宜的檢測方法,如XC空斑試驗(XC plaque)、延時XC空斑試驗、S + L - 灶點分析(S + L - Focus)等。試驗時需注意設立恰當的陰/陽性對照。
3.2.1.4.2逆轉錄酶檢測
為提高檢測的敏感性,通常需要將受試細胞經適當的化學誘導劑誘導后,收集上清液分別與檢測細胞聯合培養,再檢測逆轉錄酶的活性,注意設立恰當的陰/陽性對照。
3.2.1.4.3透射電鏡檢查
透射電鏡下可觀察細胞基質超微結構的形態學特征以及逆轉錄病毒和病毒樣顆粒的存在,需比較未經和經過化學誘導劑誘導的細胞。另外,需要對細胞培養液超速離心后所得的沉淀物經負染后進行檢查。觀察有無逆轉錄病毒顆粒以及顆粒的類型。
上述三種方法具有不同的檢測特性和靈敏度。因此,需采用不同的方法聯合檢測。若逆轉錄酶活性檢測陽性時,建議進行透射電鏡檢查或感染性試驗,如果確證對人或者其它靈長類動物細胞有感染性的逆轉錄病毒顆粒,該細胞不可用于生產。
4.細胞穩定性研究
需包括庫細胞、生產過程中細胞、生產終末期和/或超過生產終末期等不同培養時期的細胞。庫細胞需重點考察貯存、復蘇等操作處理因素的影響和傳代過程中的遺傳穩定性,在此基礎上確定庫細胞傳代限度,也需基于質粒拷貝數及其在載體細胞內的狀態限定生產過程中載體細胞的最高傳代次數,驗證試驗所涉及的傳代范圍需等于或超過規定的細胞最高限定代次。生產過程中細胞、生產終末期和/或超過生產終末期細胞需考察模擬生產工藝和培養條件對細胞生長狀況、表達能力等的影響,并確定生產細胞增殖限度和/或連續培養時間;使細胞始終能夠持續、穩定地表達重組人源化膠原蛋白,并將對最終膠原蛋白原材料產生安全性影響的風險因素嚴格控制在最低限度。
4.1貯存條件下的穩定性
當儲存的細胞復蘇后用于生產膠原蛋白材料時,需進行細胞存活率和功能活性等與細胞質量密切關聯項目的研究測定,以證實復蘇細胞表達能力的穩定性,需有對建庫細胞貯存條件下穩定性監測的方案。這種監測需在一支或多支冷凍保藏的WCB復蘇后制備生產用細胞時進行,或當一支或多支冷凍保藏的MCB復蘇并用于制備新WCB時進行。如果長時間未進行生產時,需按上市申請時所述的間隔時間對生產用細胞庫進行活力測試。如果細胞的活力沒有明顯的減退,一般不需對MCB或WCB作進一步檢定。
4.2傳代/擴增過程中的穩定性
需對庫細胞和生產過程細胞進行傳代/擴增的穩定性研究,可將復蘇的庫細胞連續傳代培養至一定的代次和將工作庫細胞在模擬實際生產條件下連續培養、擴增(逐級放大擴增過程),直至預期培養時間以及超過預期時間之外的延長時間點,收獲后進行檢測分析。通過考察目的基因、表達框架等在重組工程細胞中的傳代穩定性和目的產物表達的穩定性,制定庫細胞的限傳代次和生產細胞的增殖限度以保證實際生產過程中細胞整體擴增水平以及伴隨的內源性病毒和/或致瘤性風險等的抑制狀態在預期限度范圍內。至少需包括以下方面的試驗研究:
4.2.1基因水平的比較
目的基因編碼序列和表達框架不應有錯誤,包括突變、缺失、插入。并注意比較基因拷貝數的變化。
4.2.2目的產物表達水平的比較
目的產物的表達量和表達活性不應有明顯降低,根據不同的重組人源化膠原蛋白和具體研究結果確定適宜的可接受標準。
4.2.3細胞自身的穩定性
需重點檢測細胞在傳代/擴增過程中的形態、生長、代謝等基本狀況,遺傳特征和致腫瘤特性的變化。
4.2.4內源因子檢查
需動態考察內源因子的復制是否得到有效抑制。重點檢測由細胞來源動物和宿主細胞特性所決定的易染病毒如內源性逆轉錄病毒,分析其對于人類的致病性和重要性,嚴格控制其產生的條件。
4.2.5致瘤性監測
對于致瘤性試驗陽性的細胞,尤其對動物細胞,需通過比較研究考察細胞培養傳代過程中致瘤性特征的改變,例如試驗陽性時的細胞代次、最低接種量、腫瘤轉移擴散、腫瘤增殖時間、瘤組織病理特征等。建議對不同劑量(低、中、高)進行不同宿主細胞的致瘤性試驗,直至篩選出低致瘤性細胞。
5.生產過程細胞質量控制
種子庫細胞需在全面質量研究和檢測分析基礎上,模擬實際生產過程進行擴增培養,并檢測分析目的基因表達的穩定性、細胞生長狀況、污染控制、致腫瘤風險性等;規模化生產后須建立細胞生產培養過程的監控標準,生產細胞培養終末期需符合質量控制相關要求。
對于內源性逆轉錄病毒和/或致瘤性試驗陽性的細胞,需依據工藝處理能力制定風險性成分的控制條件,并根據模擬生產狀態下取得的試驗研究數據制定廢棄收獲液的標準;生產工藝須包括有效的病毒和/或致瘤性成分的滅活/去除方法并經過充分驗證。
如果整個培養過程中的關鍵環節例如培養基、培養條件、培養時間和/或限制代次、培養方式等發生重大改進,細胞培養工藝進行了放大,影響了原已確定的監控標準,需重復進行一次全面的檢測驗證。
5.1常規生產過程監控
經研究確定了生產工藝條件之后,常規生產過程中可重點監測微生物污染和細胞生長狀況,例如活細胞數目和形態、代謝和功能狀態、目的蛋白表達狀況、潛伏性逆轉錄病毒基因組激活狀況、細菌和支原體污染以及其它要求等,在比較分析的基礎上確定批次或者連續培養生產的終末細胞的檢測項目及可接受標準。
5.2細胞增殖限度
在細胞穩定性試驗研究的基礎上,需結合細胞培養、維持等工藝過程中實際采用的生產方式如批式培養(batch culture)、流加培養(fed-batch culture)、灌注培養(perfusion culture)等各自特點,考察細胞體外連續擴增、培養過程中發生的變化,例如細胞的生長狀態、內源性病毒抑制狀態、目的蛋白表達的下降程度以及致瘤性改變等確定適宜的收獲方式、收獲時間、細胞終止培養時間和/或增殖代次,并預留充分的安全儲備。實際生產過程中細胞不得超過預先設定的培養時間和/或增殖限度
5.3其它風險性因素控制
培養基對細胞的質量有直接的影響,也是細胞污染的可能來源之一。需明確培養基的組成、來源及質量標準。對于動物源性添加成分,需盡可能控制并減少其使用;如確需使用,需闡明選擇的理由,并說明該成分的來源和病毒安全性控制方法。目前提倡采用無血清培養基,并盡可能減少用于處理細胞(例如從貼壁狀態中游離或者分散)的動物來源的蛋白酶。各種培養基的來源和質量檢測數據均需有可追溯的文件記錄。如培養中使用了牛源性物質,需明確其來自非BSE疫區,并需按照國家食品藥品監督管理局的相關規定提供必要的證明性文件。
細胞培養條件的研究中,需考察使內源性逆轉錄病毒復制和癌基因相關序列激活或者復制受抑制的控制條件,對模擬生產條件下的狀況進行分析,確定可實際控制的程度。生產中需嚴格執行研究確定的控制條件。
6.風險評估與控制
細胞系/庫的建立,其序列的設計、生產用材料、制備工藝、質量、穩定性、內包材的要求可依具體情況,結合細胞系/庫的質量研究結果進行綜合評估。可結合生產使用情況和細胞系/庫的研究和檢測情況,制定重組人源化膠原蛋白原材料的風險控制策略。良好的重組人源化膠原蛋白原材料質量研究與控制有利于篩選、建立出質量良好的細胞系/庫,有利于后續的生產研究。在細胞系/庫建立過程中,建議對細胞系/庫進行檢定和傳代穩定性研究,關注細胞系/庫功能是否符合理論設計和預期、安全是否可控,必要時對工程細胞進行相應的質量研究,以確認其適用性。
隨著技術不斷更新和研究經驗的逐步積累,研發過程常常伴隨重組人源膠原合成表達系統的升級和工藝的優化,因此研發各階段有可能發生變更。系統的變更可能顯著影響工程細胞的安全性和有效性,是重要風險之一,研發者需評估變更引入的影響和風險。根據風險評估情況,對重組人源膠原合成表達系統及其工程細胞的質量、工藝控制、穩定性等方面進行深入研究,合理設計變更可比性研究方案。
二、常規生產過程控制
重組人源化膠原蛋白的結構特性容易受到各種理化因素的影響,且分離提純工藝復雜,因此其質量控制體系是針對生產全過程,采用化學、物理和生物學等手段而進行的全程、實時的質量控制。生產過程中每一環節或制備條件的改變均可能影響其非臨床安全性評價的合理性。
(一)載體制備工藝
不同目的基因和表達載體的載體制備工藝可能有差異。以質粒DNA為例,其制備步驟一般包括微生物培養及發酵、菌體收集、菌體裂解、質粒純化、濃縮、灌裝等。工藝研究與確定過程需對關鍵工藝參數進行探索和優化,建立穩定的制備工藝。關鍵工藝參數可能包括發酵培養基組成、發酵培養溫度、補料培養基組成、補料時間和補料量、溶氧量、堿裂解緩沖液及中和緩沖液的組成、堿裂解時間、層析柱載量、層析流速等。研究中建議關注制備全過程對質粒結構和功能的可能影響,如堿裂解步驟可能產生的質粒不可逆變性的情況等。純化工藝開發過程中,可以根據質粒的實際大小和性質選擇合適的柱層析填料,最大程度去除宿主RNA、宿主DNA、DNA碎片和細菌內毒素等雜質。根據研究,設置合理的過程控制指標和可接受標準,如質粒中間產物的濃度、超螺旋比例、雜質殘留量等。
(二)發酵
需對生產過程中使用的各種原材料進行質量控制,以保證這些原材料符合既定用途的要求。需根據生產過程中培養、增殖和蛋白表達量一致性的研究資料,確定轉罐、誘導、終止培養的技術參數。需根據生產工藝驗證資料,明確生產過程中的工藝參數,如培養基滅菌時間滅菌溫度、培養周期等;同時根據表達系統差異,針對性的建立細胞(細菌、酵母或其他)生長的主要質控指標(包括但不限于發酵液OD值、pH值、目標蛋白分子量、蛋白表達量、質粒穩定性等)。
1.有限代次生產
對于哺乳動物細胞等隨著傳代次數增加可能喪失穩定表達的宿主細胞,需予以有限代次生產;對于大腸桿菌、畢赤酵母等表達相對穩定的宿主細胞,必要時進行代次穩定性驗證后,可不限定代次生產。用于培養和誘導基因產物的材料和方法需有詳細的資料。培養過程及收獲時,需有敏感的檢測措施控制微生物污染。
需提供培養生長濃度和產量恒定性方面的數據,并需確立廢棄一批培養物的指標。根據宿主細胞/載體系統的穩定性資料,確定在生產過程中允許的最高細胞倍增數或傳代代次,并需提供最適培養條件的詳細資料。
在生產周期結束時,必要時監測宿主細胞/載體系統的特性,例如質粒拷貝數、宿主細胞中表達載體存留程度、含插入基因的載體的酶切圖譜。一般情況下,用來自一個原始細胞庫的全量培養物進行監測,宜適時做一次目的基因的核苷酸序列分析。
2.連續培養生產
基本要求同“1.有限代次生產”。
必要時監測經長期培養后所表達基因的分子完整性,以及宿主細胞的表型和基因型特征。每批培養的產量變化需在規定范圍內。對可以進行后處理及應廢棄的培養物,需確定指標。從培養開始至收獲,需有敏感的檢查微生物污染的措施。
根據宿主/載體穩定性及表達產物的恒定性資料,需規定連續培養的時間。如屬長時間連續培養,需根據宿主/載體穩定性及產物特性的資料,在不同間隔時間作全面檢定。
(三)純化
根據生產工藝需求,可以將純化過程分為粗純、精純、換液、濃縮等工序,關于純度的要求可視膠原蛋白材料的用途和用法而確定。例如,僅使用一次或需反復多次使用時,用于健康人群或用于重癥患者時,都可對純度有不同程度要求。不同載體細胞表達系統可能對純化過程的要求有所不同,但所采用的分離、純化、濃縮方法或技術,需能適用于規模化生產并保持穩定。
生產中可能引入一些特定的工藝雜質,純化工藝需保證能將其去除或降低至可接受的水平。雜質主要包括與工藝相關的雜質和膠原蛋白材料相關雜質以及環境污染雜質。工藝相關的雜質是指生產過程中產生的雜質,如宿主細胞蛋白、DNA,培養物(誘導劑、抗生素或其他培養基成分等),純化等工藝產生的雜質(酶、化學試劑、無機鹽、溶劑、載體、抗體等);膠原蛋白材料相關雜質是指膠原蛋白材料異質性,如肽鏈的截短或延長形式、修飾形式(去酰胺化、異構體、二硫鍵錯配、糖基化、磷酸化等)、聚合體、多聚體等;環境污染雜質包括細菌內毒素、可能攜帶的病毒和有害微生物等,宿主細胞(如細菌、酵母、昆蟲、植物和哺乳動物細胞)的污染也存在潛在的危險性。具體內容詳見本指導原則“二(一)5.雜質、污染物和添加劑”的內容。
對于生產過程中的收獲、分離和純化方法需詳細記述,需特別注意污染病毒、核酸以及有害抗原性物質的去除,如采用親和層析技術,例如用單克隆抗體,需有檢測可能污染此類外源性物質的方法,不應含有可測出的異種免疫球蛋白。需驗證這些分離、純化關鍵工序及雜質檢測方法。對整個純化工藝需進行全面研究,包括對宿主細胞蛋白、核酸、糖、病毒或其它雜質以及在純化過程中加入的有害的化學物質等的去除。可以采用過濾、離心等操作進行分離,通過洗濾參數、相對離心力等工藝參數進行必要的控制;可以采用蛋白層析或者離子交換層析等技術進行純化。
可使用層析的方法提高膠原蛋白材料的純度,但需充分考慮到層析參數的選擇和層析樹脂的質量對膠原蛋白材料質量的影響,需要重點關注工藝對病毒的滅活與去除能力。病毒滅活/去除驗證需符合《中華人民共和國藥典》通則“生物制品病毒安全性控制”等技術文件的要求。所采用的分離、純化工藝需能確保較好地保留膠原蛋白材料的理化和生物學性質,保留目標肽段的生物學活性。
采用乙醇等沉淀法時,需對乙醇等試劑的質量進行控制,并對膠原濃度、溫度、pH值、離子強度、處理時間等進行研究,明確可接受的限度范圍。采用層析方法時,需根據產物中膠原的性質和濃度,優化色譜條件、確定合理的參數,如層析柱的容量、料液及緩沖液的離子強度和緩沖液的 pH值、流速、接觸時間和溫度等,這些參數的確定需以工藝開發的研究數據為基礎,均需制定限度標準和容許范圍。同時,還需對層析樹脂的清潔、再生(使用壽命)、層析柱的載量、浸出物等進行研究,尤其是使用具有潛在有害配體的層析填料。需關注每一步分離純化步驟的體積、膠原濃度、回收率、電泳純度等,評估對工藝相關雜質和膠原蛋白材料相關雜質的去除能力。必要時,為了證明該工藝對雜質的清除能力,可能需要采用加標試驗評估工藝對某些潛在污染物的清除能力。如涉及中間產物的暫存、運輸等可能影響產品質量的操作時,需有必要的穩定性研究數據支持。
鼓勵采用創新和改進工藝(包括對乙醇分離工藝的改進),提高膠原利用率和質量。在前期工藝開發過程中,需注意關鍵工藝參數的識別,關注不同分離階段工藝控制的完整性、工藝參數設置的合理性。如注冊申請人已有相同分離純化工藝的膠原蛋白材料上市,已有工藝研究數據、控制參數等可供借鑒時,需開展新膠原的3批生產規模工藝驗證。
換液可將蛋白溶劑置換至工藝要求的工作液中,濃縮將蛋白濃縮至工藝要求的濃度。質控點通常包括膜截留效率、蛋白含量、電導率等。
需建立重組人源化膠原蛋白原材料成品的鑒別、純度、穩定性和活性等方面的試驗方法,詳見正文“二、(一)重組人源化膠原蛋白原材料性能研究”。對生產過程中的原液、半成品及生產原輔料,需注意如下方面。
1.原液要求
經純化、換液、濃縮后即為重組人源化膠原原液。如需加入穩定劑或賦形劑,需不影響質量檢定,否則需在添加輔料前取樣進行原液檢定。原液的檢測項目取決于工藝的驗證、一致性確認、預期膠原蛋白材料相關雜質與工藝相關雜質的水平、預期用途等,需采用適當方法對原液質量進行檢測,必要時需與參比品進行比較。原液的儲存需通過穩定性驗證確定儲存條件和時間。參比品的建立和制備需參照《中華人民共和國藥典》“生物制品國家標準物質制備和標定”的相關要求或YY/T 1849《重組膠原蛋白》中的相關要求。
原液的檢測項目可包括蛋白表征研究(如肽段覆蓋率、C端序列、N端序列、氨基酸組成、異質組成、X-射線衍射分析(XRD)、掃描電鏡分析、晶體結構學研究、紅外光譜、圓二色譜、差示掃描量熱分析、等電點、肽圖等指標);理化性能指標檢測(如鑒別、pH、蛋白含量、純度、分子量等指標);污染物殘留指標檢測(如外源性DNA殘留、宿主細胞蛋白殘留、糖類殘留、抗生素殘留、誘導劑殘留、重金屬總量及微量元素殘留等指標);生物性能指標檢測(如微生物限度/無菌、內毒素殘留、熱原等指標)。基于膠原蛋白材料應用風險評估,提供研究性資料或驗證報告。
2.半成品要求
可由一批或多批原液合并生產半成品。擬混合的每批原液應在有效期內,需按規定的工藝生產、單獨檢驗,并符合相應的質量標準;混合的各批原液需可有效追溯;需對混合工藝進行驗證。
如需對半成品進行稀釋或加入其他輔料,如防腐劑或賦型劑甘油、甘露醇及緩沖鹽等,需確定半成品的質量控制要求,包括檢定項目和可接受標準。檢定項目可包括蛋白含量、pH等指標。
3.生產原輔料要求
原輔料需按照國家藥品監督管理局有關規定執行。動物源性原料的使用需提供來源及質控檢測資料;發酵用培養基若添加β內酰胺類抗生素,最終材料成品中不得檢出。
