各有關單位:
根據國家藥品監督管理局2021年度醫療器械注冊技術指導原則制修訂計劃的有關要求,我中心組織起草了《基因測序儀臨床評價注冊審查指導原則(征求意見稿)》。經文獻匯集、企業調研、專題研討和專家討論,形成了征求意見稿。
為使該指導原則更具有科學合理性及實際可操作性,即日起在網上公開征求意見,衷心希望相關領域的專家、學者、管理者及從業人員提出意見或建議,推動指導原則的豐富和完善。
請將意見或建議以電子郵件的形式于2021年10月27日前反饋我中心。
聯系人:鄭生偉、方麗
電話: 010-86452541;010-86452538
電子郵箱:
zhengsw@cmde.org.cn
;
fangli@cmde.org.cn
附件:1.基因測序儀臨床評價注冊審查指導原則(征求意見稿)
2.《基因測序儀臨床評價注冊審查指導原則(征求意見稿)》意見反饋表
國家藥品監督管理局 醫療器械技術審評中心 2021年10月13日
基因測序儀臨床評價 注冊審查 指導原則
( 征求意見 稿)
本指導原則旨在指導注冊申請人對基因測序儀注冊申報資料的準備及撰寫,同時也為技術審評部門審評注冊申報資料提供參考。應在遵循相關法規的前提下使用本指導原則。
本指導原則是對基因測序儀的一般要求,申請人應依據產品的具體特性確定其中內容是否適用 。 若不適用,需具體闡述理由 并提供 相應的科學依據, 同時 依據產品的具體特性對注冊申報資料的內容進行充實和細化。
本指導原則是在現行法規、標準體系 和 當前 科學 認知水平下制定的,隨著法規、標準體系的不斷完善和科學技術的不斷發展,本指導原則相關內容也 將 適時進行調整。
一 、適用范圍
本指導原則適用于 高通量測序的 基因測序儀采用通過同品種醫療器械臨床試驗或臨床使用獲得的數據或通過自身臨床試驗數據進行臨床評價。
目前高通量 基因 測序技術即指第二代測序技術 或下一代測序( Next Generation Sequencing 或 NGS )技術 , 其技術特征是:( 1 )通過測定單元的高度并行化來實現高通量(如每次運行獲得數百 Mb 及 Gb 序列);( 2 )由于化學、物理等原理的限制,序列讀長較短,一般在 150 ~ 200bp (個別原理可以實現 600bp ,比如焦磷酸測序法);( 3 )核心技術成熟。使用的元件(比如 Flow Cell 、硅基陣列、微流控電導結構等)的加工技術(一般在微米尺度以上)技術成熟,器件結構和性能不具有挑戰性。其主流平臺包括:( 1 ) DNA 聚合酶循環測序法(單色或多色熒光底物標記);( 2 ) DNA 連接酶循環測序法(單色或多色熒光底物標記);( 3 )焦磷酸循環測序法(原理一:單色或多色底物熒光;原理二:電學傳感器)。 基于其他技術的 基因測序儀 產品,可參照本指導原則相關適用條款并結合產品特點準備注冊申報資料。
本指導原則適用于申請產品注冊和相關許可事項變更的產品。
申請人應當按照《 醫療器械臨床評價技術指導原則 》的要求提交臨床評價資料,選擇通過同品種醫療器械臨床試驗或臨床使用獲得的數據進行分析評價,或者臨床試驗這兩種評價路徑中適用的任一方式,提交相應的臨床評價資料。
二 、通過同品種醫療器械臨床試驗或臨床使用獲得的數據進行分析評價要求
(一)同品種基因測序儀判定
注冊申請人可按照通則中 “ 同品種醫療器械 ” 的定義和判定,選擇對比產品,并根據產品特征選擇合適的對比項目,基于詳實的研究結果,分析擬申報產品和同品種產品是否存在差異。
申請人所選取的同品種基因測序儀,其與擬申報產品工作原理 相同 、 關鍵模塊相同 ,其 數據質量(包含所測序列中每個堿基的準確度:一般為儀器或分析軟件系統的堿基判定時特有的質量值( quality score ))、一次運行( run )的數據產量(包括平均產量、最大產量、產量在質量 Q 值在不同質量閾值下的平均產量等)、測序在一定質量閾值下的平均讀長(可包括高質量的最長讀長和最短可用讀長等)、儀器指定的不同 測序 模式、不同測序模式產生的數據量和運行時間差異 等關鍵指標 , 不應顯著差異于擬申報產品。
對比項目包括但不限于附件 1 所列舉的項目。對比內容包括定性和定量數據、驗證和確認結果,應詳述二者的相同性和差異性,對差異性是否對產品的安全有效性產生不利影響,應通過擬申報產品自身的數據進行驗證和 / 或確認。對于相同性,也應提交充分的證據。
(二)擬申報產品與對比產品的評價關系
根據《 醫療器械臨床評價技術指導原則 》中規定的評價路徑可知,擬申報產品與對比產品關系有兩種,或為同品種產品,或為非同品種產品,如為同品種產品,還需對兩者之間的差異是否對產品安全性、有效性產生不利影響進行進一步評價。
針對擬申報產品與對比產品的差異,注冊申請人需分析差異性是否對產品的安全性和有效性產生不利影響,將擬申報產品自身的數據作為支持性資料,如申報產品的非臨床研究數據、臨床文獻數據、臨床經驗數據、針對差異性 的 臨床試驗數據等。注冊申請人還需進一步評價差異是否影響性能參數,以及影響的程度和范圍,必要時提供臨床試驗數據進行確認。
針對申報產品的 生化原理(包括但不限于酶學反應、信號發生、信號源強度等)、物理原理(包括但不限于信號采集部件、光源、濾光器件等)、堿基質量判斷 軟件 (包括但不限于堿基判斷 算法、 核心數據集、錯誤率評估、系統弱點評估等)、 系統 集成原理和性能(包括但不限于:系統結構、核心模塊、系統操控軟件、操控人需求、 可靠性 等)等 基本性能等通過功能測試過程與同品種產品進行對比。
與同品種產品相比,申報產品的性能指標、數據質量不低于對比產品時,可認為申報產品 基本 符合同品種產品預期的臨床應用要求;若申報產品的關鍵 模塊 、產品結構、主要功能等與同品種產品具有顯著差異,且該差異影響申報產品的性能指標,尤其是影響數據質量時,注冊申請人還需開展對應差異的臨床試驗,對申報產品性能是否滿足臨床使用需要進行確認。
不同情形評價關系所需提交的支持性資料不盡相同,具體內容見表 1 ,表 1 給出的具體情況舉例可能不能涵蓋所有情況,申請人應根據擬申報產品的具體情況進行列舉和判定,并給出判定的具體理由。
表 1 擬申報產品與對比產品關系及需提交資料類型表
|
擬申報產品與對比產品關系 |
擬申報產品與對比產品差異類型 |
具體情況舉例 |
需提交 資料類型 |
|
屬于同品種(差異評價路徑可參考附件 3 ) |
通常提交 非臨床研究 可能充分證明的差異 |
1. 擬申報產品適用范圍 不超出 對比產品。 2. 擬申報產品芯片密度與對比產品 相當 ,僅數量不一致 ,后期信號數據處理基本一致 。 3. 擬申報產品流動槽支架的性能與對比產品不一致。 4. 擬申報產品流體自動化模塊的性能與對比產品不一致。 5. 擬申報產品緩沖劑吸管裝置的性能與對比產品不一致。 以上差異未造成性能差異和數據質量下降。 |
通常提交 非臨床研究 可能充分證明的差異: 非臨床研究、和 / 或臨床文獻數據、和 / 或臨床經驗數據 |
|
需要提交 臨床試驗資料 的差異 |
1. 擬申報產品適用范圍多于對比產品。 2. 擬申報產品軟件組件的主要功能、核心算法 (信號采集、信號建模、信號糾錯等) 與對比產品不一致。 3. 擬申報產品芯片 設計構架、密度及后期信號數據處理 等關鍵 功能 有較大差異。 |
針對差異的臨床試驗資料 |
|
|
不屬于同品種 |
|
2. 擬申報產品的檢測原理和判讀方法與對比產品不相同。 3. 擬申報產品的使用環境與對比產品不相同。如臺式、便攜式與落地式。 4. 擬申報產品關鍵模塊的原理與對比產品不一致。如成像模塊的原理不一致。 5. 擬申報產品的性能與對比產品差異較大 。 |
重新選擇同品種產品進行比較或補充針對產品的臨床試驗資料 |
(三)證明差異對產品的安全性、有效性未產生不利影響的支持性資料( 臨床經驗數據、臨床文獻數據、 非臨床研究等 )
支持性資料中應明確說明擬申報產品與同品種基因測序儀的差異;詳細說明針對擬申報產品與同品種基因測序儀的差異進行的研究方式及研究結果,提供的研究證據應證明擬申報產品與同品種基因測序儀的差異對產品臨床使用的安全性和有效性帶來的收益 / 影響。
1. 申請人應當完整地列出擬申報產品與 同品種 基因測序儀的所有差異點,并說明這些差異點的相互關系。若不同差異點之間存在相關性或相互影響,則應提供單個差異點影響的研究證據和關聯性差異點共存時影響的研究證據。
2. 申請人應當根據擬申報產品與同品種基因測序儀的具體差異點提供相應的支持性資料,資料的類型和數量應根據擬申報產品和對比產品的差異點對產品安全性、有效性的影響進行確定。
(四)針對差異性的 非臨床研究資料
根據擬申報產品與同品種產品的差異性分析,申請人應當對擬申報產品與對比產品的差異性及各差異點對產品安全性和有效性的影響進行全面評估,針對差異分別列出所進行的非臨床研究的內容和結果,包括但不僅限內部研究資料或驗證報告等。
基于擬申報產品和同品種基因測序儀的對比結果,如果非臨床研究、臨床文獻數據、臨床經驗數據等無法充分地證明該差異對產品安全性和有效性的影響,則申請人應提供相應的臨床試驗資料。
(五)針對適用范圍項目的對比,應提供的臨床數據
針對適用范圍項目的對比,相同點應提交同品種產品的臨床數據以及申報產品的非臨床數據作為支持性資料,對于較同品種產品增加的適用范圍,應提交申報產品的臨床試驗數據,同時可提交其他支持性資料。
支持性資料為臨床文獻數據時,申請人應根據擬申報產品與同品種產品的差異點,合理選擇臨床文獻數據庫,準確設置檢索詞,進行全面的科學文獻檢索,完成文獻檢索和篩選方案、文獻檢索和篩選報告。
支持性資料為臨床經驗數據時,在綜合考慮、科學分析擬申報產品與同品種產品差異的基礎上,可提供臨床經驗數據收集內容,包括對已完成的臨床試驗、不良事件、與臨床風險相關的糾正措施等數據的收集。
臨床文獻和經驗數據的支持性資料應重點分析適用范圍項目的對比。其中可應用于臨床項目應考慮選擇不同變異類型、不同核酸類型的檢測項目。并 充分 分析項目中的數據質量。對于數據質量 進行 比較 和充分 評價。
支持性資料、同品種醫療器械臨床使用獲得的數據的收集、同品種醫療器械臨床數據分析評價方法、臨床評價報告撰寫等方面的具體內容可參照《醫療器械臨床評價技術指導原則》的相關規定。
三、臨床試驗路徑
臨床試驗的開展、方案的制定以及報告的撰寫均應符合相關法規及《 醫療器械臨床評價技術指導原則 》的要求,如相關法規、文件有更新,臨床試驗應符合更新后的要求。下面僅說明該類產品臨床試驗中應關注的重點問題。
(一)臨床試驗機構
應選擇不少于兩家(含兩家)符合要求的臨床試驗機構開展臨床試驗。臨床試驗機構應具備相應的檢測資質和人員。
(二)臨床試驗目的及設計
1. 臨床試驗目的
證明申報產品與已上市同類產品 臨床性能的 一致性。
2. 對比方法的選擇
對于已有同類產品上市的臨床研究,可以選擇臨床參考方法或已在中國境內上市的同類產品作為對照。如選同類產品作為對照,建議選擇目前在臨床檢測方面使用狀況良好的機型,應注意申報產品的適用范圍不應超過同類產品的適用范圍,同時應提供對照產品的信息,如生產企業、型號、適用范圍等。如申報產品的適用范圍超過已批準上市同類產品,則可與同類產品作為對照對相同的適用范圍進行評價,并應另外選擇臨床參考方法作為對比方法,對超出同類產品的適用范圍進行臨床評價。
對于無同類已上市產品的臨床研究,可選擇臨床參考方法作為對比方法進行比較研究,以評價申報產品的臨床性能。
臨床試驗中還應對申報產品和對照產品 / 方法檢測結果不一致樣本進行 分析 ,以明確結果不一致的原因。
臨床參考方法可委托第三方機構檢測,但應在臨床試驗方案中予以明確。
3. 驗證項目的選擇
應根據申報產品所聲稱的適用范圍,選擇代表性的檢測項目進行臨床評價,同時應考慮到不同樣本類型。
如申報產品的適用范圍為對來源于人體樣本的人脫氧核糖核酸( DNA )進行測序,以檢測基因 序列 變化。至少應選擇人類基因靶向測序以及 非靶向 測序項目進行評價。其中人類基因靶向測序, 建議選擇腫瘤組織的基因突變為對象, 應包括代表性的突變類型,如點突變、 小片段的插入 / 缺失、拷貝數變化 。如適用范圍還包括核糖核酸( RNA )的測序, 即將 RNA 逆轉錄成 DNA 后進行測序, 則還應對基因融合(如 ALK 融合)進行驗證。
如申報產品的適用范圍不限于人 DNA ,則應增加病原體檢測項目, 不建議采用宏基因組測序的方式進行臨床試驗。病原體應來自于人體樣本, 包括病毒、細菌、真菌等,每種類別各選一種代表性項目進行評價。如同時包括 RNA ,則還應選擇至少 一 種 RNA 病原體進行評價。
應根據臨床試驗中所選擇的臨床項目,制定受試者的選擇標準,即入選和排除標準。同時受試者年齡、性別分布應均衡合理,充分考慮人種、地域差異對試驗結果的影響。
4. 臨床評價指標
主要評價指標一般為檢測準確性(靈敏度、特異度)或檢測一致性(陽性 / 陰性 符合率 、總 符合率 、 Kappa 值等),主要評價指標應能夠滿足評價產品臨床性能的要求。
次要評價指標一般包括儀器功能、穩定性、使用便捷性、使用安全性等。
同時申請人還應對臨床試驗檢測項目進行數據質量的分析。
5. 樣本量估算
為實現樣本代替總體的目的,臨床試驗需要一定的受試者數量(樣本量)。樣本量一般以臨床試驗的主要評價指標進行估算。需在臨床試驗方案中說明樣本量估算的相關要素及其確定依據、樣本量的具體計算方法 。 主要評價指標的相關參數根據已有臨床數據和小樣本可行性試驗(如有)的結果來估算,需要在臨床試驗方案中明確這些估計值的確定依據。一般情況下, Ⅰ 類錯誤概率 α 設定為雙側 0.05 或單側 0.025 , Ⅱ 類錯誤概率 β 設定為不大于 0.2 ,預期受試者脫落和方案違背的比例不大于 0.2 ,申請人可根據產品特征和試驗設計的具體情形采用不同的取值,需充分論證其合理性。
如臨床試驗采用申報產品與已上市同類產品進行比較研究的試驗設計, 建議 采用單組目標值法樣本量公式估算最低樣本量。
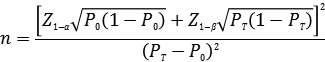
公式中, n 為樣本量; Z 1-α 、 Z 1-β 為顯著性水平和把握度的標準正態分布的分數位, P0 為評價指標的臨床可接受標準, PT 為試驗用體外診斷試劑評價指標預期值。
對于 所選擇 進行 臨床 驗證 的代表性項目大類,如人類基因 靶向測序 ,總樣本量應滿足統計學要求, 其中每種代表性 的突變類型 均應有 一定例數。
臨床試驗中如采用多中心臨床,則所有中心臨床樣本總數應滿足統計學要求,如采用非多中心臨床,則每家臨床機構樣本量應均滿足統計學要求。
6. 統計分析
應選擇合適的統計方法對臨床試驗結果進行統計分析,對于申報產品與 參考方法 / 已上市同類產品的一致性評價,一般選擇 2×2 表的形式總結兩種產品的檢測結果,并據此計算 靈敏度 / 特異度 、陽 性 / 陰性符合率、 Kappa 值等指標及其 95% 置信區間。
對于不一致樣本,應進行原因分析。如臨床試驗方案規定采用其他方法進行確認,則確認結果不應納入統計分析。
(三)質量控制
臨床試驗開始前,建議進行臨床試驗的預試驗,以熟悉并掌握相關試驗方法的操作、儀器、技術性能等,最大限度控制試驗誤差。整個試驗過程都應處于有效的質量控制下,最大限度保證試驗數據的準確性及可重復性。
五、決策是否開展醫療器械臨床試驗
對于具有下列情形之一的產品,通過同品種醫療器械臨床試驗或臨床使用獲得的數據進行分析評價無法充分證明產品安全性、有效性的,應當進行臨床試驗,包括:
1. 擬申報產品或擬申報產品的某關鍵 模塊 (含軟件)具有全新的技術特性 , 或者數據質量 具有顯著 差異 。
2. 擬申報產品 具有新的 臨床預期使用場景 和功能, 且該功能從未在境內獲得批準。
3. 針對 與 同品種醫療器械之間的差異, 若不能通過非臨床研究數據 、 臨床應用數據等證據資料證明申報產品的安全性和有效性 , 申請人需要考慮通過臨床試驗來獲得臨床數據。
具體決策是否開展醫療器械臨床試驗可參照附件 2 和 附件 3 ,并提供充分的依據。
六 、參考文獻
[1] 《醫療器械臨床評價技術指導原則》( 2015 年第 14 號通告)
[2] YY/T 17 23 -202 0 《 高通量基因測序儀 》 [S]
七、起草單位
起草單位:國家藥品監督管理局醫療器械技術審評中心
附件: 1. 擬申報產品與同品種基因測序儀對比表
2. 同品種比對路徑
3.
基因測序儀同品種比對差異評價路徑
附件 1
擬申報產品與同品種基因測序儀對比表
1.基本原理
1.1擬申報產品和同品種產品的工作原理應一致。應詳述核心結構模塊和原理,包括:樣本來源和處理(包括片段化、定向擴增、定向捕獲或純化等)、生化原理(包括催化酶、底物標記、熒光化學、試劑保存、硅基表面處理等)、物理原理(光學或電學模塊并行化、信號采集、信號處理、液路設計、廢液收集處理等)、堿基判斷和質量評估原理(包括信號采集處理、質量評估、序列組裝等核心算法和軟件來源)等。
1.2產品類型應明確臺式、便攜式、大型儀器。
|
序號 |
對比項目 |
同品種產品 |
擬申報產品 |
差異性 |
支持性資料概述 |
備注 |
|
|
基本原理 |
1.1 |
工作原理 |
|
|
|
|
|
|
1.1.1 |
生化原理 |
|
|
|
|
|
|
|
1.1.2 |
物理原理 |
|
|
|
|
|
|
|
1.1.3 |
信號放大和采集原理 |
|
|
|
|
|
|
|
1.1.4 |
信號處理原理(信號建模、轉換、糾錯) |
|
|
|
|
|
|
|
|
1.1.5 |
堿基識別和質量評估原理 |
|
|
|
|
|
|
|
1.1.6 |
高通量、并行化原理 |
|
|
|
|
|
|
|
1.1.7 |
液路系統 |
|
|
|
|
|
|
|
1.1.8 |
信號放大和采集原理 |
|
|
|
|
|
|
|
|
... |
|
|
|
|
|
|
|
1.2 |
產品類型 |
|
|
|
|
|
2. 結構組成
2.1產品組成應包括描述申報產品的所有結構組成。對成像模塊、流動槽支架、流體自動化模塊、緩沖劑吸管裝置等功能模塊、主體模塊等核心結構模塊進行逐項詳細比對。
2.2核心部件應至少對加樣裝置、恒溫反應裝置、芯片、信號采集、檢測器及其原件技術要求進行對比。
|
序號 |
對比項目 |
同品種產品 |
擬申報產品 |
差異性 |
支持性資料概述 |
備注 |
|
|
結構組成 |
2.1 |
產品組成 |
|
|
|
|
|
|
|
|
... |
|
|
|
|
|
|
2.2 |
核心部件 |
|
|
|
|
|
|
|
2.2.1 |
流體液路系統 |
|
|
|
|
|
|
|
2.2.2 |
恒溫反應裝置 |
|
|
|
|
|
|
|
|
2.2.3 |
芯片設計構架 |
|
|
|
|
|
|
|
2.2.4 |
恒溫反應裝置 |
|
|
|
|
|
|
|
2.2.5 |
信號采集處理裝置 |
|
|
|
|
|
|
|
|
... |
|
|
|
|
|
3.性能要求
3.1性能參數應包括 最大數據量/run*run,reads長度,突變類型以及人與病原體的檢測性能,并對數據質量進行充分評價。
3.2反應模式及時間應包括所有的反應模式如PE150,PE250,SE35等。
|
序號 |
對比項目 |
同品種產品 |
擬申報產品 |
差異性 |
支持性資料概述 |
備注 |
|
|
性能要求 |
3.1 |
性能參數 |
|
|
|
|
|
|
3.2 |
功能參數 |
|
|
|
|
|
|
|
|
|
反應模式及用時 |
|
|
|
|
|
|
|
|
... |
|
|
|
|
|
4.軟件核心功能及算法
4.1對比產品的軟件核心功能及算法
|
序號 |
對比項目 |
同品種產品 |
擬申報產品 |
差異性 |
支持性資料概述 |
備注 |
|
|
軟件核心功能 |
4.1 |
運行控制 |
|
|
|
|
|
|
4.2 |
狀態監控 |
|
|
|
|
|
|
|
|
4.3 |
堿基識別 |
|
|
|
|
|
|
|
4.4 |
數據質控 |
|
|
|
|
|
|
|
4.5 |
結果判讀 |
|
|
|
|
|
|
|
|
... |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5.適用范圍及 預期用途
5.1樣本類型通常包括血清、全血、組織、FFPE及其他含有人類以及各種病原體的核酸的樣本類型等,可采用代表性樣本類型(根據樣本中基因組特征)。
5.2變異類型通常包括點突變、插入缺少、結構變異等變異類型。
5.3檢測的核酸樣本類型通常包括人類基因組DNA、細胞內RNA、細胞外循環DNA或RNA,病原體DNA或RNA等。所有各類不同來源的RNA均須逆轉錄成互補DNA后才能用于測序。
|
序號 |
對比項目 |
同品種產品 |
擬申報產品 |
差異性 |
支持性資料概述 |
備注 |
|
|
適用范圍 預期用途 |
5.1 |
預期用途 |
|
|
|
|
|
|
5.2 |
代表性樣本類型 |
|
|
|
|
|
|
|
5.3 |
可完成試驗項目 |
|
|
|
|
|
|
|
5.4 |
變異類型 |
|
|
|
|
|
|
|
5.5 |
檢測的核酸類型 |
|
|
|
|
|
|
|
5.6 |
使用環境 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
6.配套要求
|
序號 |
對比項目 |
同品種產品 |
擬申報產品 |
差異性 |
支持性資料概述 |
備注 |
|
|
配套要求 |
6.1 |
上機文庫質量要求 |
|
|
|
|
|
|
6.2 |
樣本來源和處理(包括片段化、定向擴增、定向捕獲或純化等) |
|
|
|
|
|
|
|
|
6.3 |
配套使用的測序通用試劑要求 |
|
|
|
|
|
|
|
|
... |
|
|
|
|
|
7.安全性評價
|
安全性 評價 |
7.1 |
通用電氣安全 |
|
|
|
|
|
|
7.2 |
專用安全 |
|
|
|
|
|
|
|
|
7.3 |
網絡安全 |
|
|
|
|
|
8.其他
|
序號 |
對比項目 |
同品種產品 |
擬申報產品 |
差異性 |
支持性資料概述 |
備注 |
|
8 |
標簽 |
|
|
|
|
|
|
9 |
產品說明書 |
|
|
|
|
|
|
10 |
禁忌癥 |
|
|
|
|
|
|
11 |
防范措施和警告 |
|
|
|
|
|
|
12 |
產品符合的國家 /行業標準 |
|
|
|
|
|
|
|
... |
|
|
|
|
|
以上所列出的內容為擬申報產品與同品種基因測序儀對比需要具體考慮的事項,申請人可根據產品特點增加對比項目。
附件 2
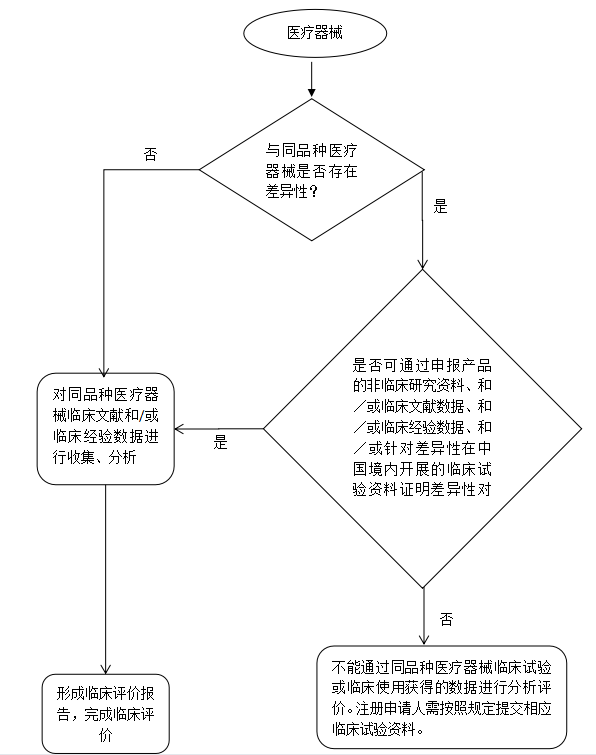
通過同品種醫療器械臨床試驗或臨床使用獲得的數據進行分析評價路徑
|
|
|
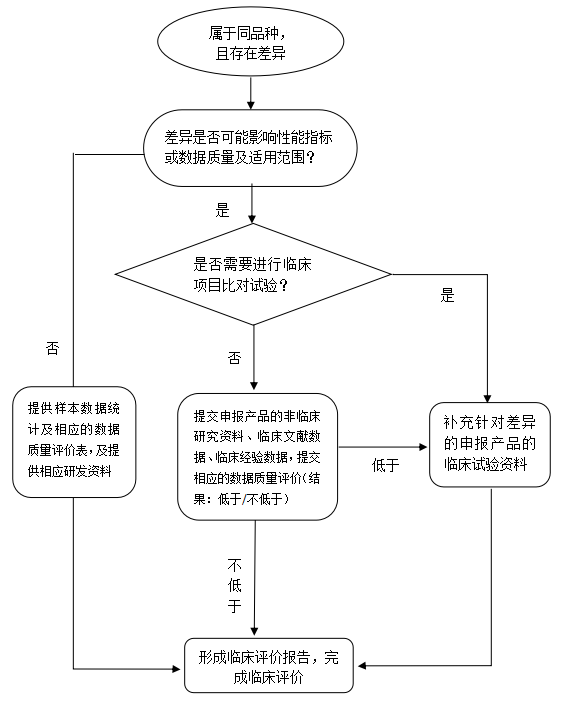
附件 3
同品種比對差異評價路徑
附件2
意見反饋表
部門 :
聯系人:
聯系方式:
|
編號 |
頁碼 / 行號 |
章節 |
需要修改的內容 |
建議修改后的內容 |
修改理由 |
|
1 |
|
|
|
|
|
|
2 |
|
|
|
|
|
|
3 |
|
|
|
|
|
|
4 |
|
|
|
|
|
請明確至三級標題,即阿拉伯數字編號。