近年來,國家藥品監督管理局不斷在“規范臨床試驗,提高注冊管理水平,完善臨床試驗機構管理方式,并且讓臨床試驗監督抽查常態化”工作上,投入大量的人力、物力,在此過程中大批企業撤回注冊申請,同時感慨臨床試驗規范化程度已不可同日而語。如今的臨床試驗環境,使得監管方、申辦方、CRO及臨床試驗機構進入一種微妙的狀態,促使第三方稽查作為獨立于利益相關方之外的角色日益受到申辦方重視。瑞旭小編今天對醫療器械臨床試驗稽查進行拆分和解析,與君共勉。
醫療器械臨床稽查標準及依據
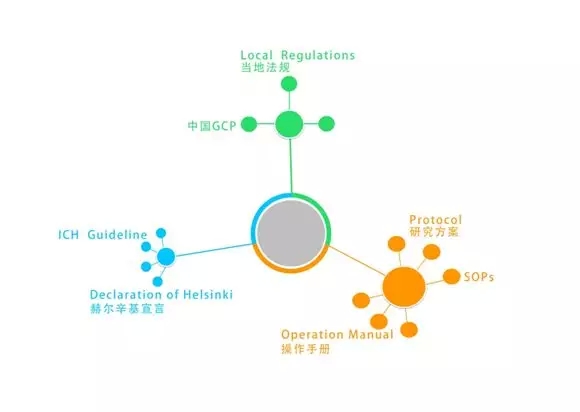
臨床試驗特別是多中心臨床試驗,是一個復雜的過程,稽查是臨床試驗結果可靠的保證,保證臨床試驗的質量是通過臨床試驗的稽查來進行的,因此嚴格遵守稽查標準和依據更是重中之重!
醫療器械臨床稽查類型
樹有分叉,葉有分型。醫療器械臨床試驗稽查,需求不同可分為,試驗機構稽查、研究稽查、監管部門稽查等。
這里簡單介紹一下獨立的第三方稽查要點:
Ⅰ、針對臨床試驗的操作部門(包含以下五點)
①研究中心
②試驗器械管理部門
③申辦者的試驗操作部門
④申辦者內部或外部的試驗支持部門
⑤研究程序
Ⅱ、針對實驗室
Ⅲ、針對研究第三方部門(存放文件的倉庫等)
Ⅳ、針對合同研究組織
Ⅴ、任何針對試驗真實完整性的質疑
醫療器械臨床試驗稽查是一個系統性檢查工作,更多的是將各個環節稽查串聯在一起才能完整的評價試驗是否保證受試者的權益,是否符合相關SOP、GCP和法規。
醫療器械臨床稽查內容
醫療器械臨床試驗稽查反應了各個試驗參與方履行質量標準和標準操作規程的真實情況,其在內容上主要包含了以下幾部分:
Ⅰ、申辦者按GCP所保存文件(TMF)
Ⅱ、臨床試驗中心資料、研究者文件夾
Ⅲ、試驗方案依從性、原始記錄及病例記錄表填寫
Ⅳ、知情同意書(ICF)
Ⅴ、臨床試驗現場
Ⅵ、臨床試驗質量保證與監查工作
Ⅶ、試驗相關設備校正、質控
Ⅷ、統計與數據處理等
Ⅸ、其他
醫療器械臨床稽查程序
醫療器械臨床試驗本身就是一項復雜的工作,既包含隨研究進展的橫向推移,又有縱向各臨床試驗環節的嚴謹配合,稽查需要在短時間內完成大量工作,需要科學合理的稽查周期和程序。稽查周期主要有以下幾步:
第一步:制定稽查計劃明確方案中關鍵因素、制定稽查方案等;
第二步:稽查啟動會議向被稽查對象介紹稽查目的、內容和程序,請PI介紹試驗相關情況;
第三步:查閱試驗資料和文件重點查看試驗方案、研究計劃、SOP等修改的批準情況,原始記錄、CRF、儀器設備校準和驗證等文件;
第四步:現場查看第五步:詢問有關人員
第六步:結束會議和答辯第七步:稽查報告和跟蹤Tip:為保證稽查工作的獨立性及其價值,管理當局不應常規要求稽查報告。當存在嚴重違反GCP的證據時,或在訴訟過程中,管理當局可以根據具體情況要求稽査報告。
