近日,山東問題疫苗事件炒得沸沸揚揚,“疫苗事件”牽動著千萬父母的心,同時也牽涉到疫苗從生產、經營、使用及監管等整個產業鏈的規范性問題,瑞旭技術專家透過“疫苗事件”的始末,解析醫療器械行業的監管趨勢。
疫苗事件始末- 2016年3月18日,媒體爆出2010年以來,山東省濟南龐某衛母女涉嫌非法經營疫苗,非法購入25種兒童、成人用二類疫苗,未經嚴格冷鏈存儲運輸銷往全國18個省市,涉案金額達5.7億元。
- 2016年3月19日,山東省食藥監局發布“關于龐某等非法經營疫苗案有關線索的公告”,根據濟南市食品藥品監督管理局在協助公安機關偵破龐某等非法經營疫苗案件中掌握的信息,共梳理出向龐某等提供疫苗及生物制品的上線線索107條,從龐某等處購進疫苗及生物制品的下線線索193條,涉及全國24省市。原文
- 2016年3月20日,山東發文確認龐某非法經營疫苗案查封疫苗品種的清單,疫苗12種、免疫球蛋白2種、治療性生物制品1種:原文
12種疫苗無第一類疫苗,全部為第二類疫苗:
- 凍干人用狂犬病疫苗(Vero細胞)
- 脊髓灰質炎滅火疫苗
- B型流感嗜血桿菌結合疫苗
- 乙型流腦減毒活疫苗
- 腮腺炎減毒活疫苗
- 凍干乙型腦炎滅活疫苗(vero細胞)
- 重組乙型肝炎疫苗(CHO細胞、漢遜酵母)
- A群C群腦膜炎球菌結合疫苗
- ACYW135群腦膜炎球菌多糖疫苗
- 水痘減活疫苗
- 口服輪狀病毒活疫苗
- 甲型肝炎滅活疫苗(人二倍體細胞)
- 狂犬病人免疫球蛋白
- 乙型肝炎人免疫球蛋白
細菌溶解物
- 2016年3月22日,世界衛生組織(WHO)回應中國疫苗事件。
- 2016年3月22日,國務院總理李克強對非法經營疫苗系列案件作出重要批示,徹查“問題疫苗”的流向和使用情況,及時回應社會關切,依法嚴厲打擊違法犯罪行為,對相關失職瀆職行為嚴肅問責,絕不姑息。同時,抓緊完善監管制度,落實疫苗生產、流通、接種等各環節監管責任,堵塞漏洞,保障人民群眾生命健康。原文
近年來,隨著新的醫療器械監管條例的實施及配套管理辦法的修訂實施,醫療器械的監管從傳統的重審批輕監管逐步向輕審批重監管轉變,醫療器械供應及使用者將成為醫療器械質量責任方,基于產品生命周期風險管理已經逐漸成為醫療器械產業健康發展的新動力。
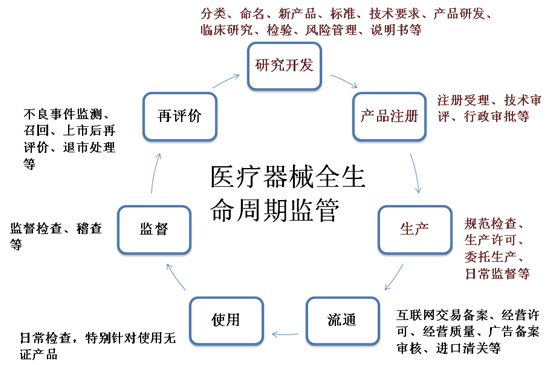
醫療器械相關機構應確保在生產、經營或使用過程中符合最新《醫療器械監督管理條例》及質量管理規范要求,確保醫療器械產品質量安全,促進醫療器械產業健康發展,合規創造社會價值。
