2021年6月,新版《醫療器械監督管理條例》(國務院第739號令)施行,明確規定“進行醫療器械臨床評價,可以根據產品設計特征、臨床風險、已有臨床數據等情形,通過開展臨床試驗,或者通過對同品種醫療器械臨床文獻資料、臨床數據進行分析評價,證明醫療器械安全、有效”。
2021年9月,國家藥監局發布醫療器械臨床評價配套規范性文件,其中《決策是否開展醫療器械臨床試驗技術指導原則》(2021年第73號,以下簡稱“《決策導則》”,見附件1)從“高風險醫療器械”、“新型醫療器械”、“已有證據的充分性”三個方面指導申請人決策申報產品是否需要開展臨床試驗。
為進一步指導申請人確定具體產品的臨床評價路徑,器審中心根據目前已有產品的審評經驗,基于《醫療器械分類目錄》中的子目錄12有源植入器械和13無源植入器械的產品描述、預期用途和品名舉例,編寫了《基于<醫療器械分類目錄>子目錄“12有源植入器械”臨床評價推薦路徑》(見附件2)和《基于<醫療器械分類目錄>子目錄“13無源植入器械”臨床評價推薦路徑》(見附件3),給出具體產品臨床評價路徑選擇的推薦意見。對于產品數量較少,近幾年無相關產品申報的,暫未在該文件中體現。
文件中標注“臨床試驗”的產品,基于目前認知,通常為《決策導則》中的“高風險醫療器械”,除該指導原則第三部分第(一)款中可考慮免于開展臨床試驗的情形,原則上需要開展臨床試驗。
文件中標注“同品種”的產品,如申報產品與同品種醫療器械相比,適用范圍、技術特征和/或生物學特性等方面具有顯著差異,屬于《決策導則》中提出的“新型醫療器械”,除《決策導則》第三部分第(二)款中可考慮免于開展臨床試驗的情形,需提交申報產品的臨床試驗資料。
文件中標注“同品種”的產品,如不屬于《決策導則》中提出的“新型醫療器械”,申請人可按照《醫療器械臨床評價技術指導原則》《醫療器械臨床評價等同性論證技術指導原則》《醫療器械注冊申報臨床評價報告技術指導原則》(2021年第73號)的相關要求,根據申報產品特征、臨床風險、已有臨床數據等情形,選取合適的同品種醫療器械,通過對同品種醫療器械臨床數據進行分析評價,證明醫療器械的安全性、有效性。此種情形下,如通過非臨床研究未能證明差異性部分的安全有效性,即《決策導則》中提出的“已有證據不能證明產品符合醫療器械安全和性能基本原則”,需提交申報產品的臨床試驗資料。
為便于注冊申請人查詢,在推薦路徑表單中標注了《免于臨床評價醫療器械目錄的通告》(2021年第71號)相關內容。是否可免于進行臨床評價,需按照《免于臨床評價醫療器械目錄》進行判定。
我中心將根據醫療器械風險變化,參考國際經驗,遵循最新科學認知,立足監管實際,對相關產品的臨床評價推薦路徑進行動態調整。
目前,除首批公布的《醫療器械分類目錄》子目錄“12有源植入器械”和“13無源植入器械”相關產品臨床評價推薦路徑,對于《醫療器械分類目錄》中其他子目錄產品的臨床評價推薦路徑,我中心正在組織編寫,擬逐步公布。<醫療器械分類目錄><醫療器械分類目錄>
附件1
決策是否開展醫療器械臨床試驗技術指導原則
決策是否開展醫療器械臨床試驗是綜合考慮產品的適用范圍、技術特征、生物學特性、風險程度及已有研究數據(包括臨床數據和非臨床數據)等方面來確定開展臨床試驗必要性的過程。需要開展臨床試驗的,可根據具體情況,選擇在境內開展臨床試驗、全部或同期在境外開展臨床試驗。
本指導原則旨在為注冊申請人和審查人員判斷擬申請注冊的產品是否需要開展臨床試驗提供技術指導,不涉及注冊審批等行政事項,亦不作為法規強制執行,如有能夠滿足法規要求的其他方法,也可以采用,但應提供詳細的研究資料和驗證資料。應在遵循相關法規的前提下使用本指導原則。
一、 適用范圍
本指導原則適用于需要開展臨床評價的第二類、第三類醫療器械產品注冊時,是否需要開展臨床試驗的判定,不適用于按醫療器械管理的體外診斷試劑。
二、總則
在醫療器械設計開發過程中,設計確認是其重要環節,以確保產品能夠滿足規定的使用要求或者預期用途的要求。可采取多種方法實現設計確認,如模體試驗、計算機模擬試驗、動物試驗、臨床評價等。可用于臨床評價的臨床數據包括在境內或境外,合法的臨床使用過程中生成的安全性、有效性信息,例如臨床試驗數據、臨床文獻數據和臨床經驗數據等。鼓勵注冊申請人采用最有效的方式獲取證明符合醫療器械安全和性能基本原則所需的最少量信息,消除或減輕不必要的負擔,可使患者能夠及早并持續獲得安全有效的醫療器械。臨床試驗的必要性應全面考慮醫療器械的適用范圍、技術特征、生物學特性、風險程度、與現有醫療器械或現有診療方法的差異等方面,如果非臨床研究的結果和/或現有臨床數據不足以證明產品對醫療器械安全和性能的基本原則的符合性,則可能需要開展臨床試驗。基于良好設計和規范實施的臨床試驗能夠提供科學、可靠的醫療器械安全有效性數據。
本指導原則提到的符合醫療器械安全和性能基本原則,是指對臨床證據與其他設計驗證和確認文件、器械描述、說明書和標簽、風險管理文件以及生產信息進行綜合評價后得出的結論。
三、考慮因素
(一) 臨床使用具有高風險的第三類醫療器械(以下簡稱“高風險醫療器械”),原則上需要開展臨床試驗,但以下情形可考慮免于開展臨床試驗:
1.申報產品的前代產品未在中國獲準上市,申報產品是對前代產品進行的設計變更,注冊申請人可通過已有數據(如非臨床研究數據、前代產品的臨床試驗數據、申報產品境外臨床數據)證明申報產品符合醫療器械安全和性能基本原則。
2.注冊申請人可按照《接受醫療器械境外臨床試驗數據技術指導原則》的要求提供申報產品境外臨床試驗數據,結合其他設計驗證和確認文件、器械描述、說明書和標簽、風險管理文件以及生產信息進行綜合評價,證明申報產品符合醫療器械安全和性能的基本原則。
3.申報產品的前代產品已在中國獲準上市,申報產品是對前代產品進行的設計變更,且注冊申請人可通過已有數據(如非臨床研究數據、前代產品的臨床數據、申報產品境外臨床數據)證明申報產品符合醫療器械安全和性能基本原則。
前代產品是指與申報產品屬于同一注冊申請人、具有相同適用范圍且技術特征和生物學特性相似的產品,申報產品與前代產品為迭代關系。
(二)申報產品雖然不屬于高風險醫療器械,但為新型醫療器械,原則上應開展臨床試驗,但以下情形可考慮免于開展臨床試驗:
1.注冊申請人可通過非臨床研究數據充分證明申報產品符合醫療器械安全和性能基本原則。
2.申報產品在我國為新型醫療器械,但其自身已有臨床數據(例如境外臨床文獻數據、境外臨床試驗數據等),注冊申請人可通過非臨床研究數據、申報產品的臨床數據證明申報產品符合醫療器械安全和性能基本原則。
3.申報產品在我國為新型醫療器械,但其前代產品已有境外臨床數據,申報產品是對前代產品進行的設計變更,注冊申請人可通過非臨床研究數據、申報產品的境外臨床數據和前代產品的境外臨床數據充分證明申報產品符合醫療器械安全和性能基本原則。
新型醫療器械是指與已在中國境內獲準上市的醫療器械相比,在適用范圍、技術特征和/或生物學特性等方面具有顯著差異的醫療器械。大部分醫療器械是一個漸進的變更過程,并不屬于新型醫療器械,很多情形下,可以通過非臨床研究來證明其符合醫療器械安全和性能的基本原則。
(三)產品不屬于高風險醫療器械,也不屬于新型醫療器械,在注冊申請人已開展充分的非臨床研究且全面收集已有臨床數據的基礎上,若已有證據不能證明產品符合醫療器械安全和性能的基本原則時,有可能需要通過開展臨床試驗補充臨床數據。獲得的臨床試驗數據用于產品臨床評價過程且為臨床證據的一部分。
例如,對于特定申報產品,其已有同品種產品在中國獲準注冊,申報產品與同品種產品存在差異。若注冊申請人基于申報產品的非臨床研究數據以及同品種產品的臨床數據對產品實施了全面的臨床評價,但仍不能證明申報產品符合醫療器械安全和性能的基本原則,則可能需要開展臨床試驗。
當注冊申請人根據以上因素考慮是否開展醫療器械臨床試驗時,可參考《醫療器械臨床試驗決策流程圖》(見附件)。
附件:醫療器械臨床試驗決策流程圖
附件
醫療器械臨床試驗決策流程圖
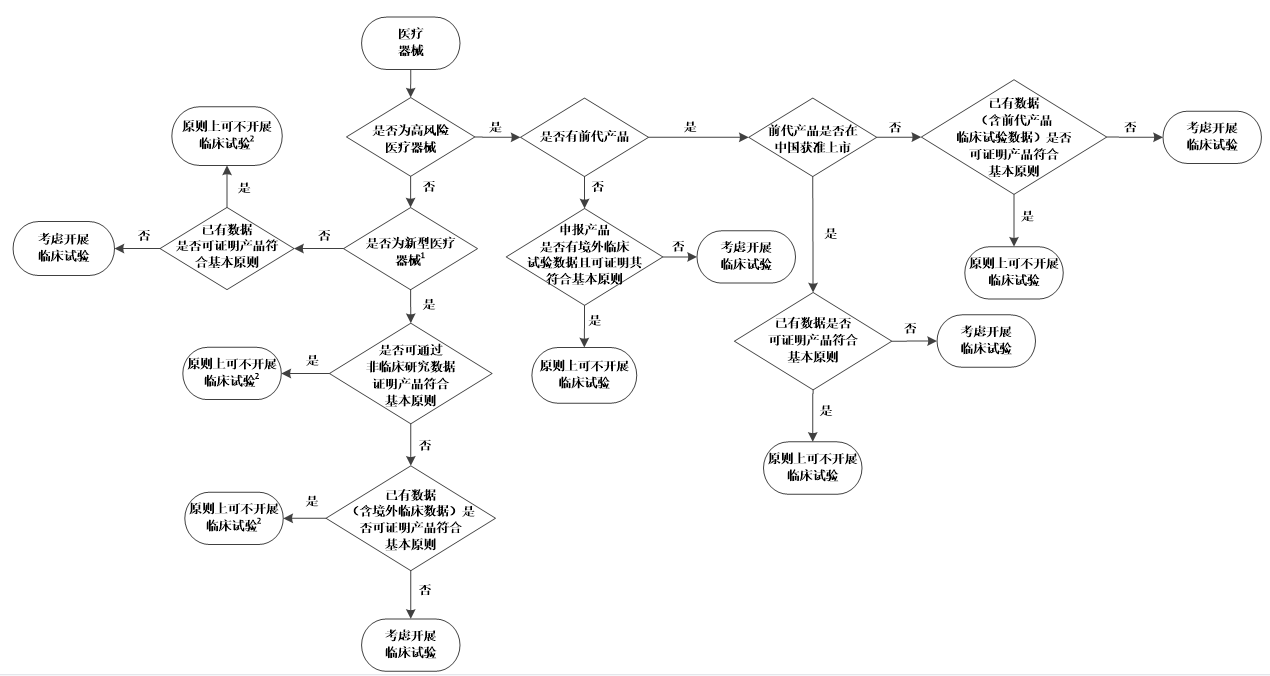
1.新型醫療器械描述見本指導原則三(二)。
2.原則上可不開展臨床試驗的,注冊申請人需結合非臨床研究、等同性論證(如需要)、臨床評價(如需要)證明產品符合醫療器械安全和性能基本原則。
| 附件2 | |||||||||
| 基于《醫療器械分類目錄》子目錄“12有源植入器械”臨床評價推薦路徑 | |||||||||
| 序號 | 一級產品類別 | 二級產品類別 | 產品描述 | 預期用途 | 品名舉例 | 管理類別 | 免臨床評價 | 臨床評價 | |
| 同品種 | 臨床試驗 | ||||||||
| 01 | 心臟節律管理設備 | 01植入式心臟起搏器 | 通常由植入式脈沖發生器和扭矩扳手組成。通過起搏電極將電脈沖施加在患者心臟的特定部位。 | 用于治療慢性心率失常。再同步治療起搏器還可用于心力衰竭治療。 | 植入式心臟起搏器、植入式心臟再同步治療起搏器 | III | 臨床試驗 | ||
| 02植入式心律轉復除顫器 | 通常由植入式脈沖發生器和扭矩扳手組成。通過檢測室性心動過速和顫動,并經由電極向心臟施加心律轉復/除顫脈沖對其進行糾正。 | 用來治療快速室性心律失常。再同步治療除顫器還可用于心力衰竭治療。 | 植入式心律轉復除顫器、植入式再同步治療心律轉復除顫器、植入式皮下心律轉復除顫器 | III | 臨床試驗 | ||||
| 03 臨時起搏器 | 通常由非植入式脈沖發生器和患者電纜(若使用)組成。 | 用于心房和心室的體外臨時起搏。 | 臨時起搏器、體外起搏器 | III | 同品種 | ||||
| 04植入式心臟起搏電極導線 | 通常由電極導線和附件組成。 | 與植入式心臟起搏器配合使用,用于治療慢性心律失常。 | 植入式心臟起搏電極導線、植入式左室心臟起搏電極導線、植入式心外膜心臟起搏電極導線 | III | 通常與配用的植入式心臟起搏器一起開展臨床試驗 | ||||
| 05植入式心臟除顫電極導線 | 通常由電極導線和附件組成。 | 與植入式心律轉復除顫器配合使用,用于治療快速室性心律失常。 | 植入式心臟除顫電極導線、植入式皮下心臟除顫電極導線 | III | 通常與配用的植入式心律轉復除顫器一起開展臨床試驗 | ||||
| 06臨時起搏電極導線 | 通常由電極導線和附件組成。 | 用于心房和心室的臨時起搏。 | 臨時心臟起搏電極導線 | III | 同品種 | ||||
| 07植入式心臟事件監測設備 | 通常由監測儀植入體本身和體外附件(若使用)組成。 | 植入于人體內記錄皮下心電圖和心律失常事件。 | 植入式心臟事件監測器、植入式心電事件監測器 | III | 臨床試驗 | ||||
| 08植入式封堵工具 | 通常由硅橡膠材料制成。 | 用于電極導線終端未使用連接器或植入式脈沖發生器未使用端口的絕緣。 | 封堵塞、電極導線帽 | III | 同品種 | ||||
| 10 起搏系統分析設備 | 通常由分析儀主機和患者電纜、電纜適配器、無菌延長線組成。 | 適合在起搏器和除顫器植入過程中用于對起搏電極系統進行分析。 | 起搏系統分析儀 | II | 同品種 | ||||
| 11 心臟節律管理程控設備 | 通常由顯示單元、打印單元、程控單元、軟件等組成。 | 用于詢問、程控、顯示數據或測試植入式心臟起搏器和植入式心律轉復除顫器等心臟節律管理設備。 | 心臟節律管理設備程控儀、心臟節律管理設備患者程控儀、程控儀 | II | 通常與配用的心臟節律管理設備一起開展臨床試驗 | ||||
| 12連接器套筒 | 通常由接觸夾及連接器環形電極組成。 | 用于連接到電極導線連接器、或者斷開連接。 | 四極連接器套筒 | II | 同品種 | ||||
| 02 | 神經調控設備 | 01植入式神經刺激器 | 通常由植入式脈沖發生器和附件組成。 | 通過將電脈沖施加在腦部或神經系統的特定部位來治療帕金森病、控制癲癇、軀干和/或四肢的慢性頑固性疼痛或腸道控制以及排尿控制、肌張力障礙等疾病。 | 植入式腦深部神經刺激器、植入式脊髓神經刺激器、植入式骶神經刺激器、植入式迷走神經刺激器、植入式可充電腦深部神經刺激器、植入式可充電脊髓神經刺激器、植入式可充電骶神經刺激器、植入式可充電迷走神經刺激器 | III | 臨床試驗 | ||
| 02植入式神經刺激電極 | 通常由電極導線和附件組成。 | 與植入式神經刺激器配合使用,用于治療帕金森病、控制癲癇、軀干和/或四肢的慢性頑固性疼痛或腸道控制以及排尿控制、肌張力障礙等疾病。 | 植入式腦深部神經刺激電極、植入式脊髓神經刺激電極、植入式骶神經刺激電極、植入式迷走神經刺激電極、植入式腦深部神經刺激延伸導線、植入式脊髓神經刺激延伸導線、植入式骶神經刺激延伸導線、植入式迷走神經刺激延伸導線 | III | 通常與配用的植入式神經刺激器一起開展臨床試驗 | ||||
| 03測試刺激電極 | 通常由電極和附件(若使用)組成。 | 與測試刺激器配合使用,用于臨時刺激與測試。 | 測試神經刺激電極、測試刺激電極、神經刺激測試電極 | III | 通常與配用的測試刺激器、植入式神經刺激器一起開展臨床試驗 | ||||
| 04神經調控充電設備 | 通常由充電器、充電線圈、適配器等組成。 | 用于對特定的可充電植入式脈沖發生器的電池進行充電,以延長可充電植入式脈沖發生器的使用期限。 | 神經調控體外充電器、體外充電器 | III | 同品種 | ||||
| 05植入式電極導線適配工具 | 通常由適配器、神經刺激器接口插頭、轉矩扳手組成。 | 用于連接植入式神經刺激器與適配的植入式延伸導線。 | 植入式電極導線適配器 | III | 同品種 | ||||
| 07測試刺激器 | 通常由控制單元、輸出單元、電源單元組成。 | 用于在電極導線放置或試驗刺激效果期間評估神經刺激系統的功效。 | 測試神經刺激器、測試刺激器、體外神經刺激器 | II | 通常與植入式神經刺激器一起開展臨床試驗 | ||||
| 08測試延伸導線 | 通常由延伸導線和附件(若使用)組成。 | 與測試刺激器、配合使用,用于臨時刺激和測試。 | 測試神經刺激延伸導線、神經刺激系統經皮延伸導線和電纜、多電極測試電纜 | II | 通常與配用的測試刺激器、植入式神經刺激器一起開展臨床試驗 | ||||
| 09神經調控程控設備 | 通常由程控單元、顯示單元、軟件等組成。 | 用于對植入式神經調控設備的詢問、程控、顯示數據和測試。 | 神經調控設備程控儀、神經調控設備患者程控儀、程控儀、患者程控儀 | II | 通常與配用的植入式神經刺激器一起開展臨床試驗 | ||||
| 03 | 輔助位聽覺設備 | 01植入式位聽覺設備 | 通常由接收部分、刺激器主體和電極(若有)組成的植入體。 | 通過對耳蝸內或蝸后聽覺傳導通路特定部位進行電刺激,或對中耳以及骨傳導進行振動來提高或恢復聽覺感知。 | 人工耳蝸植入體 | III | 臨床試驗 | ||
| 02體外聲音處理器 | 通常由言語處理器主機、控制器等組成的體外部分。 | 與植入式輔助聽覺設備體配合使用,將聲音轉化為電刺激或振動,通過對耳蝸內或蝸后聽覺傳導通路特定部位進行電刺激,或對中耳以及骨傳導進行振動來提高或恢復聽覺感知。 | 人工耳蝸聲音處理器 | II | 通常與配用的人工耳蝸一起開展臨床試驗 | ||||
| 03輔助位聽覺調控設備 | 通常由主機,連接電纜等組成。 | 用于調試或測試輔助位聽覺設備。 | 人工耳蝸調機設備、人工耳蝸檢測設備 | II | 通常與配用的人工耳蝸一起開展臨床試驗 | ||||
| 04 | 其他 | 01植入式心臟收縮力調節設備 | 通常由植入式脈沖發生器和扭矩扳手組成,通過電極將電脈沖施加在患者心臟的特定部位。 | 用于心肌收縮力的調節增強。 | 植入式心臟收縮力調節器 | III | 臨床試驗 | ||
| 通常由充電器、充電線圈、適配器等組成。 | 用于對特定的植入式心臟收縮力調節設備電池進行充電,以延長其使用期限。 | 心臟收縮力調節設備充電器 | III | 通常與配用的植入式心臟收縮力調節設備一起開展臨床試驗 | |||||
| 通常由顯示單元、程控單元、軟件等組成。 | 用于詢問、程控、顯示數據或測試植入式心臟收縮力調節設備。 | 心臟收縮力調節設備程控儀 | II | 通常與配用的植入式心臟收縮力調節設備一起開展臨床試驗 | |||||
| 02植入式循環輔助設備 | 通常由植入式泵體、電源部分、血管連接和控制器組成。 | 用于心室循環功能的輔助,代替心臟實現泵血。 | 植入式左心室輔助裝置、植入式右心室輔助裝置 | III | 臨床試驗 | ||||
| 03植入式藥物輸注設備 | 通常由輸注泵植入體、鞘內導管、附件等組成。 | 用于長期輸入藥物或液體。 | 植入式藥物泵 | III | 臨床試驗 | ||||
| 附件3 | |||||||||
| 基于《醫療器械分類目錄》子目錄“13無源植入器械”臨床評價推薦路徑 | |||||||||
| 序號 | 一級產品類別 | 二級產品類別 | 產品描述 | 預期用途 | 品名舉例 | 管理類別 | 免臨床評價 | 臨床評價 | |
| 同品種 | 臨床試驗 | ||||||||
| 01 | 骨接合植入物 | 01單/多部件金屬骨固定器械及附件 | 通常由一個或多個金屬部件(如板、釘板、刃板)及金屬緊固裝置(如螺釘、釘、螺栓、螺母、墊圈)組成。一般采用純鈦及鈦合金、不銹鋼、鈷鉻鉬等材料制成。其中金屬部件通過緊固裝置固定就位。 | 用于固定骨折之處,也可用于關節的融合及涉及截骨的外科手術等。可植入人體,也可穿過皮膚對骨骼系統施加拉力(牽引力)。 | 金屬鎖定接骨板、金屬非鎖定接骨板、金屬鎖定接骨螺釘、金屬非鎖定接骨螺釘、金屬股骨頸固定釘、金屬接骨板釘系統、金屬U型釘 | Ⅲ | 13-01-01 金屬鎖定接骨板 由符合GB 4234、GB/T 13810、ISO 5832-1、ISO 5832-2、ISO 5832-3、ISO 5832-11等標準規定的不銹鋼、純鈦、鈦合金材料,通過常規的機械加工、熱處理及表面處理工藝(例如鈍化、電解拋光、陽極氧化等)制成,不包含全新結構設計的產品,不包括3D打印等創新工藝。適用于四肢骨折內固定。 13-01-01 金屬鎖定接骨螺釘 產品由符合GB 4234、ISO 5832-1標準規定的不銹鋼和符合GB/T 13810、ISO 5832-2、ISO 5832-3、ISO 5832-11標準規定的純鈦、Ti6Al4V、Ti6Al4VELI、Ti6Al7Nb鈦合金材料,通過常規的機械加工、熱處理及表面處理工藝(例如鈍化、電解拋光、陽極氧化等)制成,不包含全新結構設計的產品,不包括3D打印等創新工藝。適用于四肢骨折內固定。 13-01-01 金屬接骨螺釘(非鎖定) 該類產品結構參見 YY 0018,產品由符合GB 4234、ISO 5832-1標準規定的不銹鋼和符合GB/T 13810、ISO 5832-2、ISO 5832-3、ISO 5832-11標準規定的純鈦、Ti6Al4V、Ti6Al4VELI、Ti6Al7Nb鈦合金材料,通過常規的機械加工、熱處理及表面處理工藝(不包括3D打印等創新工藝)制成。可單獨使用,適用于四肢骨折內固定。 13-01-01 空心接骨螺釘(非鎖定) 該類產品由符合GB 4234、GB/T 13810、ISO 5832-1、ISO 5832-3標準規定的不銹鋼、鈦合金材料,通過常規的機械加工、熱處理及表面處理工藝(不包括3D打印等創新工藝)制成。可單獨使用,適用于四肢骨折內固定。 13-01-01 解剖型金屬接骨板(非鎖定) 該類產品結構參見YY 0017,由符合GB 4234、GB/T 13810、ISO 5832-1、ISO 5832-2、ISO 5832-3標準規定的不銹鋼、純鈦、鈦合金材料,通過常規的機械加工、熱處理及表面處理工藝(不包括3D打印等創新工藝)制成。適用于四肢干骺端骨折內固定。 13-01-01 直型金屬接骨板(非鎖定) 該類產品結構參見YY 0017,由符合GB 4234、GB/T 13810、 ISO 5832-1、ISO 5832-2、ISO 5832-3標準規定的不銹鋼、純鈦、鈦合金材料,通過常規的機械加工、熱處理及表面處理工藝(不包括3D打印等創新工藝)制成。適用于四肢長骨骨干骨折內固定。 13-01-01 角度型金屬接骨板(非鎖定) 該類產品結構參見YY 0017,由符合GB 4234、GB/T 13810、 ISO 5832-1、ISO 5832-2、ISO 5832-3標準規定的不銹鋼、純鈦、鈦合金材料,通過常規的機械加工、熱處理及表面處理工藝(不包括3D打印等創新工藝)制成。適用于四肢長骨骨干骨折內固定。 13-01-01 U型釘 該類產品結構參見ISO 882,由符合GB 4234、GB/T 13810、 ISO 5832-1、ISO 5832-3標準規定的不銹鋼、鈦合金材料,通過常規的機械加工、熱處理及表面處理工藝(不包括3D打印等創新工藝)制成。適用于四肢骨折內固定。 13-01-01 骨栓 該類產品由螺桿和螺母組成,由符合GB 4234、GB/T 13810、ISO 5832-1、ISO 5832-3標準規定的不銹鋼、鈦合金材料,通過常規的機械加工、熱處理及表面處理工藝(不包括3D打印等創新工藝)制成。適用于四肢骨折內固定。 13-01-01 金屬股骨頸固定釘 該類產品結構參見YY 0346,由符合GB 4234、GB/T 13810、ISO 5832-1、ISO 5832-3標準規定的不銹鋼、鈦合金材料,通過常規的機械加工、熱處理及表面處理工藝(不包括3D打印等創新工藝)制成。適用于股骨頸骨折內固定。 13-01-01 外固定架配合用固定釘 該類產品由符合GB 4234、GB/T 13810、ISO 5832-1、ISO 5832-3標準規定的不銹鋼、鈦合金材料,通過常規的機械加工、熱處理及表面處理工藝(不包括3D打印等創新工藝)制成。與外固定支架配合,適用于四肢骨折復位時部分植入人體做固定。 13-01-01 髖臼螺釘 該類產品由符合GB 4234、GB/T 13810、ISO 5832-1、ISO 5832-2、ISO 5832-3、ISO 5832-11、ISO 5832-12標準規定的不銹鋼、純鈦、鈦合金、鍛造鈷鉻鉬材料,通過常規的機械加工、熱處理及表面處理工藝(不包括3D打印等創新工藝)制成。適用于生物型髖臼假體內固定。 13-01-01 骨缺損填充塊固定螺釘 該類產品由符合GB 4234、GB/T 13810、ISO 5832-1、ISO 5832-2、ISO 5832-3、ISO 5832-11、ISO 5832-12標準規定的不銹鋼、純鈦、鈦合金、鍛造鈷鉻鉬材料,通過常規的機械加工、熱處理及表面處理工藝(不包括3D打印等創新工藝)制成。適用于髖關節、膝關節金屬骨缺損填充塊的固定。 13-01-01 足踝鎖定接骨板系統 該類產品由鎖定接骨板和鎖定接骨螺釘組成,鎖定接骨板由符合GB 4234、GB/T 13810、ISO 5832-1、ISO 5832-2、ISO 5832-3、ISO 5832-11標準規定的不銹鋼、純鈦、鈦合金材料,鎖定接骨螺釘由符合GB 4234、GB/T 13810、ISO 5832-1、ISO 5832-3、ISO 5832-11標準規定的不銹鋼、鈦合金材料,通過常規的機械加工、熱處理及表面處理工藝(不包括3D打印等創新工藝)制成。適用于足踝骨折內固定。 13-01-01 手腕鎖定接骨板系統 該類產品由鎖定接骨板和鎖定接骨螺釘組成。鎖定接骨板由符合GB 4234、GB/T 13810、ISO 5832-1、ISO 5832-2、ISO 5832-3、ISO 5832-11標準規定的不銹鋼、純鈦、鈦合金材料,鎖定接骨螺釘由符合GB 4234、GB/T 13810、ISO 5832-1、ISO 5832-3、ISO 5832-11標準規定的不銹鋼、鈦合金材料,通過常規的機械加工、熱處理及表面處理工藝(不包括3D打印等創新工藝)制成。適用于手腕部骨折內固定 13-01-01 肋骨接骨板系統 該類產品由肋骨接骨板和螺釘組成。由符合GB/T 13810、ISO 5832-2、ISO 5832-3、ISO 5832-11標準規定的純鈦、鈦合金材料,通過常規的機械加工、熱處理及表面處理工藝(不包括3D打印等創新工藝)制成。適用于肋骨骨折內固定。 | ||
| 02單/多部件可吸收骨固定器械 | 一般采用聚乳酸或其共聚物、復合材料等制成。 | 用于非承重部位的骨折內固定術、截骨術、關節融合術中骨折部位的固定。 | 可吸收接骨螺釘、可吸收接骨板、可吸收接骨棒、可吸收板釘系統 | Ⅲ | 同品種 | ||||
| 03單/多部件記憶合金骨固定器械 | 一般采用鎳鈦記憶合金材料制成,具有特定的形狀。 | 利用形狀記憶功能,用于骨折部位的固定。 | 記憶合金聚髕器、記憶合金肋骨板、胸骨固定器、記憶合金環抱器、張力鉤、接骨器、聚髕器 | Ⅲ | 同品種 | ||||
| 04金屬髓內裝置 | 通常由主釘和/或附件組成,主釘通常為管狀、棒狀或針狀。主釘和附件一般采用鈦合金和不銹鋼等材料制成。 | 用于骨折內固定,植入骨髓腔內由螺釘等連接固定。 | 金屬髓內釘、金屬帶鎖髓內釘、金屬髓內針、金屬髓內釘系統、金屬帶鎖髓內釘系統 | Ⅲ | 13-01-04 金屬帶鎖髓內釘 由符合GB 4234、GB/T 13810、ISO 5832-1、ISO 5832-2、ISO 5832-3、ISO 5832-11等標準規定的不銹鋼、純鈦、鈦合金材料,通過常規的機械加工、熱處理及表面處理工藝制成。通常由主釘和/或附件組成,符合YY/T0727系列標準及YY/T0591標準要求,不包含全新結構設計的產品,不包括3D打印等創新工藝。適用于長骨骨折內固定。 13-01-04 金屬髓內針 該類產品結構參見YY 0019,不包含帶鎖髓內釘。由符合GB 4234、GB/T 13810、ISO 5832-1、ISO 5832-3標準規定的不銹鋼、鈦合金材料,通過常規的機械加工工藝、熱處理及表面處理工藝(不包括3D打印等新技術和新工藝)制成;適用于四肢骨折內固定。植入骨髓腔內由螺釘等連接固定。 | ||||
| 05金屬固定環扎裝置 | 通常由金屬帶、金屬扁平條或單股或多股金屬絲組成,還可包含其他附件。一般采用純鈦及鈦合金、不銹鋼、鈷鉻鉬等材料制成。 | 圍繞著長骨,通過絲或螺釘錨定在該長骨上,用于骨折固定。 | 金屬纜線/纜索、柔性金屬絲、金屬纜線/纜索系統 | Ⅲ | 13-01-05 柔性金屬絲 該類產品結構參見YY/T 0816,由符合YY 0605.9、ISO 5832-1、ISO 5832-2標準規定的不銹鋼、純鈦、高氮不銹鋼材料,通過常規的機械加工工藝、熱處理工藝(不包括3D打印等新技術和新工藝)制成。適用于四肢骨折捆扎內固定。 13-01-05 金屬纜線和纜索 該類產品結構參見YY/T 0812,可含有與其配合使用的附件(如鎖定針、束縛器等)。由符合GB/T 13810、YY 0605.9、ISO 5832-1、ISO 5832-2標準規定的不銹鋼、純鈦、高氮不銹鋼、鈦合金材料,符合ASTMF1314標準規定的22Cr-13Ni-5Mn不銹鋼材料、符合ISO5832-5/YY 0605.5標準規定的鍛造鈷鉻鎢鎳合金材料,通過常規的機械加工、熱處理工藝(不包括3D打印等創新工藝)制成。適用于四肢骨折捆扎內固定。 | ||||
| 06光面或帶螺紋的金屬骨固定緊固件 | 通常由一段剛性絲或棒組成。一般采用鈦合金、鈷鉻鉬或不銹鋼等材料制成。可以是直型或U型,端部可以是鋒利(鈍)且可能有加工成型的帶槽的頭。 | 用于骨折固定、骨重建,作為插入其他植入物的導針,也可穿過皮膚植入人體對骨骼系統施加拉力(牽引力)。 | 金屬骨針 | Ⅲ | 13-01-06 金屬骨針 該類產品包括克氏針和斯氏針,結構參見YY 0345。由符合GB 4234、GB/T 13810、ISO 5832-1、ISO 5832-3標準規定的不銹鋼、鈦合金材料,符合ISO 5832-5標準規定的鍛造鈷鉻鎢鎳材料通過常規的機械加工、熱處理及表面處理工藝(不包括3D打印等創新工藝)制成。適用于四肢骨折復位時部分植入人體做牽引、配合外固定支架進行四肢骨折固定或單獨植入用于四肢骨折內固定。 | ||||
| 02 | 運動損傷軟組織修復重建及置換植入物 | 01運動損傷軟組織修復重建植入物 | 通常為鉤狀、釘狀、門型、板狀植入物,或與可植入縫線共同使用。一般采用金屬、高分子、復合材料等制成,附著在固定裝置上的縫線分為可吸收,部分可吸收和不可吸收三大類。 | 用于肩、足、踝、髖、膝、手、腕、肘、半月板、交叉韌帶等部位的軟組織重建和修復。 | 帶線錨釘、界面螺釘(干預螺釘)、門型釘、半月板縫合釘、帶線固定板 | Ⅲ | 13-02-01 不可吸收帶線錨釘 該類產品由錨釘和縫線組成,可帶縫合針。錨釘由符合GB 4234、GB/T 13810、ISO 5832-1、ISO 5832-3、ISO 5832-11標準規定的不銹鋼、鈦合金材料,通過常規的機械加工、熱處理及表面處理工藝(不包括3D打印等創新工藝)制成。縫線可由聚乙烯、聚丙烯、聚酯、聚酰胺等不可吸收材料制成,性能指標符合YY0167標準規定的適用部分。縫合針應符合YY0166和YY0043的要求。該產品可預裝插入器,插入器與人體接觸部分通常由符合YY/T 0294、ASTM F899或YY/T 0726規定的不銹鋼材料制成。適用于骨與軟組織的連接固定。 13-02-01 不可吸收韌帶固定螺釘 該類產品由符合GB 4234、GB/T 13810、ISO 5832-1、ISO 5832-3標準規定的不銹鋼、鈦合金材料,通過常規的機械加工、熱處理及表面處理工藝(不包括3D打印等創新工藝)制成。適用于韌帶的修復和重建。 13-02-01 帶袢鈦板 產品由鈦板、線圈和縫線組成。鈦板應由符合GB/T 13810、ISO 5832-3標準規定的Ti6Al4V、Ti6Al4VELI鈦合金制成,線圈和縫線材質為高分子材料,如聚對苯二甲酸乙二酯,聚丙烯、聚乙烯,聚酯材料。適用于骨科重建術中韌帶或肌腱與骨的固定。 | ||
| 02運動損傷軟組織置換植入物 | 一般采用高分子材料或同種異體組織制成。用于全部或部分地置換損傷組織。 | 用于補償天然組織的損傷。 | 人工韌帶 | Ⅲ | 臨床試驗 | ||||
| 03 | 脊柱植入物 | 01脊柱椎板間固定系統 | 通常由多種鉤、連接桿、植入板、螺釘、螺塞、墊片、連接器等部件組成。一般采用不銹鋼、純鈦、鈦合金等材料制成。通常貫穿3塊相鄰的椎骨,拉直并固定脊柱使椎骨能夠與植入物連接并融合在一起。 | 用于治療脊柱側凸,也可用于治療脊柱的骨折和脫位、重度腰椎滑脫(3、4級)以及下背部綜合征,或脊柱椎管擴大減壓術后的椎板成形等。 | 頸椎后路非椎弓根固定系統、胸腰椎后路非椎弓根脊柱固定系統、枕頸系統、椎板固定板系統 | Ⅲ | 13-03-01 椎板固定板系統 該類產品由固定板和螺釘組成,固定板由符合GB/T 13810 、ISO 5832-2 、ISO 5832-3標準規定的純鈦、鈦合金材料,螺釘由符合GB/T 13810 、ISO 5832-3標準規定的鈦合金材料,通過常規的機械加工、熱處理及表面處理工藝(不包括3D 打印等創新工藝)制成。適用于脊柱椎管擴大減壓術后的椎板成形。 | ||
| 02脊柱椎體間固定/置換系統 | 通常由多種骨板和連接螺釘等組成。一般采用純鈦、鈦合金等材料制成,特殊產品也可采用聚乳酸或其共聚物等材料制成。 | 金屬植入物用于治療脊柱側凸,也可用于脊柱前路椎體固定,或用于椎體置換等。可吸收植入物用于與傳統堅強內固定器械配合使用,在脊柱椎體切除融合術中輔助植骨。 | 頸椎前路固定系統、胸腰椎前路固定系統、可吸收頸椎前路釘板系統、椎體置換系統 | Ⅲ | 同品種 | ||||
| 03脊柱椎弓根系統 | 通常由螺栓、鉤、螺釘、連接裝置、連接棒、連接桿、橫向連接器等多個組件組成。一般采用鈦合金、純鈦、鈷鉻鉬、聚醚醚酮等材料制成。可用于固定脊柱節段。 | 用于治療胸腰椎、骶骨脊柱畸形脊柱滑脫,退行性腰椎滑脫,椎骨骨折、脫位,脊柱側凸,脊柱后凸,脊柱腫瘤,融合失敗等。 | 頸椎椎弓根系統、胸腰椎椎弓根系統 | Ⅲ | 同品種 | ||||
| 04椎間融合器 | 通常由單個或多個部件組成。一般采用金屬、高分子或復合材料制成。可植入頸椎或腰骶的椎體間隙中或用于胸腰椎椎體置換及恢復椎體病變受損而丟失的高度。 | 用于患有椎間盤退行性疾病、椎體滑脫、椎體不穩等病癥的骨骼成熟患者,在一個或兩個相鄰椎體節段上進行融合。 | 頸椎椎間融合器、胸腰椎椎間融合器 | Ⅲ | 同品種 | ||||
| 05椎間盤假體 | 通常由上、下終板和髓核組成。終板一般采用鈷基合金、鈦合金等材料制成,兩面可帶有涂層;髓核一般采用超高分子量聚乙烯、陶瓷等材料制成。可植入椎體間置換人體椎間盤。 | 用于椎間盤置換術,以恢復椎體相鄰節段間的支撐和相對運動。 | 頸椎椎間盤假體、胸腰椎椎間盤假體 | Ⅲ | 臨床試驗 | ||||
| 06棘突植入物 | 通常由單個或多個部件組成。一般采用鈦合金等材料制成。該產品可用于在腰椎棘突間施加一定的撐開力,限制腰椎過度后伸。 | 用于維持腰椎活動節段棘突間的穩定。 | 棘突間植入物 | Ⅲ | 同品種 | ||||
| 04 | 關節置換植入物 | 01髖關節假體 | 通常由髖臼部件和股骨部件組成。一般采用鈦合金、鈷鉻鉬、不銹鋼、超高分子量聚乙烯、陶瓷等材料制成。根據人體髖關節的形態、構造及功能設計,替換髖關節的一個或兩個關節面,通過關節面的幾何形狀來限制其在一個或多個平面內的平移和旋轉。 | 用于外科手術植入人體,代替患病髖關節,達到緩解髖關節疼痛,恢復髖關節功能的目的。 | 髖關節假體系統、髖關節假體、髖臼假體、髖關節股骨假體 | Ⅲ | 同品種 | ||
| 骨水泥型髖關節假體置換術用配件 | 在骨水泥型髖關節置換術中作為配件使用 | 中置器、遠端塞、髖臼杯用孔塞、髓腔塞 | Ⅲ | 13-11 中置器 該類產品由PMMA、符合GB/T19701.2標準規定的超高分子量聚乙烯材料制造。適用于骨水泥型髖關節置換手術中保持股骨柄遠端中置,阻隔骨水泥并確保骨水泥在假體周圍的均勻分布。 13-11 遠端塞 該類產品由PMMA、符合GB/T19701.2標準規定的超高分子量聚乙烯材料制造。適用于骨水泥型髖關節置換術中,阻隔骨水泥。 13-11 髖臼杯用孔塞 產品由符合GB/T 13810、ISO 5832-3標準Ti6Al4V鈦合金制成。配合髖臼杯使用,用于髖臼杯產品孔的填塞。 13-11 髓腔塞 產品由符合GB/T 19701.2、ISO 5834-2標準規定的超高分子量聚乙烯材料制造。用于骨水泥型假體植入手術,作用為防止骨水泥溢入髓腔限制區域,適用部位為股骨、脛骨和肱骨的髓腔。 | |||||
| 02膝關節假體 | 通常由股骨部件、脛骨部件和髕骨部件組成。一般采用鈦合金、鈷鉻鉬、超高分子量聚乙烯等材料制成。根據人體膝關節的形態、構造及功能設計,替代膝關節的一個、兩個或三個間室的關節面。 | 用于外科手術植入人體,代替患病膝關節,達到緩解膝關節疼痛,恢復膝關節功能的目的。 | 膝關節假體系統、膝關節假體、膝關節股脛假體、膝關節髕股假體、膝關節髕股脛假體、膝關節股骨假體、膝關節髕骨假體、膝關節脛骨假體 | Ⅲ | 同品種 | ||||
| 03肩關節假體 | 通常由肱骨部件和關節窩部件組成。一般采用鈦合金、鈷鉻鉬、超高分子量聚乙烯等材料制成。根據人體肩關節的形態、構造及功能設計,替代肩關節的關節面。 | 用于外科手術植入人體,代替患病肩關節,達到緩解肩關節疼痛,恢復肩關節功能的目的。 | 肩關節假體系統、肩關節假體、肩關節肩盂假體、肩關節肱骨假體 | Ⅲ | 同品種 | ||||
| 04肘關節假體 | 通常由肱骨部件和橈骨部件組成。一般采用鈦合金、鈷鉻鉬、超高分子量聚乙烯等材料制成。根據人體肘關節的形態、構造及功能設計,替代肘關節的關節面。 | 用于外科手術植入人體,代替患病肘關節,達到緩解肘關節疼痛,恢復肘關節功能的目的。 | 肘關節假體系統、肘關節假體、肘關節徑向假體、肘關節肱骨假體 | Ⅲ | 同品種 | ||||
| 05 | 骨科填充和修復材料 | 01丙烯酸樹脂骨水泥 | 通常由粉體和液體組成。一般采用甲基丙烯酸甲酯、聚甲基丙烯酸甲酯、丙烯酸酯或聚甲基丙烯酸甲酯和聚苯乙烯共聚物等材料制成。粉體和液體一般經混合攪拌后使用。 | 用于關節成形術、脊柱或創傷手術中金屬或高分子植入物與活體骨的固定。也可用于椎體的填充;固定椎體的骨缺損或與內固定產品一同用于上肢、下肢或骨盆的骨質疏松性骨折治療。 | 丙烯酸樹脂骨水泥 | Ⅲ | 同品種 | ||
| 03 同種異體骨修復材料 | 通常由同種異體骨經過加工制備而成。不含活細胞成分。 | 用于骨缺損、骨不連、骨延遲愈合或不愈合的填充修復,以及脊柱融合、關節融合及矯形植骨修復。 | 同種異體骨修復材料 | Ⅲ | 同品種 | ||||
| 04 金屬填充物 | 一般采用鉭金屬、鈦或鈦合金等材料制成,具有多孔結構或粗糙表面。根據使用部位的不同,具有特定形狀。 | 用于重建由于嚴重退化、創傷或其它病理改變造成的髖關節、膝關節骨缺損;或用于翻修、補救既往關節重建術和植入物失效時的骨缺損;或用于治療未發生股骨頭塌陷的股骨頭壞死。 | 填充塊 | Ⅲ | 13-05-04 填充棒/填充塊 產品由符合ISO 13782標準規定的純鉭制成(不包括3D打印等創新工藝制備產品)。產品單獨使用,用于四肢骨填充。 | ||||
| 06 | 神經內/外科植入物 | 01單/多部件預制顱骨成形術板及緊固件 | 通常由板及緊固件組成。一般采用純鈦、鈦合金、鈷鉻合金等金屬材料以及可吸收或不可吸收高分子材料制成。其中板通過緊固裝置(如螺釘、金屬絲或其它組件)固定就位。 | 用于修補、覆蓋、填充或固定顱骨缺損或孔洞。 | 預制顱骨板系統、可塑形預制顱骨板系統、鈦網、鈦網板系統 | Ⅲ | 同品種 | ||
| 02顱骨夾/鎖 | 通常由單個或多個部件組成。一般采用鈦合金等金屬材料以及可吸收或不可吸收高分子材料制成。 | 用于開顱手術后顱骨瓣的固定。 | 顱骨夾、顱骨鎖 | Ⅲ | 同品種 | ||||
| 03單/多部件顱頜面固定器械及附件 | 通常由一個或多個部件及緊固件組成。一般采用純鈦、鈦合金等金屬材料以及可吸收或不可吸收高分子材料制成。其中板通過緊固裝置(如螺釘或其它組件)固定就位。 | 用于神經外科和頜面外科手術中骨折的固定。 | 顱頜面內固定系統、顱頜面板釘系統 | Ⅲ | 13-06-03 頭釘 產品通常由主體、基座、O形環、橡膠帽組件組合而成,其中僅主體與人體接觸。主體應使用GB 4234、ISO 5832-1、ASTM F899標準規定的不銹鋼或ISO 5832-3、GB/T 13810標準規定的Ti6Al4V、Ti6Al4VELI鈦合金材料制成,產品與顱骨固定器配合使用,在頭骨需要重度修復的外科手術過程中將患者的頭部與頸部固定在特定的位置。該產品為非植入物,僅在術中使用,與人體短期接觸,術后即刻拆除。 13-06-03 顱頜面接骨板系統 由符合GB 4234.1、GB/T 13810、ISO 5832-1、ISO 5832-2、ISO 5832-3標準規定的不銹鋼、純鈦、鈦合金材料,通過常規的機械加工、熱處理及表面處理工藝(不包括3D打印等創新工藝)制成,不包含全新結構設計的產品。適用于顱頜面骨折內固定。修補、覆蓋、填充骨缺損或孔洞者除外。 | ||||
| 05動脈瘤夾 | 通常由單個部件組成。一般采用鈦合金等金屬材料制成。用于使顱內動脈瘤頸或囊閉塞的裝置。 | 用于顱內動脈瘤瘤頸或瘤體的永久性閉塞治療。 | 動脈瘤夾、腦動脈瘤夾 | Ⅲ | 13-06-05 動脈瘤夾 一般采用鈦合金等金屬材料制成。用于使顱內動脈瘤頸或囊閉塞的裝置。用于顱內動脈瘤瘤頸或瘤體的永久性閉塞治療,也可用于動靜脈畸形小血管或動靜脈瘺的永久性閉塞治療。產品與已獲準境內注冊產品具有等同性,產品組成材料成熟。新型結構設計、新型作用機理、藥械組合產品除外。 | ||||
| 06顱內支架系統 | 通常由支架和/或輸送系統組成。支架一般采用金屬材料制成,可覆高分子材料制成的膜。經腔放置的植入物,擴張后通過提供一個機械性的支撐,以維持或恢復顱內血管的通暢性,或輔助彈簧圈治療出血性病變。 | 用于治療顱內、顱底動脈血管狹窄或輔助彈簧圈治療顱內動脈瘤等其他出血性病變。 | 顱內支架 | Ⅲ | 臨床試驗 | ||||
| 08顱內彈簧圈系統 | 通常由彈簧圈和輸送導絲組成。彈簧圈的繞絲一般采用鉑鎢、鉑銥合金等金屬材料制成,芯絲一般采用聚丙烯等高分子材料制成,部分彈簧圈表面可能含有聚酯纖維等高分子材料的纖毛。彈簧圈植入顱內可阻斷異常血流。 | 用于在神經顱內手術中治療顱內動脈瘤及其他神經血管異常的栓塞。 | 顱內彈簧圈 | Ⅲ | 同品種 | ||||
| 09人工顱骨 | 一般采用硅橡膠與滌綸網膜材料復合而成,也可采用聚醚醚酮、鈦合金等材料制成。 | 用于缺損顱骨的替代或重建。 | 人工顱骨 | Ⅲ | 同品種 | ||||
| 11顱內動脈瘤血流導向裝置 | 通常由編織植入物和輸送系統組成。編織植入物一般選用鈷鉻合金和鉑鎢合金材料制成,輸送導絲一般為不銹鋼材料制成。由多股金屬絲編織而成的植入物采用密網設計可以限制血流繼續進入動脈瘤體,從而使動脈瘤內血流停滯,直至瘤體逐漸縮小。 | 用于血管腔內治療成人頸內動脈巖段至垂體上動脈開口處近端的大或巨大寬頸動脈瘤。 | 顱內動脈瘤血流導向裝置 | Ⅲ | 臨床試驗 | ||||
| 07 | 心血管植入物 | 01血管內假體 | 通常由假體和/或輸送系統組成。假體通常由移植物(覆膜)和支撐結構組成,移植物一般采用高分子材料制成。支撐結構一般采用金屬材料制成,支撐結構通過縫合或嵌入的方式固定在移植物上。血管內假體一端可設計為錨定結構,以增強假體的固定能力。通過將血管內假體部分或全部置于血管管腔內,對患者的自體血管或人工血管進行修復、替換或者建立旁路血管通道。 | 用于治療動脈瘤、動脈夾層等血管病變。 | 胸主動脈覆膜支架、腹主動脈覆膜支架、術中支架 | Ⅲ | 臨床試驗 | ||
| 02血管支架 | 通常由支架和/或輸送系統組成。支架一般采用金屬或高分子材料制成,其結構一般呈網架狀。經腔放置的植入物擴張后通過提供機械性的支撐,以維持或恢復血管管腔的完整性,保持血管管腔通暢。支架可含或不含表面改性物質(不含藥物),如涂層。為了某些特殊用途,支架可能有覆膜結構。 | 用于治療動脈粥樣硬化、以及各種狹窄性、阻塞性或閉塞性等血管病變。 | 冠狀動脈支架、外周動脈支架、肝內門體靜脈支架 | Ⅲ | 臨床試驗 | ||||
| 通常由支架和/或輸送系統組成。支架一般采用金屬或高分子材料制成,其結構一般呈網架狀。經腔放置的植入物擴張后通過提供機械性的支撐,以維持或恢復血管管腔的完整性,保持血管管腔通暢。支架可含或不含表面改性物質,如涂層。為了某些特殊用途,支架可能有覆膜結構。含有藥物成分。 | 用于治療動脈粥樣硬化、以及各種狹窄性、阻塞性或閉塞性等血管病變。 | 藥物洗脫冠狀動脈支架、藥物洗脫外周動脈支架 | Ⅲ(藥械組合產品) | 臨床試驗 | |||||
| 03腔靜脈濾器 | 通常由腔靜脈濾器和/或輸送系統組成。腔靜脈濾器一般采用金屬材料制成。經腔放置的植入物擴張后通過機械過濾的方式來預防肺栓塞。 | 用于機械過濾下腔靜脈來預防肺栓塞。 | 永久腔靜脈濾器、可回收腔靜脈濾器、可轉換回收腔靜脈濾器 | Ⅲ | 臨床試驗 | ||||
| 04人工血管 | 一般采用完全或部分的生物材料、合成編織型材料、合成非編織型材料制成。 | 用于置換血管、在血管間旁路移植或形成分流。 | 人工血管 | Ⅲ | 臨床試驗 | ||||
| 06人工心臟瓣膜及瓣膜修復器械 | 一般采用高分子材料、動物組織、金屬材料制成,可含或不含表面改性物質。 | 用于替代或修復天然心臟瓣膜(如主動脈瓣、二尖瓣、肺動脈瓣及三尖瓣)。 | 外科生物心臟瓣膜、外科機械心臟瓣膜、經導管植入式心臟瓣膜、心臟瓣膜成形環 | Ⅲ | 臨床試驗 | ||||
| 07心臟封堵器 | 通常由封堵器和/或輸送系統組成。封堵器的網狀或傘狀結構一般采用金屬材料制成,其余部分一般采用高分子材料制成,放置于心臟缺損、異常通路或特殊開口等處,并封堵該位置,達到阻止異常血流流通的目的。 | 用于治療先天性心房間隔缺損、心室間隔缺損和動脈導管未閉、卵圓孔未閉等疾病。 | 房間隔缺損封堵器、室間隔缺損封堵器、動脈導管未閉封堵器、左心耳封堵器 | Ⅲ | 臨床試驗 | ||||
| 08 | 耳鼻喉植入物 | 01聽小骨假體 | 一般采用鉑金屬、不銹鋼、純鈦或鈦合金等金屬材料制成,亦有產品采用羥基磷灰石制成。 | 用于傳導性耳聾,對全部或部分聽小骨鏈施行置換手術。 | 生物陶瓷聽小骨置換假體、聽小骨假體 | Ⅲ | 同品種 | ||
| 02耳內假體 | 一般采用不銹鋼、鈦合金等金屬材料和/或聚四氟乙烯等高分子材料制成。 | 用于植入耳內,以重建聲音傳導鏈或治療鐙骨不能移動的耳硬化癥,也可用于預防中耳積液。 | 通風管 | Ⅲ | 同品種 | ||||
| 09 | 整形及普通外科植入物 | 02整形用注射填充物 | 通常由注射器以及預裝在注射器中的填充材料組成。 | 用于注射到真皮層和/或皮下組織,以填充增加組織容積。 | 注射用交聯透明質酸鈉凝膠、注射用透明質酸鈉凝膠、膠原蛋白植入劑、注射用聚左旋乳酸填充劑 | Ⅲ | 臨床試驗 | ||
| 03乳房植入物 | 通常由外殼和殼內填充物組成。植入體外殼一般采用多層醫用硅橡膠制成,殼內充有醫用級硅凝膠等材料。 | 用于隆乳和乳房再造。 | 人工乳房植入體、乳房植入體、硅凝膠填充乳房植入體 | Ⅲ | 臨床試驗 | ||||
| 04外科補片/外科修補網 | 一般采用一種或多種合成高分子生物材料或天然高分子生物材料制成。 | 用于植入人體,加強和修補不完整的腹壁和/或腹股溝區等軟組織的缺損。 | 疝氣補片、外科修復補片、外科修復網、疝修補補片 | Ⅲ | 13-09-04 外科疝修補補片 腹腔外置疝補片:植入體內的補片(如平片、網塞等),由聚丙烯、聚對苯二甲酸乙二醇酯或聚偏二氟乙烯材料制成,可帶有部分可吸收材料,用于腹腔外對疝與腹壁缺損進行修補;腹腔內置疝修補補片:腹壁側由聚丙烯、聚對苯二甲酸乙二醇酯或聚偏二氟乙烯材料制成,腹腔側由可降低粘連的材料制成,用于腹腔內對疝與腹壁缺損進行修補。上述兩類補片與已獲準境內注冊產品具有等同性,組成材料成熟,可降低粘連的材料在上市同類產品中已應用。新型結構設計、新型作用機理、藥械組合產品除外。不包括最終全部吸收的產品及以自體組織重建實現修復的產品。 | ||||
| 05修補固定器 | 通常由縫釘和置入裝置(器械桿、手柄、擊發扳機)組成。 | 在多種微創及開放外科手術(如疝修補術)中,用于固定對軟組織進行修補的材料。 | 可吸收釘修補固定器、可吸收夾固定裝置、固定夾 | Ⅲ | 同品種 | ||||
| 06非血管支架 | 通常由支架和/或輸送系統組成。支架一般采用金屬材料制成,可覆高分子材料制成的膜。經腔放置的植入物擴張后通過提供機械性的支撐,以維持或恢復腔道的完整性。 | 用于預防非血管腔道的狹窄或重建腔道的結構和/或功能,也可用于膽汁/胰液的內引流。 | 膽道支架、尿道支架、腸道支架、氣管支架、食道支架、前列腺尿道支架、胰管支架、十二指腸支架、結腸支架、幽門支架、氣管造口支架系統、鼻竇支架 | Ⅲ | 13-09-06 膽道/胰管/輸尿管支架 支架由不可降解/吸收的高分子材料(如聚乙烯、聚氨酯等)制成管狀結構,可帶有不透射線標記等組件,可涂有涂層,可包含輸送器組件。用于在內窺鏡下植入腔道,擴張植入部位的狹窄,進行引流。與已獲準境內注冊產品具有等同性。產品組成材料成熟,新型結構設計、新型作用機理、藥械組合產品除外。 13-09-06 非血管自擴張金屬支架 支架由具有形狀記憶性能的金屬(如鎳鈦合金等)制成,可帶有不透射線標記,可有/無覆膜,可包含輸送器組件。用于擴張食道、膽道、氣道、腸道等非血管部位的狹窄。與已獲準境內注冊產品具有等同性。產品組成材料成熟,新型結構設計、新型作用機理、藥械組合產品除外。 | ||||
| 07支氣管內活瓣 | 通常由活瓣、輸送導管、裝載器和氣道定徑套件(玻璃注射器、活塞和量規)組成。活瓣支撐架一般采用鎳鈦合金制成,覆有聚氨酯膜。 | 用于控制氣流以改善病變分布不均勻的肺氣腫患者的肺功能及減少漏氣。 | 支氣管內活瓣 | Ⅲ | 臨床試驗 | ||||
| 10 軟組織擴張器 | 一般由擴張器殼體、導管、注射座及連接管組成,其中注射閥由硅橡膠和不銹鋼碗組成。 | 用于獲取自體皮膚組織以解決皮膚供區不足,也可用于頭皮缺損、禿發再造、耳鼻再造和各類疤痕的修補。 | 軟組織擴張器 | Ⅲ | 13-09-10 組織擴張器 一般由殼體、導管、注射座(或起相同作用的組件)和連接器(如果有)等組成。殼體的主要材料為硅橡膠。作用原理為可填充鹽水以增大自身體積對組織進行擴張。用于獲取自體皮膚組織以解決皮膚供區不足,手術中使用或植入6個月內取出。與已獲準境內注冊產品具有等同性。新型結構設計、藥械組合產品除外。 | ||||
| 10 | 組織工程支架材料 | 01脫細胞皮膚 | 通常由異種或同種異體皮膚組織經一系列處理后制成,包括真皮層及表皮層,其主要成分為膠原蛋白。不含活細胞成分。 | 用于皮膚缺損創面的修復,引導患者皮膚組織的修復和再生。 | 脫細胞豬皮、脫細胞異體皮膚 | Ⅲ | 臨床試驗 | ||
| 02脫細胞真皮基質 | 通常由異種或同種異體皮膚組織經一系列處理后制備的脫細胞真皮基質制成,其主要成分為膠原蛋白。不含活細胞成分。 | 用于真皮層缺損的創面修復,引導患者皮膚組織缺損的修復和再生。 | 豬皮脫細胞真皮基質、脫細胞異體真皮基質 | Ⅲ | 臨床試驗 | ||||
| 03 膠原蛋白支架材料 | 通常為膠原蛋白。不含活細胞成分。 | 用于皮膚、真皮的修復和再生。 | 醫用膠原修復膜 | Ⅲ | 臨床試驗 | ||||
| 04神經修復材料 | 通常由異種或同種異體的神經或肌腱組織經脫細胞處理后獲得的細胞外基質制成。或者由人工合成高分子材料或天然高分子材料制成。不含活細胞成分。 | 用于修復各種原因所致的外傷性神經缺損。 | 脫細胞同種異體神經修復材料、脫細胞人工神經鞘管、聚乳酸人工神經管、神經套管 | Ⅲ | 臨床試驗(生物型) | ||||
| 05 含重組人骨形態發生蛋白質的骨修復材料 | 通常在異種骨、同種異體骨、膠原、無機鈣鹽類材料、可吸收高分子材料中的一種或兩種以上的復合材料中加入骨形態發生蛋白質-2(BMP-2)。 | 用于骨缺損、骨不連、骨延遲愈合或不愈合的填充修復,以及脊柱融合、關節融合及矯形植骨修復。 | 含蛋白質-2(rhBMP-2)的骨修復材料、含蛋白質-2(rhBMP-2)的膠原基骨修復材料 | Ⅲ(藥械組合產品) | 臨床試驗 | ||||
| 11 | 其他 | 02漏斗胸成形系統 | 通常由肋骨成形板、固定片、固定桿等部件組成。一般由純鈦、鈦合金或不銹鋼等材料制成。 | 用于漏斗胸和其他胸骨畸形成形術中的內固定。 | 漏斗胸成形系統、縱向胸廓成形人工鈦肋系統 | Ⅲ | 同品種 | ||
| 03 胸骨捆扎/抓扣固定系統 | 通常由結扎帶和穿引彎鉤兩部分組成,其中穿引彎鉤非植入人體,僅用于輔助結扎帶穿引安裝,安裝后廢棄。也可由上下片及螺釘組成。也可由帶或不帶夾子的捆綁鋼纜、粗隆爪、鋼纜釘、鋼纜螺絲釘、鋼板組成。 | 用于開胸術中的胸骨固定。器械可單獨使用,也可與其它傳統不銹鋼絲配合使用。 | 胸骨結扎帶 | Ⅲ | 13-11-03 胸骨結扎帶 產品由符合GB/T 13810、ISO 5832-3、ISO 5832-11、ISO 5832-1標準規定的Ti6Al4V、Ti6Al4VELI、Ti6Al7Nb鈦合金材料、不銹鋼材料制成,穿引彎鉤也可由符合ASTM F899標準規定的材料制成,產品通常由結扎帶和穿引彎鉤兩部分組成,其中穿引彎鉤非植入人體,僅用于輔助結扎帶穿引安裝,安裝后廢棄。用于開胸術中的胸骨固定。不包含全新結構設計的產品。 | ||||
