醫療器械臨床試驗設計過程中,評價指標的選擇關系到一個試驗的成敗,決定了整個臨床研究的高度、研究可推廣性以及樣本量,是臨床試驗設計中一個非常重要的影響因素,本文介紹了醫療器械臨床試驗評價指標的確認依據及確定方法。
一、醫療器械臨床評價指標定義
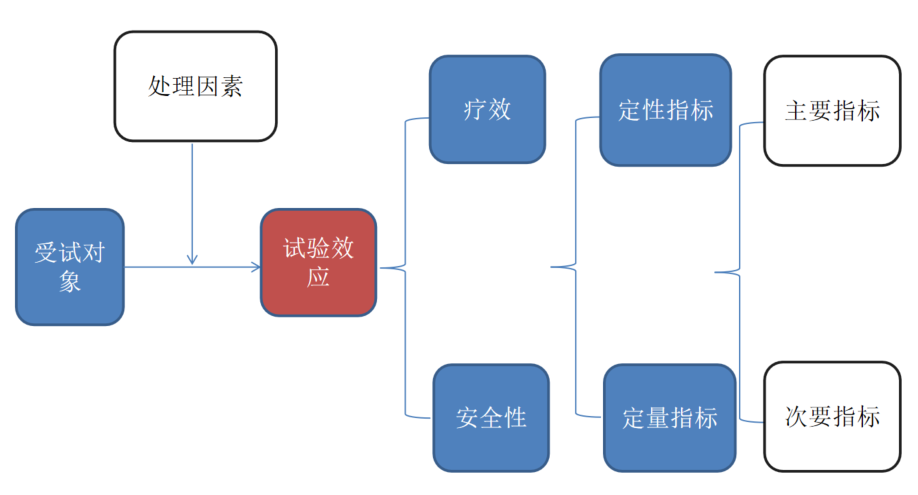
醫療器械臨床試驗的評價指標是反映醫療器械作用于受試對象而產生的各種效應,應當根據試驗目的和醫療器械的預期效應來設定。臨床試驗評價指標分為主要指標和次要指標,根據評價標準又分為定量指標、定性指標和等級指標。
對于診斷器械,臨床試驗評價指標通常包括定性檢測的診斷準確性(靈敏度、特異性、預期值、似然比、 ROC 曲線下面積等)或檢測一致性(陽性 / 陰性一致性、總一致性、 KAPA 值等),以及定量檢測回歸分析的斜率、截距和相關系數等
二、醫療器械臨床評價選擇原則
1. 盡量選擇客觀性強、易于量化、重復性高、在相關領域已有公認標準的指標,以控制評價偏倚、保證試驗質量;
2. 通常來源于已發布的相關標準或技術指南、公開發表的權威論著或專家共識等
3. 如果必須選擇有主觀成分的指標,應在試驗方案中規定判斷等級的依據和理由。
如椎體后凸成型術,選擇疼痛或解剖學指標:椎體高度、 Cobb ’ s 角 .
三、醫療器械臨床評價指標的確認依據
醫療器械臨床試驗設計中評價指標的確認應充分認識試驗產品的適用范圍、產品特點、工作原理,初步確定試驗產品的臨床效能,結合相關產品指導原則,同類產品臨床文獻及數據,獲得試驗產品的臨床研究終點,最終與研究者和統計師確認,其確認依據主要有:
- 臨床試驗目的:有效性、安全性、新增功能
- 試驗產品的適應癥(說明書)
- 相關技術指導原則
- 相關標準或技術指南
- 臨床專家共識及符合統計學意義
- 公開發表的權威論著
- 臨床常用標準、創建評價標準
四、醫療器械臨床試驗設計中評價指標確認案例
1. 當更關注試驗器械的安全性是否可滿足臨床使用的需要,其臨床試驗目的可設定為確認試驗器械的安全性是否優于 / 等效于 / 非劣于已上市同類產品,同時確認試驗器械的有效性。此時,臨床試驗的主要評價指標為安全性指標 。 乳房植入體 為例,臨床試驗通常選擇并發癥發生率(如包膜攣縮率、植入體破裂率)作為主要評價指標
2. 對于已上市產品增加適應癥的情形,臨床試驗目的可設定為確認試驗器械對新增適應癥的安全有效性 : 止血類產品 在已批準適用范圍(如普通外科、婦產科)的基礎上,增加眼科、神經外科、泌尿外科使用的適應癥
3. 當已上市器械適用人群發生變化時,臨床試驗目的可設定為確認試驗器械對新增適用人群的安全有效性 。如膜式氧合器產品,在原批準適用范圍的基礎上新增體重 ≤ 10kg 的適用人群;治療類呼吸機在已批準的適用于成人的基礎上新增適用于兒童的適用范圍。
4. 當已上市器械發生重大設計變更時,可根據變更涉及的范圍設定試驗目的。例如冠狀動脈藥物洗脫支架平臺花紋設計發生改變時,臨床試驗目的可設定為確認變化部分對于產品安全有效性的影響
5. 當已上市器械的使用環境或使用方法發生重大改變時,試驗目的可設定為確認產品在特定使用環境和使用方法下的安全有效性 。如已上市的植入式心臟起搏器通常不能兼容核磁共振檢查,如申請兼容核磁共振檢查,其臨床試驗目的可設置為對兼容核磁共振檢查相關的安全有效性進行確認。
