近期藥械圈搜索詞排行榜占首位的一定是應急審批,但隨著疫情的好轉,各地藥品監督管理部門都陸續發布關于停止應急審批申請有關事項的通告。例如:江蘇省3月22日發通知:停止受理醫用防護服醫用口罩應急審批申報申請有關事項。
隨著應急審批通關的關閉,針對應急審批的醫療器械注冊證到期后,部分省將優先納入到優先審批通道,與應急審批相似,醫療器械優先審批同樣在注冊申請、技術審評、行政審查等環節優先安排,能給生產企業注冊申報醫療器械帶來不少的便利。
優先審批的優勢:
1. 審批優先排隊
器審中心對列入優先審批的醫療器械注冊申請,按照接收時間單獨排序,優先進行技術審評。
2. 體系核查優先
對于優先審批的項目,省級食品藥品監督管理部門優先安排醫療器械注冊質量管理體系核查。
3. 審批優先
對于優先審批的項目,器審中心在技術審評報告中注明為優先審批項目,國家食品藥品監督管理總局優先進行行政審批。
4. 專項交流
對于優先審批的項目,器審中心在技術審評過程中,應當按照相關規定積極與申請人進行溝通交流,必要時,可以安排專項交流。
5. 優先審批過程分同步確定
對于申請優先審批的境內醫療器械注冊申請項目,器審中心確認該產品屬于第二類醫療器械的,受理部門及時將第二類醫療器械注冊申報資料和分類意見轉申請人所在地省級食品藥品監督管理部門審評審批。
這些優勢促使產品整個注冊上市周期提前,為企業迎得了上市的時間,搶占市場先機。
申請優先審批的條件:
國家食品藥品監督管理總局對符合下列條件之一的境內第三類和進口第二類、第三類醫療器械注冊申請實施優先審批:
(一)符合下列情形之一的醫療器械:
1.診斷或者治療罕見病,且具有明顯臨床優勢;
2.診斷或者治療惡性腫瘤,且具有明顯臨床優勢;
3.診斷或者治療老年人特有和多發疾病,且目前尚無有效診斷或者治療手段;
4.專用于兒童,且具有明顯臨床優勢;
5.臨床急需,且在我國尚無同品種產品獲準注冊的醫療器械。
(二)列入國家科技重大專項或者國家重點研發計劃的醫療器械。
(三)其他應當優先審批的醫療器械。
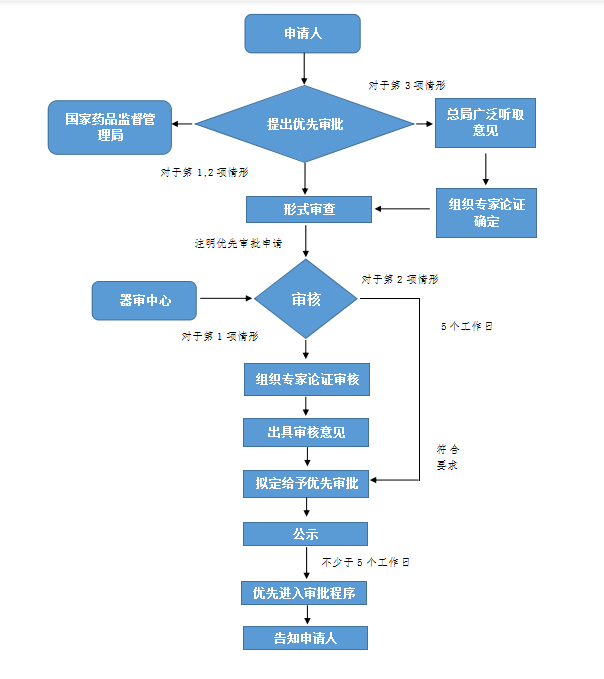
優先審批的流程及要求: