自2015年4月1日起,新《醫療器械監督管理條例》(650號令)下醫療器械注冊證到期延續注冊過渡期結束,所有醫療器械注冊證書應在有效期屆滿6個月前向食品藥品監督管理部門提出延續注冊申請,而原《條例》規定的重新注冊不再適用。
依據新的醫療器械監督管理條例規定,醫療器械注冊證書到期前可申請延續注冊,取代了原《條例》規定的重新注冊申請,新的《醫療器械注冊管理辦法》和《體外診斷試劑注冊管理辦法》自2014年10月1日起生效,延續注冊也隨之正式實施,我們可以從下圖了解新《條例》醫療器械延續申請是如何實施。
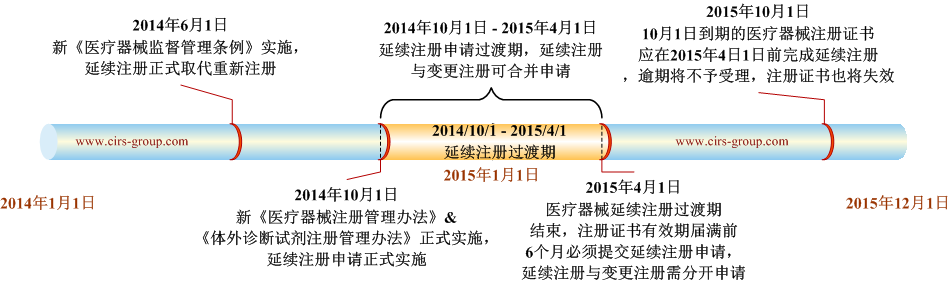
醫療器械企業應關注其中的幾個關鍵時間點:
- 2014年6月1日: 新《醫療器械監督管理條例》正式生效,延續注冊取代重新注冊;
- 2014年10月1日: 新《醫療器械注冊管理辦法》和《體外診斷試劑注冊管理辦法》正式生效,延續注冊正式開始實施;
- 2015年4月1日:醫療器械延續注冊6個月的過渡期結束,延續注冊與變更注冊需分開申請;
哪些情況下延續注冊申請不被受理:
- 注冊人未在規定期限內提出延續注冊申請的;
- 醫療器械強制性標準已經修訂,該醫療器械不能達到新要求的;
- 對用于治療罕見疾病以及應對突發公共衛生事件急需的醫療器械,批準注冊部門在批準上市時提出要求,注冊人未在規定期限內完成醫療器械注冊證載明事項的。
注:企業應及時關注醫療器械相關國家標準及行業標準的修訂情況,一旦強制性標準修訂,企業應及時調整產品技術要求,直到達到新的標準要求。
醫療器械延續注冊申報資料要求:
- 申請表 (采用新的申報軟件編寫)
- 證明性文件,主要包括企業營業執照、組織機構代碼證、代理人委托書、代理人承諾書等。
- 關于產品沒有變化的聲明
- 原醫療器械注冊證及其附件的復印件、歷次醫療器械注冊變更文件復印件
- 注冊證有效期內產品分析報告
- 產品臨床應用情況,用戶投訴情況及采取的措施。
- 醫療器械不良事件匯總分析評價報告,報告應對本產品上市后發生的可疑不良事件列表、說明在每一種情況下生產企業采取的處理和解決方案。對上述不良事件進行分析評價,闡明不良事件發生的原因并對其安全性、有效性的影響予以說明。
- 在所有國家和地區的產品市場情況說明。
- 產品監督抽驗情況(如有)。
- 如上市后發生了召回,應當說明召回原因、過程和處理結果。
- 原醫療器械注冊證中載明要求繼續完成工作的,應當提供相關總結報告,并附相應資料。
如醫療器械強制性標準已經修訂,應提供產品能夠達到新要求的產品檢驗報告。產品檢驗報告可以是自檢報告、委托檢驗報告或符合強制性標準實施通知規定的檢驗報告。其中,委托檢驗報告應由具有醫療器械檢驗資質的醫療器械檢驗機構出具。
7. 符合性聲明及其它文件1)注冊人聲明本產品符合《醫療器械注冊管理辦法》和相關法規的要求;聲明本產品符合現行國家標準、行業標準,并提供符合標準的清單。
2)所提交資料真實性的自我保證聲明(境內產品由注冊人出具,進口產品由注冊人和代理人分別出具)。
3)如在原醫療器械注冊證有效期內發生了涉及產品技術要求變更的,應當提交依據注冊變更文件修改的產品技術要求一式兩份。
相關鏈接:
