醫用隔離眼罩作為疫情防控重要醫用防護產品,依據醫療器械法規,按照第一類醫療器械管理,因此企業在生產銷售前應獲得產品備案憑證和生產備案憑證。瑞旭集團依據相關法規及標準規范要求,將醫用隔離眼罩的備案過程中的技術細節整理于本文中供參考。
1、醫用隔離眼罩結構組成:
醫用隔離眼罩通常由高分子材料制成的防護罩、泡沫條和固定裝置組成。非無菌提供,一次性使用。
2、醫用隔離眼罩適用范圍:
用于醫療機構中檢查治療時起防護作用,阻隔體液、血液飛濺或潑濺。
3、醫用隔離眼罩分類信息
分類編碼 | 子目錄 | 一級產品類別 | 二級產品類別 | 產品描述 | 預期用途 | 品名舉例 | 管理類別 |
14-14-06 | 14注輸、護理和防護器械說明 | 14 醫用人員防護用品 | 06隔離護罩 | 通常由高分子材料制成的防護罩、泡沫條和固定裝置組成。非無菌提供,一次性使用。 | 用于醫療機構中檢查治療時起防護作用,阻隔體液、血液飛濺或潑濺。 | 醫用隔離面罩、醫用隔離眼罩 | Ⅰ |
4、醫用隔離眼罩類型
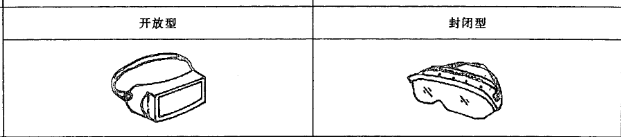
其中鏡片類型包括:1)無機鏡片;2)有機鏡片;3)膠合鏡片:由黏結劑將多層鏡片粘合而成。
5、醫用隔離眼罩主要技術指標
5.1 材料
a 佩戴者接觸的部分不應使用會引起皮膚刺激的材料;
b 防護部分的材料應滿足其功能的需求
5.2 結構
a 表面光滑、無毛刺、無銳角或可能引起眼面部不舒適感的其他缺陷;
b 具有良好的透氣性;
c 可調零件或結構部件應易于調節和替換。
5.3 頭箍
在于佩戴者接觸的任一部分頭箍至少應保持10mm寬,頭箍應能調節,選用的材料應質地柔軟,經久耐用。
5.4鏡片規格
a 單鏡片:長*寬尺寸不小于:105*50mm;
b 雙鏡片:圓鏡片的直徑不小于40mm;成形鏡片的水平基準長度*垂直高度尺寸不小于:30mm*25mm
5.5 鏡片的外觀質量
鏡片表面應光滑、無劃痕、波紋、氣泡、雜質或其他可能有損視力的明顯缺陷。
5.6光學性能
5.6.1屈光度互差為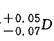 ;
;
5.6.2棱鏡度
a)平面性鏡片棱鏡度互差不得超過0.125 ;
b)曲面型鏡片的鏡片中心與其他各點之間垂直和水平棱鏡度互差均不的超過0.125 ;
c)左右眼鏡片的棱鏡度互差不得超過0.18 。
5.6.3可見光投射比
a)在鏡片中心范圍內,濾光鏡可見光投射比的相對誤差應符合表1所規定的范圍。
表1 濾光鏡可見光透射比相對誤差
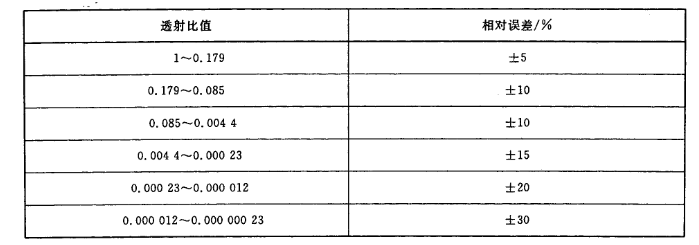
b)無色透明鏡片:可見光透射比應大于0.89。
5.7抗沖擊性能
能經受直徑為22mm、重約45g鋼球從1.3m高度自由落下的沖擊。
5.7.1鏡片
按照GB 14866-2006中6.2.1規定的方法測試,不應發生下列缺陷:
a) 鏡片破損:如鏡片碎裂為二片或二片以上,或者從鋼球沖擊的另一表面脫落大于5mg的碎片,或者鋼球穿透鏡片,則認為該鏡片已破損;
b) 鏡片變形:經鋼球撞擊后,鏡片背面的白紙上出現斑點,則可認為其變形。
57.2 眼護具
按照GB 14866-2006中6.2.1規定的方法測試,不應發生下列缺陷:
a) 鏡片破損:同7.1 a);
b) 鏡片變形:同7.1 b);
c) 眼護具框架破損:經鋼球撞擊后,其分離成幾個部分,或其不在具有裝夾鏡片的能力,則可認為其破損。
5.8耐熱性能
按照GB 14866-2006中6.3規定的方法測試后,應無異常現象出現。鏡片的光學性能在6規定的范圍內變化。
5.9耐腐蝕性能
按照GB 14866-2006中6.4規定的方法測試后,眼罩的所有金屬部件應呈無氧化的光滑表面。
5.10有機鏡片表面耐磨性能
按照GB 14866-2006中6.5規定的方法測試后,鏡片表面磨損率H應低于8%。
5.11 防高速粒子沖擊性能
應符合GB 14866-2006中5.11的規定。
5.12 熔融金屬和熾熱固體防護性能
眼罩對眼部提供防護的所有零件的材料應為非金屬或經過防熔融金屬粘附及抗熾熱固體穿透的處理。
a)按照GB 14866-2006中6.7.1規定的方法測試后,鏡片無熔融金屬粘附或破損;
b)按照GB 14866-2006中6.7.2規定的方法測試后,在7s內沒有發現鋼球完全穿透鏡片。
5.13化學霧滴防護性能
應符合GB 14866-2006中5.13的規定。
5.14 粉塵防護性能
按照GB 14866-2006中6.9規定的方法測試后,測試后與測試前的反射率比大于80%。
5.15 刺激性氣體防護性能
按照GB 14866-2006中6.10規定的方法測試后,鏡片中心范圍內試紙無色斑出現。
6、包裝及標簽要求
產品應有合適的包裝,并且必須附有產品合格證和使用說明書。在產品表面不妨礙視野的地方,應表示制造廠名或商標,在包裝上應有下列標識:產品名稱;2)功能標識;3)制造廠名;3)生產日期。
7、醫用隔離眼罩適用的標準:GB 14866-2006
8、醫用隔離眼罩的臨床試驗要求
醫用隔離眼罩作為第一類醫療器械,免于進行臨床試驗,只需要提供臨床評價報告即可。
9、醫用隔離眼罩備案時限
醫用隔離眼罩作為第I類醫療器械,采用備案制,網上申請后現場提交備案資料,審核通過后,當場發放醫用隔離眼罩備案憑證。
其中醫用隔離眼罩備案憑證含兩部分內容:第一類醫療器械備案憑證和第一類醫療器械備案信息表。
