聚對二氧環己酮(PDO)面部埋植線主要用于植入淺表肌肉腱膜系統(SMAS)及其淺層組織以糾正面部皺紋,通過面部軟組織提拉、固定、除皺、塑形和填充以達到面部年輕化。由于其手術微創化、簡單化,PDO面部埋植線在醫療美容機構被廣泛用于美容整形除皺手術。
依據醫療器械法規,PDO面部埋植線作為第III類醫療器械管理,在中國注冊前應先通過臨床試驗驗證其安全性和有效性,本文總結了PDO面部埋植線的臨床試驗要求。
一、機構倫理要求:
符合臨床試驗質量管理文件與《醫療器械臨床試驗質量管理規范》(GCP),需要在二甲資質以上且已經備案的有相關臨床試驗經驗的醫療機構開展。
二、臨床試驗設計
根據可吸收醫療器械產品技術指導則建議臨床試驗采用前瞻性、隨機對照設計,將擬申報器械與已獲準上市器械進行對比。對照器械應與擬申報器械采用類似的材料制成且具有相似的預期用途。
例如設計方法:“評價PDO埋植線在輕中度面中、下部面部提升治療的有效性和安全性前瞻性、多中心、平行、隨機對照、盲法臨床研究”,隨防1年。
三、比較的類型
如優效性檢驗、非劣效性檢驗、等效性檢驗,申請人應說明選擇的依據。
四、樣本量確定依據
試驗例數應具有統計學意義,應足以確保所申報器械將能在臨床使用條件下充分發揮作用。
樣本量的大小應根據受試產品的具體特性、主要有效性(或安全性)評價指標及其估計值、顯著性水平、研究把握度以及臨床試驗比較的類型來確定。應在臨床試驗方案中明確給出具體的樣本量計算公式及其來源出處,說明計算過程中所采用的所有參數及其估計值。建議根據下列五個方面確定所需要的樣本量:
(1)擬采取的試驗設計類型(常分為單組設計、配對設計、成組設計、單因素多水平設計、交叉設計、析因設計、重復測量設計等);
(2)擬采取的比較類型[常分為差異性檢驗(又分為單、雙側檢驗)、等效性檢驗、優效性檢驗和非劣效性檢驗];
(3)參數選擇建議:Ⅰ類錯誤概率α值為雙側0.05(即單側0.025),Ⅱ類錯誤概率β通常不超過0.2(即把握度不小于80%);
(4)主要評價指標的性質[通常分為定量的、定性的(又分為二值的和多值有序的)]和有關的基礎數據及有臨床意義的界值;
(5)應考慮20%以內的脫落率。
對于非劣效和等效性試驗,還應給出具有臨床意義的非劣效界值和/或等效性界值,若為優效性試驗,需要給出優效性界值。對各臨床試驗中心的入選受試者進行分組時,應盡可能基于重要的非試驗因素進行分層隨機化。
樣本量計算舉例(體表縫合為例)
將傷口達甲級愈合患者的比例作為主要評價指標,試驗采用隨機對照的非劣效設計,假設試驗組和對照組有效率(甲級愈合比例)均為98%,非劣效界值取5%,在統計學檢驗顯著性水平取單側0.025,把握度取80%時,每組至少需要入組124例患者,在此基礎上考慮10%的脫落率,最終每組的入選規模確定為138例。
所使用的樣本量計算公式為:
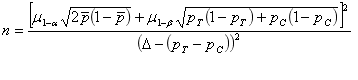
五、研究對象:
5.1納入標準
①身體健康,受試者年齡≧18 周歲。
②短期內未使用影響凝血功能的藥物或已停止使用此類藥物超過2 周者,如阿司匹林、肝素、華法林等;
③術前對面部除皺術的術后效果期望現實,及對本人面部老化程度的認識正確,并同意簽署手術同意書的患者;
④無手術相關藥物過敏史的就診者。
5.2 排除標準
①既往因面部老化曾接受過相關中下面部埋線懸吊術者,如鋸齒線、錐體線等輔助除皺材料植入者;或接受過中下面部外科手術者,如腮腺混合瘤等;
②半年內曾接受面部皮膚物理治療者,如激光、射頻等;
③一年內中下面部曾注射玻尿酸等填充治療者;
④瘢痕體質者;
⑤有嚴重心血管疾病、內分泌免疫疾病沒有得到較好控制者,有血液疾病、傳染性疾病等不適宜手術者;
⑥某些對術后效果預期不現實及對自己面部老化程度的認識不正確,或有明顯心理障礙的患者。
