
摘要
背景:如果皮膚的屏障性能可以暫時和可逆性的降低,那么皮膚為肽的遞送提供了各種益處和潛力。由于肽具有高分子量、親水性(大多數情況)和結構中的可電離基團,因此其皮膚遞送極具挑戰性。除此之外,它們還易受皮膚中蛋白水解酶的影響。抗皺肽與其他肽一樣,存在皮膚滲透性不足的問題,而其中大多數的肽必須深入皮膚才能發揮功效。盡管細胞研究表明了此類肽的有效性,但在不能充分滲透皮膚的情況下,此功效是無用的。抗皺肽的皮膚滲透性差引發了現今所進行的研究,即尋找化妝品消費者所希望的可行且無創的肽皮膚滲透的增強方法。
方法:本文全面綜述了抗皺肽經皮膚滲透的可能性,以及迄今為止用于增加這些難溶性分子滲透性的化學、物理以及包封方法。結果:大多數抗皺肽不適合作為皮膚滲透的備選物質,并且使用增強方法對提高其滲透性至關重要。為此,迄今為止僅有一些增強滲透性的方法的已采用,包括用疏水基團或細胞穿膜肽進行的化學修飾、金屬絡合、化學促滲劑、電離子透入療法、微針和納米載體包封等方法。已發表的對抗皺肽肌肽、GHK肽、PKEK肽、GEKG肽、GQPR肽和KTTKS肽的皮膚滲透性的研究結果表明,這些肽的皮膚滲透性可以成功的被提高。結論:盡管大多數抗皺肽的皮膚滲透性不夠高,且在合適的濃度下大多數抗皺肽可能無法達到其在皮膚中的靶點,但他們的滲透性可以通過各種增強方法達到治療濃度。關鍵詞:抗皺肽、美容肽、增強滲透性的方法、肽的皮膚遞送、皮膚滲透性
01 引言
擁有健康年輕的皮膚是公認的年輕標志。因此,尋找適用且便利的方法來防止衰老是研究界一個突出且有吸引力的話題,其中使用含有肽的局部抗皺產品看起來很有前景。局部肽被分為四個主要類別;信號肽、酶抑制劑肽、神經遞質-抑制劑肽和載體肽[1,2]。通常,信號肽通過刺激基質蛋白的產生起作用。酶抑制劑肽會降低或抑制參與皮膚衰老相關的酶的活性。對乙酰膽堿釋放的抑制由神經遞質-抑制劑肽所引起,載體肽運輸主要的微量元素[2,3]。無論屬于哪一類,肽都不適合作為輸送到皮膚或穿過皮膚的候選物質。抗皺肽的分子量通常大于皮膚的理想分子量界限(即500Da)。它們分配系數(log P)的對數一般小于適合穿過皮膚的logP的范圍(即1–3)。抗皺肽通常是生理PH值下的帶電分子。此外,這些肽分子是皮膚中蛋白水解酶的底物。由于具有這樣的特性,因此肽分子不能在合適的濃度下穿過皮膚[4]。盡管關于抗皺肽皮膚滲透性的文獻很少,但是含有抗皺肽的抗皺產品越來越多地在化妝品市場上推出,且這些產品尚沒有關注到皮膚滲透性是使抗皺肽產生成效的這一先決條件。
雖然衰老會影響皮膚所有的層,但真皮會發生顯著的變性變化[5]。真皮是大多數抗皺肽的作用靶點。為了有效果,這類肽分子必須通過角質層(最重要的皮膚屏障)以及活性表皮,且不會被蛋白水解酶顯著降解。然后,這些肽分子必須以合適的濃度到達真皮,以起到抗皺劑的作用。因此,對于大多數抗皺肽而言,穿過活性表皮的滲透是必需的[6]。根據文獻,大多數肽具有抗皺特性[7,8],例如,棕櫚酰五肽(Pal-KTTKS)可以增加成纖維細胞培養物中膠原蛋白的產生[9],但主要問題是局部應用Pal-KTTKS是否可以到達能真皮處的成纖維細胞。在抗皺肽領域進行的大多數研究都在關注功效而非皮膚滲透性。
以下研究是少數研究局部抗皺肽產品皮膚滲透性的研究。 乙酰基六肽-3是一種合成的神經遞質-抑制肽,分子量為889Da,clog P值為-6.67。這種肉毒桿菌樣肽在化妝品市場上以Argirelin®的品牌名稱出售。使用無毛豚鼠(作為活性皮膚模型)和人(尸)體皮膚評估了來自商業O/W乳劑的乙酰基六肽-3的皮膚滲透。受體相為HEPES緩沖的Hank平衡鹽溶液,供體相為含有10%乙酰基六肽-3的O/W乳劑。無論膜的類型如何,24小時后在真皮和受體相中均未檢測到該肽。在兩種類型膜的表皮中僅發現所用劑量的0.01%。角質層中保留肽的百分比不同,豚鼠和人(尸)體皮膚分別留有施加劑量的0.53%和0.22%。這種差異歸因于嚙齒動物的皮膚比人皮膚具有更高的滲透性[10]。乙酰基六肽-3必須靶向肌肉神經接點并影響面部表情的肌肉,但根據本研究的結果,其并無法到達真皮。 盡管對美容肽的皮膚滲透性進行的研究不多,但所進行的少數研究的結果指出,美容肽對皮膚滲透來說并非最佳備選物質。含有抗皺肽的產品并不便宜。然而,美容肽的皮膚滲透性差,在皮膚上施用后會導致大量的浪費;因此,這種產品的高成本強加給了消費者,卻沒有產生與之相配的肽的抗皺效果。為了克服滲透性差這一問題,研究人員一直試圖使美容肽具有更高的滲透性,以便它們能夠到達皮膚中的靶點。
本文全面綜述了迄今為止為提高美容肽的皮膚滲透性而開展的不同化學、物理和包封方法的研究(圖1)。表1中列出了本文中討論的抗皺肽的序列、MW以及計算的logP 值(clog P)。
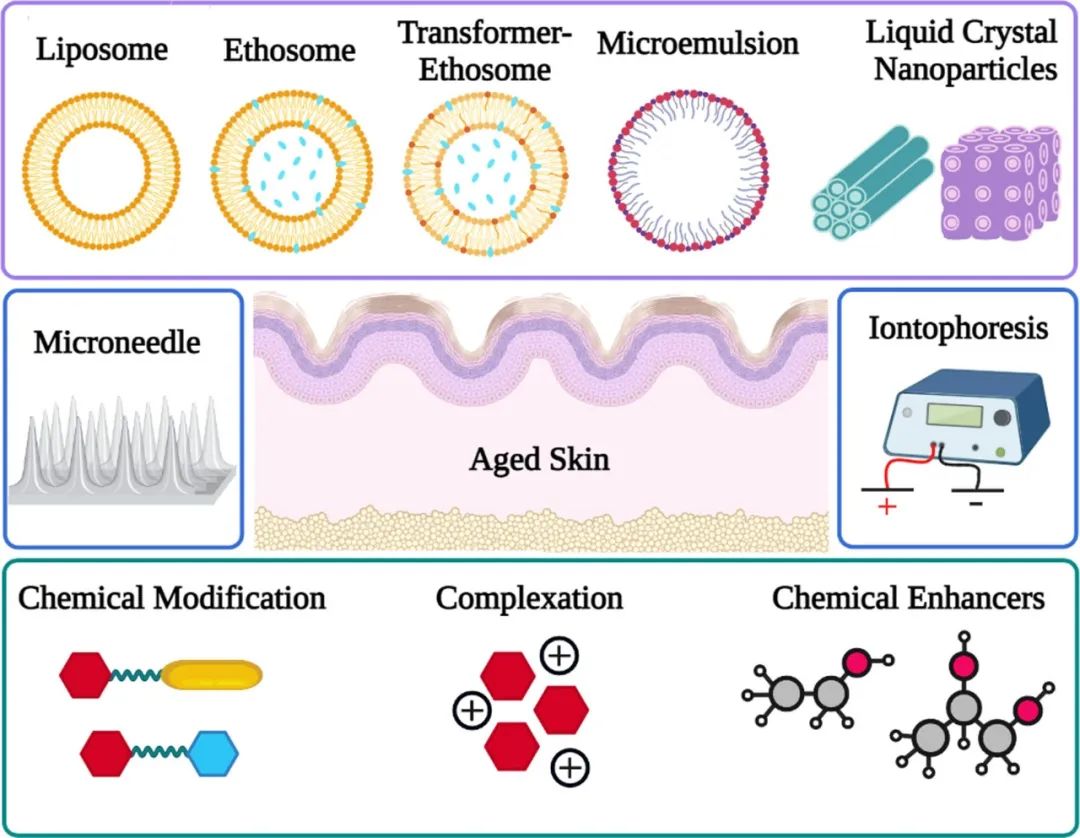
圖1. 迄今為止用于增強抗皺肽的皮膚滲透性的化學、物理和包封方法的示意圖(由BioRender.com創建)。
表1.親本抗皺肽的序列、MW和計算的log P值(clog P)
|
肽 |
序列 |
MW |
clogP值* |
|
肌肽 |
β-丙氨酸-組氨酸 |
226.2 |
−2.17 |
|
促黑素抑制素 |
脯氨酸-亮氨酸-甘氨酸 |
284.3 |
−1.07 |
|
GHK |
甘氨酸-組胺-賴氨酸 |
340.4 |
−2.24 |
|
GEKG |
甘氨酸-谷氨酸-賴氨酸-甘氨酸 |
389.4 |
−2.58 |
|
GQPR |
甘氨酸-谷氨酰胺-脯氨酸-精氨酸 |
456.5 |
−3.21 |
|
VGVAPG |
纈氨酸-甘氨酸-纈氨酸-丙氨酸-脯氨酸-甘氨酸 |
498.6 |
−0.38 |
|
PKEK |
脯氨酸-賴氨酸-谷氨酸-賴氨酸 |
500.6 |
−2.53 |
|
KTTKS |
賴氨酸-蘇氨酸-蘇氨酸-賴氨酸-絲氨酸 |
563.6 |
−3.54 |
|
Pal-KTTKS |
棕櫚酰-賴氨酸-蘇氨酸-蘇氨酸-賴氨酸-絲氨酸 |
802.0 |
3.72 |
|
乙酰六肽-3 |
乙酰-谷氨酸-谷氨酸 酸-蛋氨酸-谷氨酰胺-精氨酸-精氨酸-酰胺 |
889.0 |
−6.67 |
注:*本文中的所有clogP值均由ACD/ChemSketch免費軟件計算得出[68]。
02 用于抗皺肽的化學增強方法
通過使用化學方法優化肽的皮膚遞送,一種策略是通過化學修飾或絡合并產生新的化合物來改變肽的結構,另一策略是通過化學促滲劑改變角質層的結構。如下所述,化學修飾、絡合和化學促滲劑已被應用于增強抗皺肽的皮膚滲透。
2.1 化學修飾
通過共價鍵將化學基團結合到肽分子的天然結構中的過程被稱為化學修飾。化學修飾不僅可以影響肽的皮膚滲透性,還可以使肽分子對蛋白水解酶有一定的抗性[4]。疏水基團(例如,脂肪酸、萜類)、具有生物學特性的基團(例如,抗壞血酸、硫辛酸)和細胞穿膜肽(例如,聚賴氨酸、聚精氨酸)均是已用于美容肽化學修飾的基團[8,11–14]。在美容肽領域中使用化學修飾的三個主要目的是增強皮膚的滲透性、生物功效和代謝穩定性。例如,用硫辛酸(一種可以調節黑素生成酶表達的含硫脂肪酸)對KTTKS進行化學修飾,將KTTKS轉化為具有抗皺和抗黑色素生成特性的結合物[8]。另一例子是通過使用棕櫚酸進行化學修飾來增強KTTKS的代謝穩定性。Choi等人的研究表明,與KTTKS相比,Pal-KTTKS在表皮和真皮皮膚提取物以及皮膚勻漿中的穩定性更高[15]。下文中,我們嘗試將評述的范圍限制于如下問題事項,如皮膚滲透性。
疏水基團疏水基團如脂氨基酸和具有不同鏈長(C2至C18)的脂肪酸已被用于增加治療性多肽的滲透性[16–20]。脂氨基酸尚未應用于抗皺肽。除了脂肪酸之外,萜烯基團還用于抗皺肽的化學修飾[14]。疏水基團通過改變分配系數改變了肽向角質層細胞間脂質的趨向[4]。對于抗皺肽,可能會改變親本肽的功能性基團,以獲得更少的親水性肽。本節還將討論這一類型的結構性修飾。 五肽KTTKS(MW:563.6 Da,clog P:-3.54)被歸類為能夠促進細胞外基質生物合成的信號肽[7,21]。但是KTTKS的皮膚滲透性差是阻礙其抗皺性能的原因[15]。用疏水基團進行的化學修飾可能會影響這種高效肽的滲透性。KTTKS及其衍生物的化學結構如圖2所示。
2000年,Sederma公司在化妝品市場推出了名為Matrixyl®的Pal-KTTKS。這種分子量為802Da、clog P值為3.72的肽綴合物是通過使用棕櫚酸(16碳鏈)對KTTKS進行化學修飾而產生的。請注意,使用疏水基團的化學修飾同時增加了肽的疏水性和分子量。為了弄清疏水性、MW和疏水基團結構對肽的皮膚滲透性的影響,Mortazavi等人比較了棕櫚酸(脂肪酸,線型,MW:256.4 Da,clog P: 7.15)、香茅酸(萜烯,線型,MW:170.25,clog P: 3.35)和紫蘇酸(萜烯,環狀,MW:166.22,clog P: 2.97)對KTTKS滲透性的影響。為此,合成了KTTKS、Pal-KTTKS、香茅酸-KTTKS (Cit-KTTKS)和紫蘇酸-KTTKS(Per-KTTKS)(圖2)。Pal-KTTKS、Cit-KTTKS和Per-KTTKS的clogP值分別為3.72、-0.08和-0.88。使用人表皮以及n-十六烷膜模型作為完全親脂性屏障評估了肽的皮膚滲透。以多肽水溶液和10%乙醇溶液分別作為擴散池的供體相和受體相。
就膜模型而言,暴露24小時后,受體相未發現KTTKS和Per-KTTKS,而發現Pal-KTTKS和Cit-KTTKS,其預估滲透系數(kp)分別為17×10-4cm/h和2.9×10-4cm/h。結果還顯示,20%的Pal-KTTKS應用劑量被n-十六烷膜模型以某種方式留存。該膜根據肽分子的分配系數對其進行篩選。就人表皮而言,暴露48小時后,受體相中未發現可檢測含量的KTTKS和Pal-KTTKS。然而,與膜模型相比,Cit-KTTKS以更高的kp(7.3×10-4cm/h)透過人表皮,因此檢測到2.6%的Cit-KTTKS應用劑量。
根據研究者的說法,鑒于棕櫚酸是人角質層細胞間板層脂質基質的一種成分,并且由于棕櫚酸和KTTKS都具有線性結構,因此有可能將Pal-KTTKS截留在角質層的板層結構中。Cit-KTTKS比Pal-KTTKS更小,疏水性也更低。它有一個不飽和的短碳鏈是分支的,這種結構使截留的可能性較低[14]。該研究表明,在化學修飾過程中,除了疏水性之外,還必須考慮其他性質,如分子量和化學基團結構。為了增加抗皺肽的滲透性,萜烯基團可能是脂肪酸的良好替代物[14]。
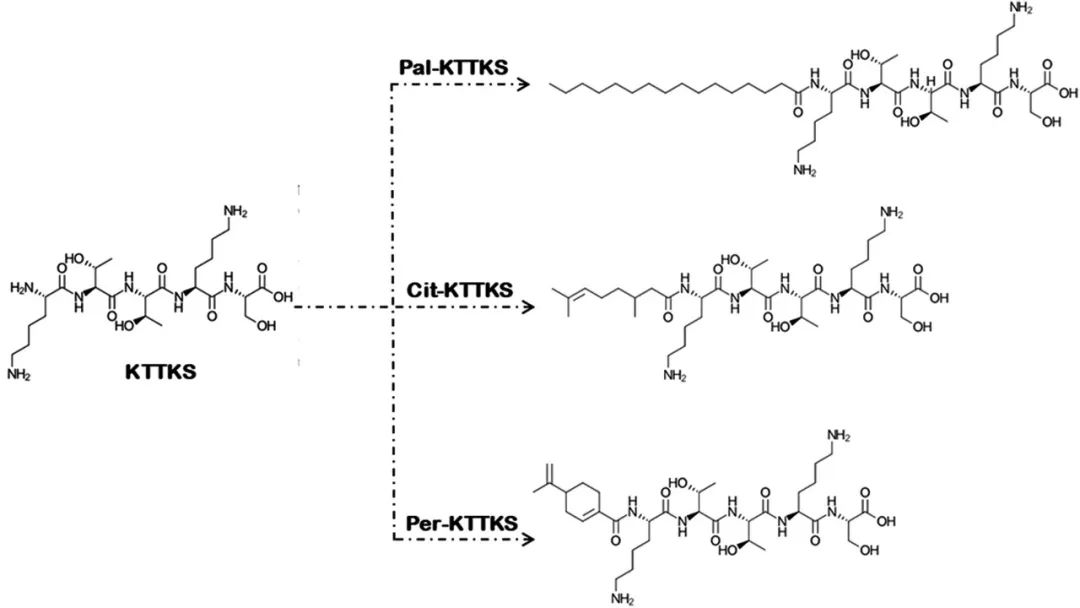
圖2.帶有疏水基團的KTTKS的化學修飾
為了減少兩性離子型肽Argireline(Arg0)的形成,對其氨基酸側鏈進行了化學修飾,并制備了三種類似物(Arg1、Arg2和Arg3)。Arg0由八個氨基酸殘基(Ac-Glu-Glu-Met-Gln-Arg-Arg-NH2)組成(圖3)。在所有類似物中,兩個谷氨酸側鏈的羧酸官能團均被酯化。對于Arg2,兩個精氨酸氨基酸的側鏈中的胍官能團被轉化為乙酰胺官能團。在Arg3中,這些胍官能團被修飾成雙氨基甲酸酯官能團。這些氨基甲酸酯官能團均以叔丁基為末端。這些結構性修飾的改變引起了MW和logP值的變化。Arg0、Arg1、Arg2和Arg3的分子量分別為889、917、1085和1317Da,其log P值分別為為-6.67、-4.67、-4.18和-1.75。使用人(尸)體皮膚和縱向Franz擴散池(供體相:含肽的丙二醇水溶液(0,30,50,70,100%),受體相:磷酸鹽緩沖液)進行24小時的皮膚滲透研究。Arg2(MW: 1085 Da和clog P:4.18)和Arg3(MW: 1317 Da和clog P: 1.75)顯著表現出皮膚滲透性增強。丙二醇是一種加入化妝品中的已知化學增強劑。在純丙二醇中,與純水相比,所有肽的皮膚滲透性都更高。對于Arg1、Arg2和Arg3,100%丙二醇溶液的滲透性最高。Arg0的濃度為70%[22]。值得注意的是,當丙二醇濃度為70%時,與其類似物相比,Arg0具有最高的皮膚滲透性,這表明了化學促滲劑的重要性。
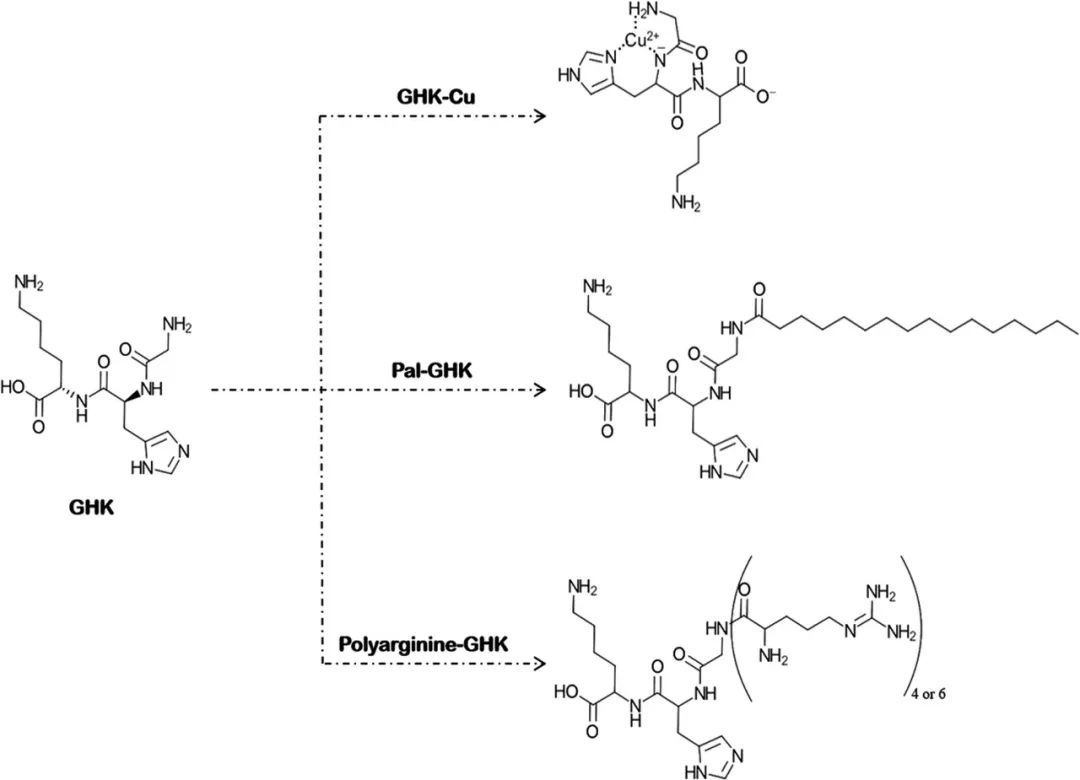
圖3.argireline的結構性修飾
一些用棕櫚酸進行化學修飾的肽已進入抗衰市場。除上述所提及的Matrixyl®之外,Pal-GHK和Pal-GQPR的組合產品也作為抗皺血清上市,品牌名稱為Matrixyl®3000。Pal-GQPR是2018年抗衰老產品中使用最廣泛的肽[3]。然而,尚沒有關于這種棕櫚酰肽滲透性的研究發表。對含有棕櫚酸和其他疏水基團的化學修飾肽的皮膚滲透性還需要更多的研究。
細胞穿膜肽細胞穿膜肽(CPP)由5-30個氨基酸組成。盡管根據物理性質,大多數CPPs是聚陽離子的,但還有其他兩類,是含兩親性和疏水性結構的。CPP能夠穿過膜并輸送各種大小的物質,從小分子(例如肽)到大分子(例如蛋白質)。CPPs利用內噬和非內噬通路內化到活細胞內[23–25]。然而,角質層含有死亡細胞,即角化細胞。與分子量相對較低且clogP值高于零的疏水基團相反,CPPs通常是具有親水性質的大分子。因此,抗皺肽與CPPs的結合不僅增加了肽的分子量,還降低了其進入角質層細胞間脂質基質的傾向。CPPs如何增加皮膚滲透性仍不清楚,但根據文獻,這似乎與皮膚蛋白相互作用、改變其二級結構以及誘導細胞間脂質流動性有關[26-28]。使用CPPs的化學修飾不僅會改變親本肽的結構,還會導致角質層屏障特性的劇烈變化。
事實上,親本肽擴散系數的修飾是CPPs的主要作用[4]。 三肽-1(GHK)是一種信號肽,可促進膠原蛋白、彈性蛋白、蛋白聚糖和糖胺聚糖的產生。由于GHK能夠釋放酶促過程所必需的微量元素銅,因此也被歸類為載體肽[2]。其分子量為340.4Da,clogP值為-2.24。Park等人評估了GHK(包括GHK、GHK-Cu和Pal-GHK)的皮膚滲透性。他們還研究了精氨酸低聚物(四和六-D-精氨酸、分別為R4,R6)與這些肽的共價連接是如何影響其皮膚滲透性的。GHK及其衍生物的化學結構見圖4。將合成表皮(Neoderm®-E)和Franz擴散池(供體相:肽水溶液,受體相:磷酸鹽緩沖液,試驗持續時間:24h)用于皮膚滲透研究。不同GHKs的皮膚滲透性順序如下(括號內為累積滲透肽的百分比):Pal-GHK(4.61%)>GHK-Cu(3.86%)> GHK(2.53%)。兩種精氨酸低聚物都增加了GHKs的皮膚滲透,但R4表現更好。在GHK與R4的綴合物中,Pal-GHK + R4的皮膚滲透性最好,GHK + R4的皮膚滲透性最差[Pal-GHK+R4(9.79%)>GHK-Cu+R4(8.68%)> GHK+R4(7.61%)][11]。由GHK+ R4顯示出比Pal-GHK更高的皮膚滲透性,因此可以得出結論,至少就GHK來說,CPP比疏水基團具有更好的性能。
盡管需要更多的比較研究,但鑒于CPPs和疏水基團的作用機制,CPPs在增加肽的皮膚滲透方面似乎更有效。當然,根據CPPs的皮膚滲透增強機制,當涉及到用CPPs對抗皺肽進行化學修飾的應用時,首先想到的問題之一是其潛在的副作用。不僅需要對使用CPPs制備的肽綴合物進行副作用研究,還需要對通過操縱親本肽的結構制備的所有肽進行副作用研究,以便將其用于臨床應用。
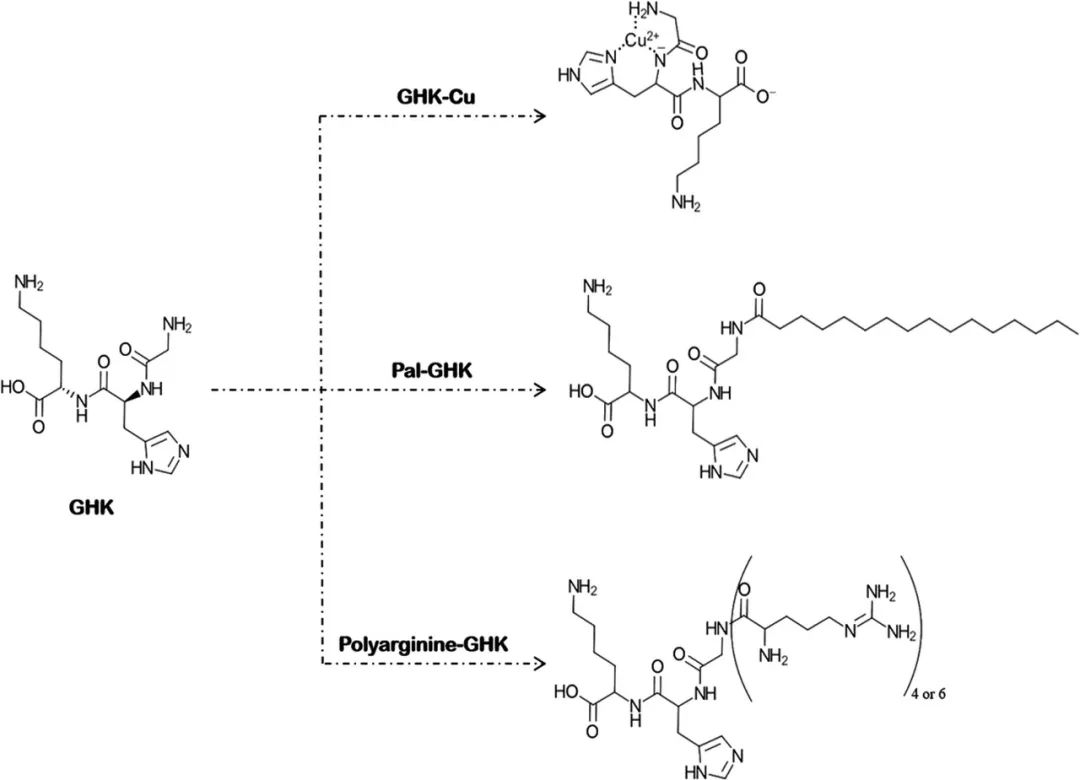
圖4.GHK的金屬絡合和化學修飾
2.2 化學促滲劑
化學促滲劑對角質層的屏障性能有暫時且可逆的降低作用。為此,這些分子通過廣泛的機制分配到角質層中并與其成分相互作用。根據化學結構,化學促滲劑可分為醇類、酰胺類、脂肪酸類、酯類、醚醇類、表面活性劑、亞砜類、精油類、萜類及其衍生物、吡咯烷類、噁唑烷類、磷脂類和酶類。化學促滲劑可以通過流化、脂質提取、極性改變和相分離來影響細胞間脂質結構域。它們還可以通過改變橋粒和蛋白質結構來改變角質層粘附的完整性。各機制已在別處進行了全面綜述[28–30]。化學促滲劑已成功增加了肽的皮膚滲透性。在皮膚滲透研究中,化學促滲劑以兩種方式應用;將化學增強劑與肽的物理混合物暴露于膜,或者最初用化學增強劑處理膜,然后將肽制劑施加于膜上。
肌肽是一種具有抗糖基化活性的抗氧化二肽,因此具有作為抗皺肽的潛力。肌肽(MW:226.23 Da,clog P值:-2.17)及其代謝產物N-乙酰腺苷(MW:268.27Da,clog P值:-2.56)也能減少人皮膚的UVB紅斑[31]。與肌肽相反,N-乙酰腺苷已被證明不是肌肽酶的底物。由于N-乙酰腺苷對蛋白酶降解的抗性更強,因此與肌肽相比,它可能是一種更好的抗皺劑。在使用Franz擴散池(供體相:含有肌肽或含和不含PG的N-乙酰腺苷的水分散凝膠(HDG),受體相:磷酸鹽緩沖鹽水)存在和缺乏作為化學增強劑的1,2-戊二醇(PG)的情況下,Goebel等人研究了肌肽和N-乙酰腺苷的皮膚滲透。PG作為一種兩親性二醇,增加了親水二肽的皮膚滲透性。已經提出了一些二醇增強效用的機理,包括α-角蛋白的溶劑化、非極性通路的修飾、極性分子分配系數的修飾等。
關于含有肌肽的制劑,無論制劑類型如何(含或不含PG),在受體相中并未檢測到肌肽,但在所有皮膚層中均發現了肌肽。角質層中肌肽的含量沒有顯著差異。100mins后,PG引起了表皮(約為無PG的HDG的6倍)和真皮(約為無PG的HDG的4倍)中積聚了較高含量的肌肽。對于含有N-乙酰腺苷酸的制劑,PG會致使更快和更高的皮膚滲透,因此在1000mins后,在所有皮膚層和受體腔中均檢測到57%的N-乙酰腺苷酸應用劑量。不含PG的制劑的N-乙酰腺苷酸量為38%。所有皮膚層中的N-乙酰腺苷含量均高于肌肽。與肌肽相比,有兩個可能的原因,即親水性降低以及對蛋白酶的耐藥性增加。研究人員介紹稱PG是一種有潛力的親水性肽增強劑[32]。Lim等人的研究(在化學修飾一節的前面已徹底的闡明)證明了丙二醇對Argirelin®滲透性的增強作用[22]。盡管沒有關于其他化學促滲劑對抗皺肽滲透性影響的研究發表,但對LHRH大小的治療性肽進行的研究表明,二醇、脂肪酸、萜類等也能夠增強肽的皮膚滲透[33–35]。
2.3 金屬絡合
金屬絡合是指由具有空電子軌道的金屬離子和一組具有供電子官能團的配體形成金屬絡合物的過程。金屬離子與配體之間形成的鍵是配位鍵或配價鍵(一種特殊的共價鍵)。一些肽(如GHK肽和肌肽)可作為配體,與金屬離子(如Cu2+和Mg2+)形成配合物。
肌肽是一種多齒配體,可以與Mg2+離子配位形成帶正電荷的復合物(圖2)。Dissette等人研究了復合劑鎂離子對肌肽穿透重建人表皮(呈現所有分化的細胞層)(作為人皮膚組織模型)滲透性的影響。使用菌類植物膠作為膠凝劑,他們制備了三種不同的凝膠:含有1.5%肌肽復合物的凝膠、含有1.5%游離肌肽但不含鎂鹽的凝膠和含有鎂鹽的凝膠。24小時和48小時的對比性滲透研究顯示,與游離肌肽相比,在使用肌肽復合物后的受體相中檢測到的肌肽濃度增加了1.5倍。對48小時后截留在皮膚模型中的肌肽的測量顯示,皮膚模型對于游離肌肽和肌肽復合物具有相同的趨向。肌肽復合物皮膚滲透性的增強歸因于其能更好地與長鏈糖胺聚糖和膜蛋白上存在的氮原子電子電荷相互作用。研究人員介紹了金屬螯合是一種提高肌肽皮膚滲透性的好方式[31]。 GHK-Cu是化妝品行業中著名的抗皺肽復合物。GHK是一種能夠攜帶Cu2+的信號肽,因此也可用作載體肽。事實上,這種金屬絡合物是有效抗皺肽和影響衰老過程的金屬的結合。成纖維細胞的線粒體產生含銅酶,參與結締組織的交聯。這就是為什么GHK-Cu能作為活性成分被納入抗衰產品[36]。Park等人進行的研究(詳見“細胞穿透肽”部分)顯示,GHK-Cu的皮膚滲透性高于GHK,這表明了金屬絡合對該肽滲透性的增強作用[11]。
03 用于抗皺肽的物理增強方法
已經應用了各種物理增強方法來降低皮膚對滲透物進入的阻力。物理技術遵循了兩種基本途徑;一是表皮的機械性破壞(例如,微晶磨皮、微針),二是皮膚中的空化或孔道形成(例如,超聲促滲和離子電滲作用)[37]。盡管物理方法具有所有優勢,但其局限性之一是需要特殊的設備將這些技術應用于臨床皮膚上。據我們所知,只有兩種物理技術,微針和離子電滲療法,被用于抗皺治療的研究。以下討論了這些技術。
3.1 微針
微針是皮下注射針和透皮貼劑的混合體,其中微米大小的針排列在小貼劑上。有不同穿透深度的微針,它們最重要的特征是其允許藥物/化妝品分子通過角質層,角質層是最具挑戰性的皮膚屏障[38]。角質層的平均厚度在10–30微米之間,藥物輸送針頭的長度在數百微米之間。這就是為什么微針不會引發痛感反而可以將藥劑有效地輸送到它們在皮膚中的靶點[39,40]。
Zhang等人使用豬耳皮膚和Franz擴散池(供體相:溶解在磷酸鹽緩沖鹽水中的肽,受體相:磷酸鹽緩沖鹽水)研究了微針預處理20秒對三種化妝品肽(包括GQPR(MW: 456.6 Da)、VGVAPG (MW: 498.6 Da)和乙酰基六肽-3(MW: 889 Da)以及一種治療性九肽(包括催產素(MW:1007.2 Da))的皮膚滲透性的影響。圖5中呈現了所提及的美容肽的結構。為了調查作為親水化合物的乙酰基六肽-3的運輸是如何被微針影響的,根據親水溶質和載體運輸之間的關系,在滲透研究中還測試了溶解在用D2O制造的磷酸鹽緩沖鹽水中的乙酰基六肽-3的供體相,并且研究了D2O通量以及乙酰基六肽-3的滲透清除率。固體微針的長度為150μm。使用包被有鈣黃綠素水凝膠的微針進行皮膚預處理后獲得的共聚焦激光掃描顯微鏡圖像證實,使用微針進行預處理可在皮膚中形成微導管。觀察到鈣黃綠素熒光在皮膚深度達80微米時的分布。在使用微針和不使用微針(被動擴散)的皮膚滲透研究中獲得的數據之間的比較表明,微針可以顯著增強肽的滲透性。暴露24小時后,催產素、乙酰基六肽-3、VGVAPG和GQPR的增強率分別約為58、38、36和32。結果還顯示,D2O通量與乙酰基六肽-3清除率之間存在適當的相關性,這表明了微針產生的對流對肽的皮膚滲透性的重要性及影響[41]。
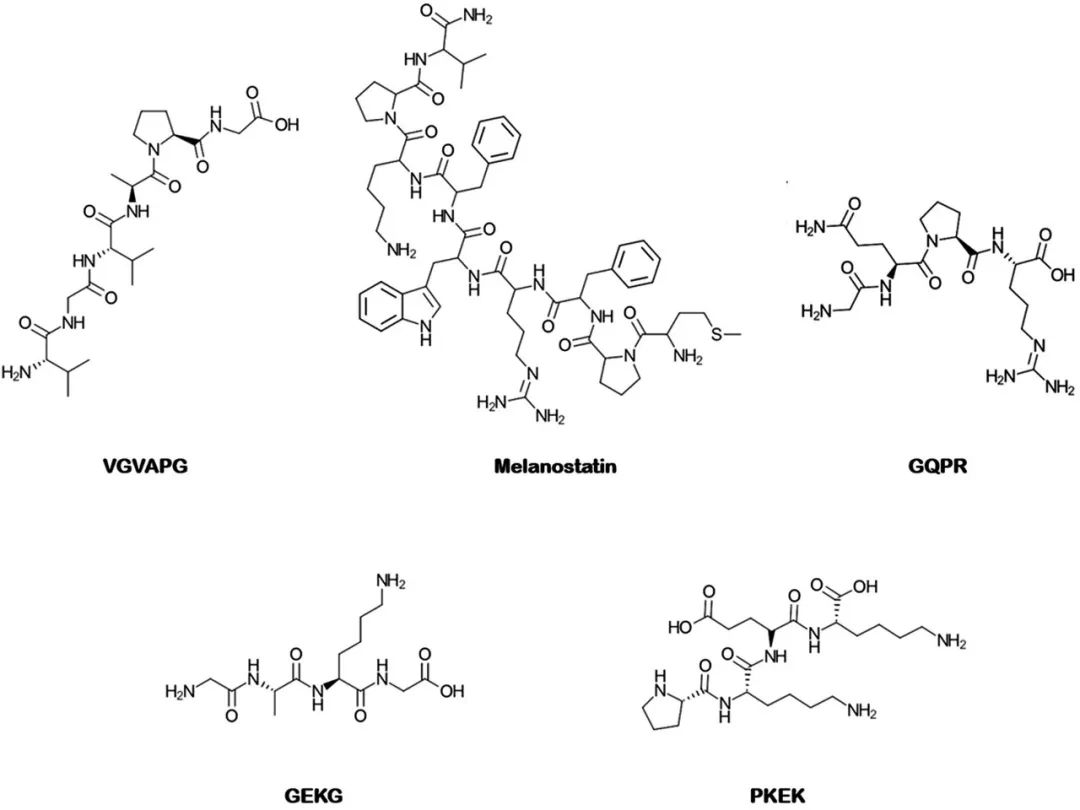
圖5. 經過物理方法和包封方法處理的抗皺肽的化學結構
Mohammed等人使用共焦顯微鏡評估了不同鏈長的熒光標記肽(黑素抑制素、GQPR和Pal-KTTKS)的被動擴散和微針促滲。圖2和5中顯示了提及的肽的化學結構。使用700μm的微針對人皮膚進行預處理顯著增加了黑素抑制素和GQPR的滲透,但這種技術對于本研究中最大的肽(即Pal-KTTKS)是無效的。研究人員討論稱單純地在皮膚中產生孔道并不意味著能增加所有類型的肽的滲透性,應針對每一種特定的肽來定制促滲技術[42]。
為了確定微針的幾何形狀和曲率對抗皺肽(乙酰基-六肽3)皮膚滲透的影響,Lim等人使用3DM可澆鑄樹脂通過3D打印制造了特制微針眼貼片。使用人(尸)體皮膚和Franz擴散池,研究了乙酰基六肽-3在完整皮膚、用特制微針眼貼片處理的皮膚和用市售扁平微針貼片處理的皮膚上24小時后的皮膚滲透。供體相為10%w/v濃度的乙酰基六肽-3溶液,受體相為磷酸鹽緩沖鹽水。在皮膚滲透研究中還使用了一種含有乙酰基六肽-3的市售透皮貼劑。基于這些結果,使用特制微針貼片處理的皮膚中肽的累積滲透量分別是完整皮膚和使用柔性微針貼片處理的皮膚的90倍和45倍。對于含有乙酰基六肽-3的市售貼劑,在受體相中未發現可檢測含量的肽。除了特制微針眼用貼片與含有乙酰基六肽-3的市售貼片之間的比較外,所有治療組,在皮膚中捕獲的肽總量在統計學上沒有差異。與扁平微針貼片相比,特制微針貼片預處理的皮膚滲透性更好,這強調了在使用過程中使微針貼片貼合皮膚表面的重要性[43]。
上述研究是關于固體微針預處理對抗皺肽皮膚滲透性的影響。其他類型的微針,如:包被微針、可溶微針和中空微針[44]。這些類型的微針尚未考慮在抗皺肽領域使用。
3.2 離子電滲療法
離子電滲療法是一種物理技術,其中使用生理學上可接受的電流來傳輸分子穿過皮膚[45]。電斥力(驅動帶電分子穿過皮膚)和電滲(在膜中產生攜帶帶電和不帶電分子的大量液流)的機制導致離子電滲過程對帶電和不帶電分子都有效用[46,47]。這種物理滲透增強的方法可能有助于肽的皮膚遞送。關于藥物和模型肽的離子電滲遞送已有許多已發表的研究[33,34,48,49],但談及抗皺肽時,文獻的匱乏是顯而易見的。
各種參數會影響離子電滲療法的效果。Krishnan等人研究了與制劑相關的參數(如濃度、pH和競爭離子的存在)、與離子電滲療法過程相關的參數(如施加電流的方向:陽極與陰極)以及與滲透劑相關的參數(如分子大小和電荷)對肽的皮膚滲透性的影響[47]。滲透物按分子量增加的順序有小肽樣藥物(5-氨基乙酰丙酸)、模型二肽(丙氨酸-色氨酸)、治療性四肽(丙氨酸-丙氨酸-脯氨酸-纈氨酸;AAPV)、美容肽(乙酰基六肽-3)和治療性十肽(醋酸曲普瑞林)。采用人表皮膜、Ag/AgCl電極的0.4 mA恒定離子電滲電流和帶有電解質溶液(20 mM HEPES + 137 mMNaCl)受體相的并排擴散池進行滲透研究。與被動滲透相比,離子電滲療法致使所有肽的皮膚滲透增加了30倍。對于低分子量帶電荷的肽,電斥力是相當大的。對于高分子量帶電肽,電滲是一個重要的決定參數。根據文獻,與較小的肽相比,大肽所攜帶的總電流比例非常小[48]。在較低的pH值下,滲透率降低,這可能是由于電滲作用降低所致。供體腔中背景電解質的存在降低了全部肽的離子電滲遞送,這可能是由于離子強度的增加,從而增加了電荷載體之間的競爭所導致。電滲的減少被認為是另一個可能的原因。供體相中肽濃度的增加致使肽離子電滲通量增加,離子電滲滲透系數降低,因為通量增加并不等同于濃度增加。離子電滲療法的電荷飽和可能是該事件的一個可能的原因。電流方向對僅針對AAPV和乙酰基六肽-3(兩種肽pH在 7.4下)進行的離子電滲遞送影響的研究表明,盡管AAPV具有負電荷,但對其與電流方向無影響,這表明對于該肽的離子電滲滲透而言電斥力和電滲這兩種機制很重要。在pH 7.4時,乙酰基六肽-3的凈電荷為零,因此電滲是其離子電滲療法滲透的主要機理。因此,陽極電流下乙酰基六肽-3的離子電滲療法的滲透系數約是陰極電流下的14倍。在本研究中已經很好地彰顯了將各種參數調節到最佳水平對于獲得最佳離子電滲療法的肽遞送的重要性[47]。
04 抗皺肽在脂質納米載體中的包封
近年來,人們對納米技術的興趣越來越大,這種創新技術的痕跡可以在許多領域看到,包括化妝品領域。利用基于納米的遞送系統來有效地遞送化妝品成分已經引起了人們的廣泛關注,抗皺肽也不例外。眾多納米載體已被用于化妝品研究,但其中許多載體尚未被研究用于增加抗皺肽的皮膚滲透。以下是對研究嘗試的綜述,其中調查了將抗皺肽包封到納米載體中對肽的皮膚滲透性的影響。以下就抗皺肽包封于納米載體對其皮膚滲透性的影響進行綜述。
4.1 磷脂囊泡納米載體
脂質體是化妝品行業最早獲得成功的體系之一。1986年,Christian Dior推出了第一款以CaptureTM品牌命名的脂質體抗衰老霜[50]。脂質體是由至少一個磷脂雙層包圍的親水核組成,可用于裝載親水物質和疏水物質[51]。傳遞體和醇質體是其他類型的基于磷脂的囊泡體系,它們比脂質體更具柔韌性和彈性。這些彈性囊泡呈現出比脂質體更好的皮膚滲透性。傳遞體的主要特征是在其結構中存在引起變形性的邊緣活化劑(例如單鏈表面活性劑)。醇質體的結構中含有乙醇分子。乙醇是一種化學促滲劑,可以流化醇質體結構中的脂質以及角質層中的脂質[52]。本章節并非關注磷脂囊泡體系的特征和組成。如需了解詳情,請閱讀參考文獻[53]。磷脂囊泡體系如何增加裝載物質的皮膚滲透性仍有爭議。這些假設包括完整囊泡通過角質層的細胞間脂質基質的皮膚滲透、組分的滲透增強作用以及完整囊泡通過經附件途徑的皮膚滲透[54]。對于常規脂質體,通過附件途徑的可能性更大,如毛囊,而對于柔性脂質體,通過附件途徑和細胞間脂質基質的可能性更大,如傳遞體和醇質體。
為了改善Pal-KTTKS的皮膚滲透性,Kim等人利用大豆磷脂酰膽堿、乙醇和不同脂肪酸(C10、C12、C14、C16、C18)設計了名為transformer-ethosomes的新型載體。然后將這些載體與脂質體和醇質體在增加Pal-KTTKS滲透性的靈活性和能力方面進行比較。與其他transformer-ethosomes以及脂質體和醇質體相比,磷脂雙層中含有癸酸(C10)和肉豆蔻酸(C14)的transformer-ethosomes呈現出最小的轉化溫度和最大的靈活性。使用擴散池進行的人工膜皮膚滲透研究表明,當使用含Pal-KTTKS的15%乙醇溶液、脂質體或醇質體作為供體相時,24小時后在受體相中未發現可檢測含量的肽。然而,所有類型的transformer-ethosomes均致使在受體相中可發現Pal-KTTKS。結果表明,鏈較短的飽和脂肪酸對脂雙層的柔韌性和Pal-KTTKS的通透性均有較大影響。在transformer-ethosomes中,最具滲透性的是那些含有癸酸或肉豆蔻酸的物質。癸酸和肉豆蔻酸改變了磷脂雙層的流動性,從而提高了transformer-ethosomes擠過角質形成細胞間孔隙的能力。此外,乙醇和脂肪酸都可以作為化學皮膚促滲劑。使用具有熒光標記物(若丹明-6G)的共聚焦激光掃描顯微鏡的皮膚滲透研究表明,在經4h暴露后,在15%乙醇溶液的情況下僅在角質層中發現熒光探針,而在脂質體和醇質體中,標記物可以到達表皮基底層。在transformer-ethosomes中觀察到了熒光探針向真皮最下層的滲透。這種可變形的磷脂囊泡似乎一種有前景的載體,其可將信號肽如Pal- KTTKS遞送至其在真皮中的作用位點[55]。
4.2 液晶納米粒子
液晶是研究人員已經考慮用于各種美容目的的另一遞送系統[56,57]。液晶或中間相是介于液態和固態之間的中間狀態。因此,有些液晶的性質類似于液體(如流動性),有些(如結構順序)類似于固體。中間相有兩大類,熱致性和溶致性。熱致性中間相是因溫度變化形成的,而溶致性中間相是在一定溫度下,向一定量的兩親性分子中加入溶劑形成的[58,59]。溶致性中間相作為藥物遞送系統備受關注。溶致性中間相有三個主要類別,即層狀、立方形和六邊形中間相。親水性和親脂性物質均可并入溶致性中間相。液晶可以在納米尺度上制備;立方小體和六胞體是兩個常見的例子[60]。為獲得合適的Pal- KTTKS皮膚遞送系統,Selvaraj等人制備了粒徑小于300 nm、包封率大于99%的液晶納米粒子。液晶納米粒子由磷脂酰膽堿、單油酸甘油酯和不同濃度的部分水解人參皂苷制備。將全層豬皮和Franz擴散池(供體相:含Pal-KTTKS和含和不含脂肪酶的磷酸鹽緩沖鹽水(50:50 v/v)的液晶納米顆粒,受體相:磷酸鹽緩沖鹽水)用于皮膚滲透和滯留研究。研究人員利用供體相中的脂肪酶研究了液晶納米粒子是否能穩定Pal-KTTKS對酶的作用。液晶納米粒子增加了Pal-KTTKS的皮膚滲透性和滯留性。在缺乏和存在脂肪酶的情況下,載有Pal-KTTKS的液晶納米粒子的穩態通量分別是丙二醇中溶解的Pal-KTTKS的4.6倍和6倍。結果還顯示,隨著部分水解的人參皂苷的濃度增加,Pal-KTTKS的皮膚滲透性和滯留量增加。研究者得出,該化合物可用作皮膚滲透促進劑[61]。
盡管液晶已經成功地用于遞送化妝品成分,例如視黃醇、白藜蘆醇、抗壞血酸[56,62,63],但它們作為肽遞送系統的應用還沒有像其它基于脂質的遞送系統那樣普遍。因此,對于含抗皺肽的液晶十分需要進一步的研究。
4.3 微乳液
微乳液是一種穩定的膠體體系,由三至四種主要成分組成;水、油、表面活性劑和助表面活性劑。雖然微乳一詞中使用了micro的前綴,但微乳的液滴尺寸< 100 nm。有望將親水性和疏水性物質混合到微乳液中。微乳液具有增強皮膚滲透的特性,并已被廣泛用作向皮膚遞送不同物質(藥物或化妝品)的載體[64]。表面積/體積比大、單個組分的作用、皮膚水合作用的增高和高負載能力均被認為是微乳液增加皮膚滲透性的機理[65]。
PKEK是一種能夠抑制色素沉著過程的四肽(化學結構見圖4 )。為此,該肽必須要到達表皮細胞的基底層。由于其MW為500.6 Da,clogP值為–2.53,并且存在多種可電離基團;對于PKEK來說,實現此目標具有挑戰性。利用人皮膚和Franz擴散池,比較了W/O微乳液與標準乳膏的PKEK滲透性。受體相為磷酸鹽緩沖液。在30mins、100mins、300 mins后測定皮膚不同深度中的肽的濃度。使用含有PKEK的兩種制劑后,觀察到皮膚中肽的濃度梯度顯著。隨著時間的推移,皮膚中的肽濃度增加。微乳液和標準乳膏30 mins后在皮膚上殘留的肽的百分比分別為48%和42%。100 mins和300 mins后,微乳液的殘留肽百分比明顯高于標準乳膏;這表明當肽被摻入微乳液中時肽具有更高的皮膚滲透性。就角質層而言,盡管30mins后標準乳膏和微乳液的滲透肽百分比相似,但與微乳液相比,在100和300分鐘后在角質層中檢測到的標準乳膏中PKEK的百分比顯著更高。
相反,與標準乳膏相比,在皮膚上涂抹微乳液后,在受體相中檢測到的PKEK百分比標準乳膏更高。一般來說,當使用標準乳膏時,肽主要留存在角質層中,而微乳液則允許更高含量的PKEK到達更深的皮膚層[66]。 GEKG如果達到真皮靶點,可減少皺紋并改善皮膚表觀。其化學結構如圖4所示。在另一項旨在了解微乳液對肽滲透性影響的嘗試中,前一組比較了來自標準乳膏、W/O納米載體系統和含有增強劑(辛酸甘油酯/辛酸酯)的GEKG (MW: 389.4,clog P:2.58)的皮膚滲透性。滲透研究中使用了Franz擴散池和人皮膚。與先前的研究一樣,結果顯示,使用標準乳膏后,皮膚表面和角質層中仍殘留大量GEKG。化學增強劑略微增加了GEKG對角質層和活性表皮的滲透。微乳液是最佳的制劑,可使高百分比的肽通過皮膚[67]。
根據這些研究,盡管微乳液呈現出遞送美容肽的前景,但對這一領域的進一步研究仍非常必要。表2. 呈現了所提及的由不同增強方法增加抗皺肽皮膚滲透性的全部研究的總結。
| 肽 | 增強方法 | 膜類型 | 結論 | 文 獻 |
| 肌肽 | 絡合(肌肽-鎂) | 表皮模型 | 應用肌肽復合物后培養基中肌肽濃度提高1.5倍。 | 31 |
| 化學促滲劑(戊二醇) | 人體皮膚 | 戊二醇導致更大量的肌肽在表皮和真皮中積累。 | 32 | |
| GHK | 化學修飾(Pal-GHK,精氨酸低聚物-GHK)和絡合(GHK-銅) | 人工表皮 | 就滲透率而言:Pal-GHK + R4 > GHK-Cu + R4 > GHK + R4 | 11 |
| PKEK | 微乳液 | 人體皮膚 | 微乳液允許更高含量的PKEK到達更深的皮膚層。 | 66 |
| GEKG | 化學促滲劑(辛酸甘油酯/辛酸酯)和微乳液 | 人體皮膚 | 化學增強劑略微增加了GEKG的滲透率。微乳液致使高百分比的肽通過皮膚 | 67 |
| 化學修飾(Cit-KTTKS和Per-KTTKS) | 人體表皮 | 只有Cit-KTTKS滲透到人表皮中,kp為7.3×10-4cm/h。 | 14 | |
| Pal-KTTKS | 液晶納米粒子 | 豬皮膚 | 液晶納米粒子增加了兩種皮膚的滲透性和滯留性 | 61 |
| 脂質體 | 人工皮膚 | 與Transformer-ethosomes相反,就脂質體和醇質體在受體相中無可檢測到的量。 | 55 | |
| 醇質體 | ||||
| Transformer-ethosomes | ||||
| 微針 | 人體皮膚 | 對Pal-KTTKS該技術無效。 |
42 |
|
| GQPR | 微針 | 人體皮膚 | 增強率=32 | 41 |
| 促黑素抑制素 | 微針 | 人體皮膚 | 增強了皮膚滲透性 | 42 |
| 乙酰基六肽-3 | 結構修飾和化學滲透增強劑(丙二醇) | 人(尸)體皮膚 | 在所有衍生物中,100%丙二醇溶液的滲透率最高。親體肽的此濃度為70%。 | 22 |
| 微針 | 人(尸)體皮膚 | 增強率=38 | 41 | |
| 離子電滲療法 | 人體皮膚 | 增強率=6.8 | 47 | |
| VGVAPG | 微針 | 人(尸)體皮膚 | 增強率=36 | 41 |
Note:除 [31] 外,所有滲透研究均使用擴散池進行。
05 結論
抗皺肽作為活性成分在護膚品中的應用是化妝品行業當前備受關注的領域。許多已發表的研究證實了此類肽的抗皺性能,但其皮膚滲透性尚未得到證實。大多數抗皺肽不具有用于皮膚遞送的理想滲透的特征,并且還必須使用增強方法來增加它們的滲透性。盡管有眾所周知的化學、物理和包封方法來增強聚合物和大分子的皮膚滲透,但對于抗皺肽,目前為止已經采用了其中的一些方法(但并非全部)。化學修飾、絡合、化學促滲劑、離子電滲療法、微針和納米載體包封已呈現出對增加抗皺肽的皮膚滲透性的前景。當然,還需要進一步的研究來確定每種增強方法的優缺點。應始終注意,抗皺產品由化妝品消費者使用,因此增加肽皮膚滲透的方法不可有損產品的吸引力。盡管我們希望抗皺肽具有更高的皮膚滲透性,但也不能忽視應用增強方法可能會引起的皮膚副作用。關于抗皺肽的皮膚滲透增強仍有許多問題沒有得到解答,如電穿孔、超聲、多極射頻以及大多數化學增強劑對這些難溶性分子的滲透率的影響。因此,需要進一步研究找出抗皺肽的最佳滲透增強策略。
原文鏈接: 點擊查看
相關推薦:
