人類使用化妝品的歷史源遠流長,原始社會就已經出現了簡單天然的護膚方式。原始部落在祭祀活動中會把動物油脂涂抹在皮膚上,使自己的膚色看起來健康而有光澤,從古至今,人們追逐美麗的腳步從未停止過,化妝品現如今已成為人們生活中最為常見的消費品之一。2019年全球化妝品市場規模達到4996億美元,其中我國約占據全球化妝品市場份額的14%,僅次于美國,排名第二。2019年,我國化妝品行業市場規模高達4777億元,同比增長13.84%,增速高于全球。但從人均化妝品消費水平來看,中國人均消費仍落后于發達國家,隨著經濟發展、人民消費水平的持續提升以及消費意識的轉變,化妝品行業發展空間更為廣闊,化妝品生產在經濟發展中屬于朝陽產業。
與藥品不同,化妝品主要發揮美化、點綴生活的作用,因此安全性是其最基本的特性,然后才是產品的功效。企業研發化妝品應將產品安全性置于首要位置。我國現行法規將化妝品分為特殊化妝品和普通化妝品,其中特殊化妝品包括染發、燙發、祛斑美白、防曬和防脫發化妝品以及宣稱新功效的化妝品。相對于普通化妝品(例如宣稱具有清潔、滋潤、保濕等功效的化妝品),特殊化妝品因具有較高的風險,依照我國按風險程度實行分類管理的原則,對其實行注冊管理。我國化妝品安全評價部門在產品安全性審查過程中發揮著重要的技術支撐作用,化妝品安全技術評價是我國化妝品監管體系的重要環節,其中特殊化妝品的安全評價又是評價體系的重要組成部分。
目前尚無對特殊化妝品安全評價中所發現問題進行系統分析和梳理的相關報道。作者結合開展化妝品安全技術評價的工作經歷,歸納并整理了影響產品安全性的若干問題,并結合相關法規、部門規章和規范性文件,對具體案例開展分析,為化妝品產品研發、相關監管部門、技術機構評估產品安全性提供借鑒。
1、化妝品安全技術評價相關法規、部門規章和規范性文件
1.1 化妝品監管法規
《化妝品衛生監督條例》的效力至2020年12月31日止,2019年國務院曾對其進行了局部修正。自2021年1月1日起施行的化妝品監管法規為《化妝品監督管理條例》(下稱“《條例》”),2020年6月16日由李克強總理簽署并于2020年6月29日由國務院正式發布。
《條例》中規定,化妝品是指以涂擦、噴灑或者其他類似方法,施用于皮膚、毛發、指甲、口唇等人體表面,以清潔、保護、美化、修飾為目的的日用化學工業產品。該定義從使用方法、使用部位、使用目的和產品屬性四個方面對化妝品進行了界定。
1.2 化妝品監管部門規章
化妝品安全技術評價的參考文件依據除監管法規外,還包括了一系列部門規章,如和《化妝品衛生監督條例》配套的《化妝品衛生監督條例實施細則》、《化妝品標識管理規定》等。隨著新《條例》的實施,配套出臺的部門規章有《化妝品注冊備案管理辦法》、《化妝品生產經營監督管理辦法》以及《牙膏監督管理辦法》。目前《化妝品注冊備案管理辦法》和《化妝品生產經營監督管理辦法》已經由國家市場監督管理總局正式發布,前者自2021年5月1日起施行,后者自2022年1月1日起施行。《牙膏監督管理辦法》已公開征求了意見。
1.3 化妝品監管規范性文件
在《化妝品衛生監督條例》框架下,安全技術評價參考的規范性文件有2009年發布的《化妝品行政許可申報受理規定》,此為申報資料準備和受理工作的重要依據;2010年發布的《化妝品技術審評要點》和《化妝品技術審評指南》、《化妝品命名規定》及《化妝品命名指南》、《國際化妝品原料標準中文名稱目錄》和《化妝品中可能存在的安全性風險物質風險評估指南》等系列文件,為安全技術評價工作的重要依據。2015年發布了《化妝品安全技術規范》(下稱“《規范》”),2021年發布了《已使用化妝品原料目錄》,前者是進行安全性評價的重要技術參考,后者是判定配方中是否使用了化妝品新原料的重要依據;2019年發布了《化妝品注冊和備案檢驗工作規范》,是設定化妝品注冊檢驗和備案檢驗項目、評價檢驗報告規范性的重要參考。
此外國家局發布的通知、通告、公告及其解讀,以及國家局發布的《化妝品監督管理常見問題解答》,也是安全技術評價所依據的參考。國家標準(如GB5296.3—2008消費品使用說明化妝品通用標簽)、推薦性國家標準和行業標準,也作為參考文件使用。
配合新《條例》的實施,一系列配套文件已經出臺,如《化妝品標簽管理辦法》、《化妝品注冊備案資料管理規定》、《化妝品新原料注冊備案資料管理規定》、《化妝品安全評估技術導則》等,這些文件會替代原《化妝品衛生監督條例》框架下的部分文件。
2、特殊化妝品技術評價涉及安全性的問題及分析
從特殊化妝品安全技術評價工作實際發現,涉及產品安全性的問題主要包括以下幾種情況:產品不符合化妝品定義范疇、產品中使用了未經我國化妝品監管部門批準的新原料、產品配方不符合《化妝品安全技術規范》要求以及申報資料前后不一致等。
2.1 產品不符合化妝品定義范疇
《化妝品衛生監督條例》第十條規定特殊用途化妝品是指:用于育發、染發、燙發、脫毛、美乳、健美、除臭、祛斑、防曬的化妝品。其中脫毛類化妝品在配套的《化妝品衛生監督條例實施細則》第五十六條規定:脫毛化妝品為具有減少、消除體毛作用的化妝品。某進口蜜蠟申報脫毛類化妝品,原包裝有“臉部蜜蠟”字樣,宣稱“擺脫臉部細小毛發帶來的煩惱”,并在其中文標簽的使用方法中宣稱用于面部脫毛。這和脫毛類化妝品定義不符合,超出了脫毛類化妝品范疇。因為按照《化妝品衛生監督條例》框架下的檢驗要求,脫毛類產品需要開展汞、鉛、砷、鎘等理化檢驗項目,毒理學試驗僅需開展皮膚變態反應試驗,物理脫毛類產品需要進行微生物檢驗,上述檢測無法保證產品應用于“眉毛周圍、唇周下巴、面頰”等部位的安全性。需要說明的是,新《條例》及其配套文件《化妝品分類規則和分類目錄》中,將脫毛類化妝品列為普通化妝品;在《化妝品分類規則和分類目錄》功效宣稱分類目錄中,“脫毛”類功效宣稱的釋義和說明中,將“脫毛”解釋為“用于減少或除去體毛”,在“化妝品作用部位分類目錄”中,作用部位體毛“不包括頭面部毛發”。因此在新《條例》框架下,脫體毛類產品實行備案制,脫面部毛發產品按照宣稱新功效的特殊化妝品來監管。
某進口面膜產品,在原包裝中宣稱“對準面部穴位貼敷,輕輕按壓,可改善循環,改善浮腫”。使用方法為“穴位貼敷”,與《條例》中“涂擦、噴灑或者其他類似方法”的使用方法不符,使用目的為“改善循環”、“改善浮腫”,與“清潔、保護、美化、修飾”的使用目的不符,超出了化妝品的定義,無法判定產品安全性。
2.2 產品中使用了未經我國化妝品監管部門批準的新原料
原國家食品藥品監督管理總局在2015年發布了《已使用化妝品原料名稱目錄》,此目錄是對在我國境內生產、銷售的化妝品所使用原料的客觀收錄,共收錄了8783種化妝品原料。2021年國家藥品監督管理局發布了《已使用化妝品原料目錄》,收錄了8900余種原料,自2021年5月1日起施行。未收錄于該目錄中的原料,按照新原料管理。需要注意的是,化妝品生產企業在選用目錄中所列原料時,應當符合國家有關法規、標準、規范的相關要求,并對原料進行安全性風險評估。
《化妝品監督管理條例》規定,在我國境內首次使用于化妝品的天然或者人工原料為化妝品新原料,化妝品新原料經國務院藥品監督管理部門注冊或備案后方可使用。我國化妝品新原料的注冊或備案需要經過嚴格的安全評價,提供能夠證明原料安全性的毒理學評價資料和風險評估資料,有一系列申報材料支撐,并且要經過嚴格的注冊或備案程序。在《化妝品新原料注冊備案資料管理規定》中對新原料的注冊備案工作有了明確的要求。產品配方中使用未經監管部門注冊或備案的新原料顯然是不允許的。
在安全技術評價工作中發現,注冊人將收錄在《已使用化妝品原料目錄》中原料的發酵產物等同于該原料,導致在配方中使用新原料的問題發生。發酵技術是利用微生物細胞或細胞內的酶催化反應體系對原料中的成分進行結構修飾和改造,并運用技術手段控制過程,從而實現大規模生產發酵產品的技術。原料經過微生物發酵后,結構會發生變化,且往往會形成與化學合成法所不同的特殊結構,因此原料經過發酵的產物不能等同于發酵前的原料。例如,申報配方中填寫的原料為“冬蟲夏草菌絲體經發酵、過濾、烘干、碾磨而得到的淺棕色粉末”。冬蟲夏草在中國藥典一部中收載,為麥角菌科真菌冬蟲夏草菌Cordycepssinensis(BerK.)Sacc.寄生在蝙蝠蛾科昆蟲幼蟲上的子座和幼蟲尸體的干燥復合體,為傳統中藥。冬蟲夏草(CORDYCEPSSINENSIS)提取物收錄在《已使用化妝品原料目錄》中,但配方中實際使用的是冬蟲夏草經發酵工藝后的加工品,其發酵產物未收錄于《已使用化妝品原料目錄》中,屬于未經化妝品監督管理部門批準的新原料。
安全技術評價工作中還發現,對配方中寡肽類原料的使用,注冊人也存在誤用新原料的情況。例如寡肽-1,容易和植物合成多肽、重組肽以及人寡肽-1(即人表皮生長因子,hEGF)發生混淆。在歐盟委員會官方化妝品成分數據庫中,寡肽-1為甘氨酸、組氨酸和賴氨酸的寡聚物(Glycine,oligomerwithhistidineandlysine);《國際化妝品原料字典》將寡肽-1描述為由甘氨酸、組氨酸和賴氨酸組成的合成肽。在評價工作中發現,“寡肽-1”原料的質量規格顯示,配方中使用的“寡肽-1”為59個氨基酸組成的植物合成多肽,或者來源于大腸桿菌的由18種氨基酸組成的重組肽,這些不符合寡肽-1的氨基酸組成。人寡肽-1是一種廣泛存在于人類皮膚細胞的小分子蛋白質,由53個氨基酸組成,可以促進多種細胞生長,包括促進人干細胞生長,如可促進受損表皮的修復和再生,用于皮膚科術后促進傷口愈合等。國家藥品監督管理局《化妝品監督管理常見問題解答(一)》中提到,寡肽-1一般作為皮膚調理劑使用。人寡肽-1一般在醫學領域使用較多,由于分子量較大,在正常皮膚屏障條件下較難被吸收,一旦皮膚屏障功能不全,可能會引發其他潛在安全性問題。基于有效性及安全性方面的考慮,人寡肽-1不得作為化妝品原料使用。因此顯示使用寡肽-1的化妝品配方,應根據原料質量規格判斷實際使用的原料。
2.3 產品配方不符合《化妝品安全技術規范》要求
我國《化妝品安全技術規范》充分借鑒了美國、歐盟等國家和地區化妝品安全性評價的管理法規,并綜合了我國化妝品風險評估及化妝品監管的重要經驗,重點關注對風險物質的管理。《規范》要求化妝品配方不得使用《規范》表中所列的禁用組分,若技術上無法避免禁用物質作為雜質帶入化妝品時,國家有限量規定的應符合其規定;未規定限量的,應進行安全性風險評估,確保在正常、合理及可預見的適用條件下不得對人體健康產生危害。
當使用限用組分表中所列物質時,《規范》要求化妝品配方應符合限用組分表中適用及(或)使用范圍(如產品類型、作用等)、使用時的最大允許濃度以及其他限制和要求。
另外,《規范》的準用組分表列出了配方中準用的防腐劑、防曬劑、著色劑和染發劑,這四類原料相對風險較高,因此監管部門制定了準用清單,并對原料的純度、規格,使用范圍,使用的最大允許濃度等作出了明確規定。在產品安全技術評價中發現配方中限用組分、準用組分的使用不符合《規范》要求的情況。
2.3.1 配方中原料有形成亞硝胺風險
某產品配方中同時使用了“2-溴-2-硝基丙烷1,3-二醇”和“三乙醇胺”。2-溴-2-硝基丙烷-1,3-二醇收錄于《規范》準用防腐劑列表中,使用范圍和限制條件項下注明“避免形成亞硝胺”;三乙醇胺屬于《規范》限用組分表中“三鏈烷胺、三鏈烷醇胺及它們的鹽類”項下的三鏈烷醇胺,要求不和亞硝基化體系一起使用,避免形成亞硝胺,最低純度99%,原料中仲鏈烷胺最大含量0.5%,產品中亞硝胺最大含量50g/kg,存放于無亞硝酸鹽的容器內。即三乙醇胺應當滿足幾個方面的要求:1)使用條件限制其不和亞硝基化體系一起使用,避免形成亞硝胺;2)原料的純度、以及原料中無法避免帶入禁用物質仲鏈烷胺的最大含量限制;3)使用該原料的終產品中亞硝胺的最大允許限量;4)原料的存放條件要求其存放于無亞硝酸鹽的容器中。
亞硝胺是包含了R2(R1)N-N=O結構的一類化合物,在自然界中,亞硝酸鹽極易與胺類發生反應生成亞硝胺。亞硝胺的毒性主要體現在急性毒性和致癌性兩個方面,可引起急性肝損傷,在體內經代謝酶活化后產生廣譜致癌性。從上述分析可以看出,2-溴-2-硝基丙烷-1,3-二醇和三乙醇胺兩種原料同時使用,有形成亞硝胺風險,不符合《規范》要求,可能影響產品安全性。
2.3.2 防腐劑使用超出了限制條件
化妝品中含有大量水和營養物質,為防止微生物生長繁殖,導致產品腐敗變質,配方中通常會添加防腐劑。碘丙炔醇丁基氨甲酸酯(IPBC)是有效的防腐劑,能抑制霉菌、酵母菌等真菌生長,常與抑制細菌生長的防腐劑搭配使用,構成防腐體系,但IPBC有可能導致接觸性皮炎的報道,吸入后會引起神經毒性、肝臟毒性,研究表明IPBC含量為0.2%時能夠滿足人體安全要求。在我國《化妝品安全技術規范》中對其使用有一系列限制:要求禁用于三歲以下兒童,禁用于唇部產品,使用于駐留類產品時禁用于體霜體乳等;對其最大允許使用濃度的要求為,淋洗類產品0.02%,駐留類產品0.01%,除臭產品和抑汗產品0.0075%。
某產品配方中含有IPBC,使用方法為“取適量本品均勻涂抹于可能暴露在陽光下的皮膚上”。根據該產品的使用方法,作為駐留類產品其可能大量用于身體表面,因此,具有一定的安全隱患。
2.3.3 著色劑使用不符合《規范》要求
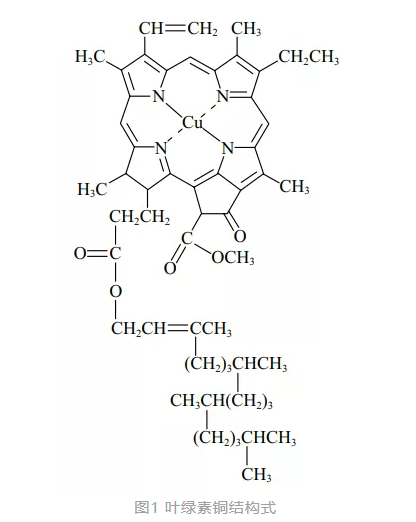
某染發產品申報配方含有葉綠素銅(COPPERCHLOROPHYLL),使用目的為“著色劑”。而《規范》準用著色劑列表中收錄了著色劑索引號為CI75810的物質,其著色劑索引通用中文名為天然綠3(葉綠酸-銅絡合物)。在歐盟委員會化妝品成分數據庫中,著色劑索引號CI75810對應的物質INCI名稱為CHLOROPHYLLIN-COPPERCOMPLEX(CAS號:11006-34-1),作為著色劑使用;葉綠酸-銅絡合物(CHLOROPHYLLIN-COPPERCOMPLEX)是葉綠素(CHLOROPHYLL)通過堿水解,取代了甲基等基團,并以銅取代鎂來制得的。經過水解過程,去除疏水性側鏈,增加了水溶性。
葉綠素銅(COPPERCHLOROPHYLL)也是一種著色劑,其結構式如圖1所示。葉綠酸-銅絡合物和葉綠素銅不是同一種物質,葉綠素銅未收載于《化妝品安全技術規范》著色劑列表中,其作為著色劑使用的安全性需要進一步論證。
2.4 申報資料前后不一致的情況
申報資料前后不一致,影響技術判斷的情況具體包括:產品申請注冊時經檢驗機構確認的配方發生改變;配方以外的資料與申報配方不符;在補充資料階段,提交的產品的生產工藝和首次申報時不一致;已作出建議不批準結論的產品,復核時申報單位自行改變產品原申報資料。下面結合具體案例就上述問題開展分析。
2.4.1 檢驗機構確認的配方發生改變
在產品申報階段,注冊人將產品送到化妝品注冊和備案檢驗檢測機構,經過檢驗檢測機構蓋章確認的產品配方一般情況下不能更改,如果的確在配方填報出現了文字性的錯誤,需要作出修改的,需要注冊人提交說明材料,以備技術評價時參考判斷。
某產品配方中申報了“浮游生物提取物”,按照我國《已使用化妝品原料目錄》,“浮游生物提取物”是一類原料,應當說明所包含的具體原料。該產品與檢驗機構蓋章確認的配方相比,注冊人將“浮游生物提取物”所指的具體原料進行了修改,并提供了藻類在分類學上的相關資料,以證明修改前后的所指的具體原料僅為文字表述的不同,配方并未發生實質性改變。經查,提供的說明性文件不能夠支持注冊人的說法,修改前后所指的兩種藻類拉丁學名不同,不是同一原料。
2.4.2 配方以外的資料與申報配方不符
配方以外的資料顯示原料種類或含量與申報配方不符,此類情況比較常見,往往是注冊人疏忽導致。例如某產品在生產工藝中,列出了工藝的各個分相以及各分相對應的原料序號,但是對照配方發現,配方中缺少工藝中列出的某些原料;此外標簽中標注的成分在配方中未見也是常見的和配方不符的情況,根據《GB5296.3—2008消費品使用說明化妝品通用標簽》的要求,在化妝品銷售包裝的可視面上應真實地標注化妝品全部成分的名稱。《化妝品技術審評指南》中也明確要求“產品包裝(含產品標簽、產品說明書)所標注的原料名稱,涉及含量應與產品配方相符”。標簽標示成分未在配方中出現的情形,依據《化妝品技術審評要點》,屬于出具“建議不批準”評價結論的情形。
2.4.3 生產工藝前后不一致
此類情形通常和生產工藝不合理的問題同時出現。例如某祛斑類產品的配方中,抗壞血酸作為祛斑功效成分添加量達到22%,配方中其他原料包括丙二醇、聚乙二醇-8、甘油、丁二醇等,含量均低于抗壞血酸。抗壞血酸易溶于水、甲醇,溶解度會隨著溶劑極性降低而下降,在三氯甲烷或乙醚中不溶。生產工藝為70℃攪拌溶解后冷卻、灌裝,終產品的感官指標描述為“微黃色透明液體”。
根據其生產工藝描述,技術評價時對在現有配方和工藝條件下能夠制成“微黃色透明液體”提出質疑,要求進一步提供能制成本品的科學依據,以及抗壞血酸在丙二醇等溶劑中的溶解度等資料。注冊人在后續補充資料中,申報工藝發生了明顯變化,包括原料分相、加熱溫度、以及生產設備種類等,涉及了重要工藝參數的調整。需要指明的是,產品在申報注冊時提交的工藝,應為經過小試、中試放大、實際生產等環節后,其合理性和可操作性已經確定的生產工藝,關鍵工藝參數應準確、清晰。
2.4.4 已作出建議不批準結論的產品,復核時申報單位自行改變產品原申報資料
根據上述法規、部門規章和規范性文件開展特殊化妝品技術評價時,技術結論分為3種,分別為:建議批準、補充資料延期再審和建議不批準。某產品被出具建議不批準意見之后,如果注冊人對意見有異議,可以選擇申請復核,復核階段需要提交對結論有異議的理由和相關證明資料。技術評價對復核資料不予認可的,維持原“建議不批準”結論;認可相關資料,可以修改為建議批準結論或要求補充資料后,延期再審。
“2.3.2”中因防腐劑使用超出了限制條件的產品,在復核階段注冊人提出將“使用方法”修改為“涂抹于面部肌膚”,從而滿足《規范》中“使用于駐留類產品時禁用于體霜體乳”的要求。此處需要說明的是,復核階段僅對先前作出的不恰當結論予以更正,如果先前建議不批準結論無誤,則對復核理由不予認可。同時一個產品在設計之初,就應根據配方明確具體使用方法、使用部位等,而非根據不批準意見做臨時的調整,因此復核結論為不認可復核理由,維持原結論。
3、結語
1)我國現行法規按風險程度對化妝品實施分類管理,因特殊化妝品相對于普通化妝品具有較高的風險,其化妝品安全技術評價是化妝品監管中的重要組成部分。從技術評價工作實際出發,有針對性地對化妝品安全技術評價相關法規、常用的部門規章和規范性文件進行較為詳細的介紹和解讀,了解并熟悉其中內容,對于掌握評價尺度、實現科學評價大有裨益。
2)結合在第一線開展安全技術評價工作的體會,筆者對影響特殊化妝品安全性的問題進行了歸納和梳理,并進行了較為系統的分析,彌補了目前特殊化妝品安全評價常見問題相關報道的匱缺,并在結合相關法規、部門規章和規范性文件的基礎上,對具體案例開展了分析,對于指導產品研發、資料編撰、安全評價具有實際參考意義。
3)根據筆者在文中的介紹和分析,化妝品安全技術評價中發現的主要問題,以影響產品安全性的問題為主,例如產品不符合化妝品定義范疇、產品中使用了未經我國化妝品監管部門批準的新原料、產品配方不符合《化妝品安全技術規范》要求,都將導致評價過程中無法進行安全性的判斷,這也從技術評價角度反映出安全性是化妝品基本屬性的特點;此外還有申報資料前后不一致,除了涉及影響安全性判定之外,還涉及了資料真實性的問題,因此,維護技術評價工作的嚴謹性和嚴肅性也是需要堅持的重要原則。
化妝品申請人、開展評價工作的技術人員應加強學習,既要注重資料中影響安全性問題的甄別,在資料編撰、資料技術評價中能夠有的放矢,同時申請人更應當注重進一步提高申報資料的質量,對于不必要的錯誤應盡量避免,從而縮短產品申報的周期,更充分地發揮技術評價資源的作用。
4)在新的《化妝品監督管理條例》框架下,對化妝品注冊人、備案人在質量管理體系、不良反應監測與評價等方面提出了更高的要求,注冊人、備案人對產品的質量安全和功效宣稱的主體責任更加突出,化妝品監管實現社會共治的理念更加凸顯;同時原料風險作為產品風險的一個重要來源,對新原料的管理要求變化較大。例如化妝品新原料將實行3年監測期制度,同時在《條例》配套文件中,對化妝品新原料在安全性評價、安全監測及突發情況報告等方面,均提出了明確的資料要求;此外《條例》還強調了化妝品監督管理的信息化建設,對于監管信息共享、失信管理也將邁上一個新臺階。
相關推薦:
- 多種原料被禁用?專家帶你全面解讀兒童化妝品新規!
- 4個化妝品新原料成功備案 化妝品企業研發創新迎來新機
- 市場監管總局關于發布《醫療美容廣告執法指南》的公告
- 化妝品注冊備案信息服務平臺使用常見問題解答
- 2021年至今,監管部門發布的化妝品檢驗檢測機構不合格問題匯總
我們的服務:
