近年來,母乳低聚糖(Human milk oligosaccharides,HMOs)儼然成為奶中“新貴”而被大眾所熟知。且隨著科學技術的發展和研究的深入,人們也越來越意識到它的重要性。母乳低聚糖,又稱人乳低聚糖,是母乳中僅次于乳糖和脂肪的第三大固體成分,是一類獨特的、天然存在于母乳中的復雜混合碳水化合物。眾多研究表明,HMOs能促進有益菌的生長,為人體提供獨特的營養價值,因此,國內外企業相繼開啟了“與母乳營養匹配”的嬰幼兒配方食品的研究和開發。
隨著HMOs在食品營養領域的重要性不斷被印證,其典型代表成分2'-巖藻糖基乳糖(2'-FL)已相繼在歐盟、美國和澳新拿下“通行證”,開啟了商業化應用模式。但在中國,2'-FL還未獲批使用,但已有許多企業開啟了申報之路。作為新興的功能性配料,2'-巖藻糖基乳糖的法規現狀和產業化研究應用前景如何?在中國何時能迎來批準的“春天”?瑞旭集團帶您一探究竟。
1、2'-FL簡介
2'-巖藻糖基乳糖是一種中性巖藻糖基化的人乳低聚糖,在HMOs中約占31%(摩爾分數),含量為0.06~3.93 g/L,是人乳中相對豐度最高的寡糖[1],組成單體包括巖藻糖、半乳糖和葡萄糖。
英文名稱:2'-Fucosyllactose,2'-O-fucosyllactose(2'-FL)
化學名稱:α-L-吡喃巖藻糖基-(1→2)-β-D-吡喃半乳糖基-(1→4)-D-吡喃葡萄糖苷
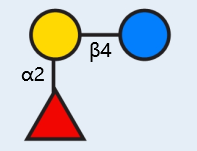
2’-巖藻糖基乳糖結構
![]()
2、2'-FL國內外法規現狀
2'-巖藻糖基乳糖是人乳中含量最高的寡糖,也是最早被美國FDA和歐盟批準可添加到嬰幼兒奶粉、普通食品、膳食補充劑和/或醫療食品中的HMOs之一。同時,澳新也已批準了微生物發酵生產的2'-FL的使用。
- 美國
截至目前,已有多款2'-巖藻糖基乳糖(單一成分或混合產品)經美國食品藥品監督管理局(FDA)批準作為“一般公認安全”(GRAS)物質。使用范圍包括嬰幼兒配方奶粉以及烘焙食品、乳制品、飲料等普通食品類別,使用量因申報單位不同而要求不一。
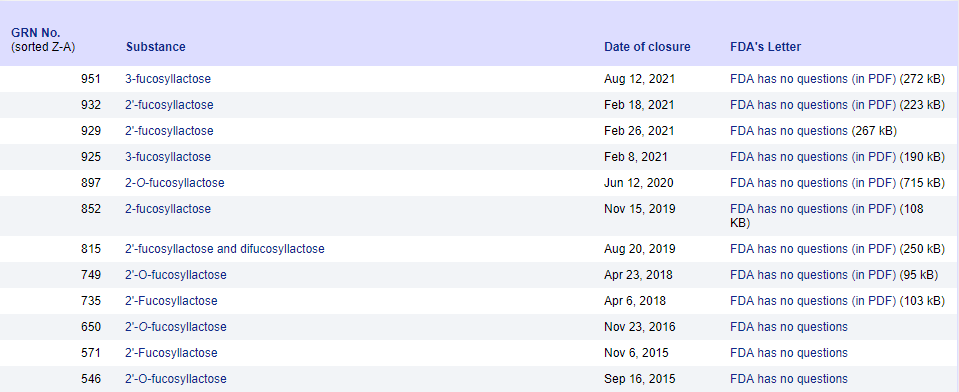
圖片來源:美國FDA
- 歐盟
根據歐洲委員會法規(EU) 2017/2470,即根據歐洲議會和理事會關于新型食品法規(EU)2015/2283建立的新型食品清單,2'-巖藻糖基乳糖已被批準作為新食品原料(Novel Food),包括合成法來源、轉基因大腸桿菌BL21菌株生產來源和轉基因大腸桿菌K-12菌株生產來源。使用范圍包括嬰兒配方奶粉、膳食補充劑、發酵乳制品、咖啡、茶等,在嬰兒和較大嬰兒配方奶粉中的單獨用量最高為1.2 g/L(以即食產品計)。
- 澳新
澳大利亞新西蘭食品標準局(FSANZ)于2019年12月首次批準了通過使用轉基因微生物發酵產生的2'-FL和LNnT在嬰兒配方食品和幼兒配方補充食品中的應用。2021年11月8日,FSANZ對通過轉基因大腸桿菌(E.co.coli)菌株發酵生產的2'-FL用于嬰兒配方食品、較大嬰兒配方食品和幼兒配方補充食品的應用申請發布批準報告。
- 中國
早在2016年8月10日,就有企業嘗試申報微生物來源的2'-巖藻糖基乳糖,申報類型為營養強化劑(受理編號:衛食添新申字(2016)第0040號),申報使用范圍為嬰幼兒配方食品。同年8月15日,國家食品安全風險評估中心(CFSA)就該受理產品資料中“可以向社會公開的內容”進行公開和意見征集(未經過CFSA技術審查)。但此后,該產品的審評消息便石沉大海。
2021年以來,衛健委共受理了多款2'-巖藻糖基乳糖作為食品添加劑新品種的申報事項,其中,有4款產品已通過專家技術審評,進行公開征求意見。
2'-巖藻糖基乳糖產品的受理、審評等信息情況匯總如下表:
|
序號 |
受理信息 (時間/受理編號) |
審評信息/狀態 |
最新公開狀態 |
|
1 |
2021.07.02 衛食添新申字(2021)第0028號 2'-巖藻糖基乳糖(合成法) |
2021.07.26:發布延期通知書信息 2021.10.21:公開征求意見(點擊查看詳情) 2021.11.22:發布延期通知書信息 2022.01.18:發布延期通知書信息2022.01.18:發布延期通知書信息 |
已征求意見 |
|
2 |
2021.10.18 衛食添新申字(2021)第0048號 2'-巖藻糖基乳糖 |
2021.11.22:發布延期通知書信息 2022.01.18:發布延期通知書信息 2022.04.15:公開征求意見(點擊查看詳情) 2022.06.13:發布延期通知書信息 2022.07.28:發布延期通知書信息 2022.10.28:公開征求意見(點擊查看詳情) 2023.01.19:發布延期通知書信息 |
已征求意見 |
|
3 |
2021.11.03 衛食添新申字(2021)第0050號 2'-巖藻糖基乳糖 |
2021.11.22:發布延期通知書信息 2022.01.18:發布延期通知書信息 2022.04.15:公開征求意見(點擊查看詳情) 2022.06.13:發布延期通知書信息 2022.07.28:發布延期通知書信息 2022.10.28:公開征求意見(點擊查看詳情) 2023.01.19:發布延期通知書信息 |
已征求意見 |
|
4 |
2022.11.15 衛食添新申字(2022)第0085號 2'-巖藻糖基乳糖 |
2023.01.19:發布延期通知書信息 |
補正中 |
|
5 |
2023.01.05 衛食添新申字(2023)第0003號 2'-巖藻糖基乳糖 |
2023.02.10:公開征求意見(點擊查看詳情) |
已征求意見 |
|
6 |
2023.07.14 衛食添新申字(2023)第0045號 2'-巖藻糖基乳糖 |
2023.07.14:發布受理信息 |
審評中 |
3、2'-FL產業化研究現狀
2'-FL是中性巖藻糖基化HMOs的典型代表,在人乳中相對豐度最高,具有調節腸道菌群、抵抗病原菌的黏附、免疫調節以及促進神經系統發育和修復等多種功能活性[2]。目前,商業化2'-FL的生產主要包括化學合成、酶催化合成和微生物發酵生產三種方式[3]。
化學合成法所需原料成本高,且一般來說生產過程較為繁瑣、耗時。酶催化合成需要特定的巖藻糖基轉移酶,雖然酶法合成2'-FL反應條件溫和可控、時間短、產物易于純化,但生產所需的糖基供體成本高,很大程度上依賴于提高糖基轉移酶效率的蛋白質工程的發現,距離工業化生產還需要一定時日[4]。
微生物發酵生產是目前工業上生產2'-FL的主要方式,是基于微生物自身(或模擬)的代謝機制,利用廉價的碳源和微生物自身細胞內的酶、代謝中間體及能量直接生物合成2'-FL。在此過程中,通過基因工程技術表達初始宿主細胞原本缺乏的酶片段,使其增添缺失的功能。此種生產方式成本相對較低且可大規模生產。
4、2'-FL在中國將迎來“春天”
如前所述,獲得美國FAD GRAS認證的2'-FL產品中,絕大多數為轉基因微生物來源,包括轉基因大腸桿菌和轉基因谷氨酸棒桿菌。而歐盟同樣批準了轉基因微生物來源的2'-FL。而在我國,事實上,在2020年之前,除了轉基因微生物來源的酶制劑能在我國進行新品種申報外,其他涉及轉基因技術的新食品原料或新食品添加劑的安全評估程序一直未能明確。而這或許便是2016年申報的那款2'-巖藻糖基乳糖遲遲未有進展的原因。
2021年,國家衛健委打開了我國轉基因微生物食品添加劑的申報路徑,正式開始受理和審批轉基因微生物食品添加劑新品種。關于轉基因微生物食品添加劑新品種的詳細申報流程及材料要求,請參看:轉基因微生物食品添加劑新品種申報。
這一好政策給通過基因改造的微生物發酵生產的HMOs們在中國的合規使用鋪設了道路。僅2021年下半年短短半年時間內,就有3家企業提交了2’-FL的新品種申請,開始在中國進行合規布局,截至2023年7月底,合計共有6款產品提交申請,且4款產品已進行征求意見。目前,相信不久后就能看到2'-巖藻糖基乳糖在中國拿到“通行證”。屆時,中國嬰幼兒營養市場將不斷被開拓,嬰幼兒配方奶粉和母乳間的空白也將逐漸填補。如此看來,在中國,2'-巖藻糖基乳糖的“春天”還遠嗎?
更多關于母乳低聚糖獲批后在嬰幼兒配方奶粉和特醫嬰配中的應用及相關企業布局,請參看:母乳低聚糖(HMOs)——預期獲批后的應用及相關企業布局。
我們的服務:
更多法規報告免費獲取:
- 免費獲取!2022年食品法規及行業熱點年度盤點報告 (點擊查看)
更多食品內容解讀查看:瑞旭集團食品會議
相關推薦:

