2016年7月1日,《保健食品注冊與備案管理辦法》(以下簡稱“《辦法》”)正式施行,該《辦法》規定生產和進口下列保健食品應當依法備案:(1)使用的原料已經列入保健食品原料目錄的保健食品;(2)首次進口的屬于補充維生素、礦物質等營養物質的保健食品(其營養物質應當是列入保健食品原料目錄的物質)。截至2019年12月31日,已有上千款保健食品獲得備案憑證。為了幫助企業更好的了解保健食品備案現狀,瑞旭集團對已備案產品進行了統計,并從多個角度進行分析。
1.保健食品備案情況
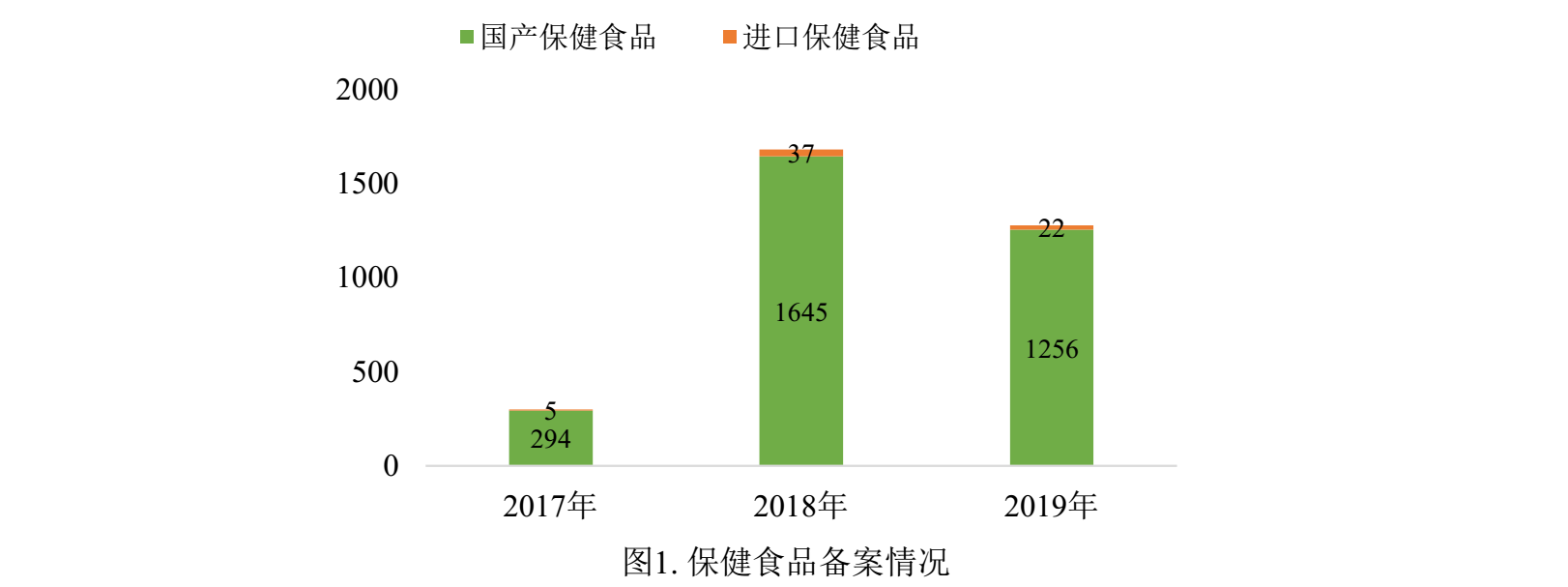
2017年7月27日原廣東省食品藥品監督管理局發布第一款國產保健食品備案公告,截至2019年12月31日,已有3259款保健食品獲得備案憑證,其中,3195款為國產保健食品,64款為進口保健食品。
2.不同地域保健食品備案情況
2.1國產備案產品
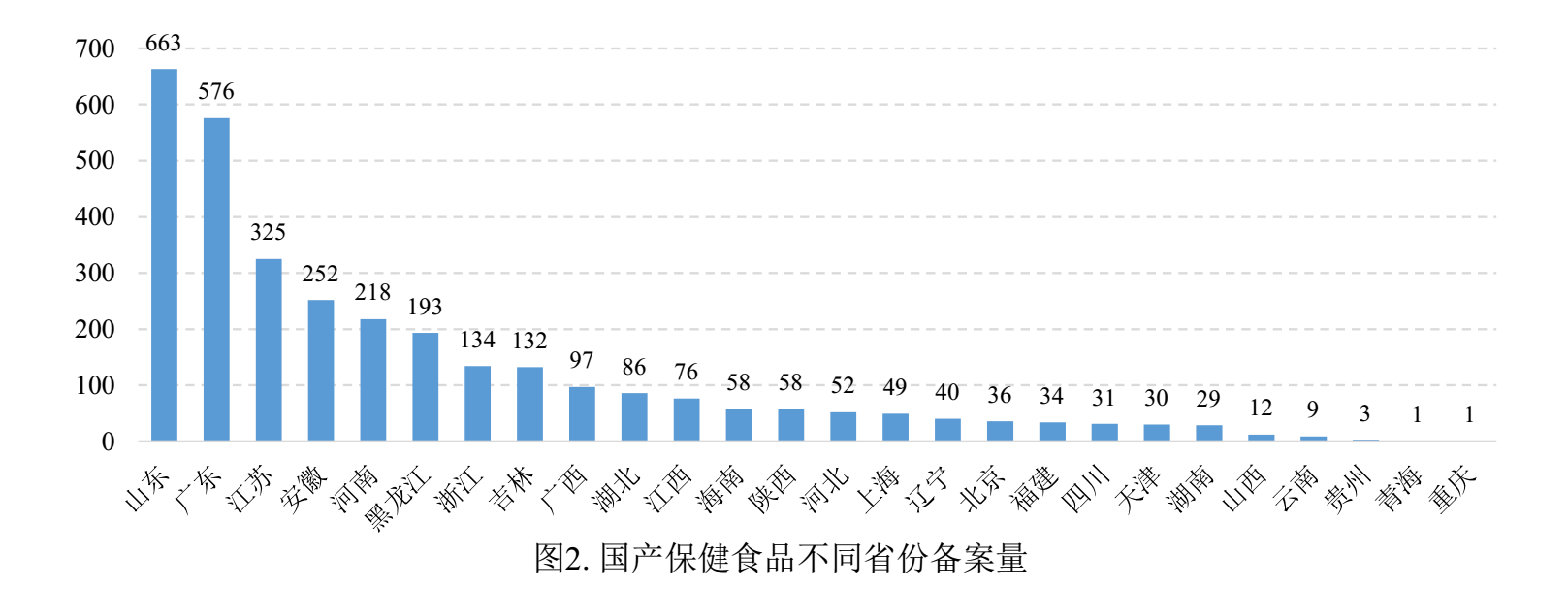
國產保健食品各省備案情況千差萬別,其中山東省和廣東省獲得備案憑證的產品分別為663款和576款,備案數量位列第一和第二位,分別占據全國備案產品總量的20.75%和18.03%。
2.2進口備案產品
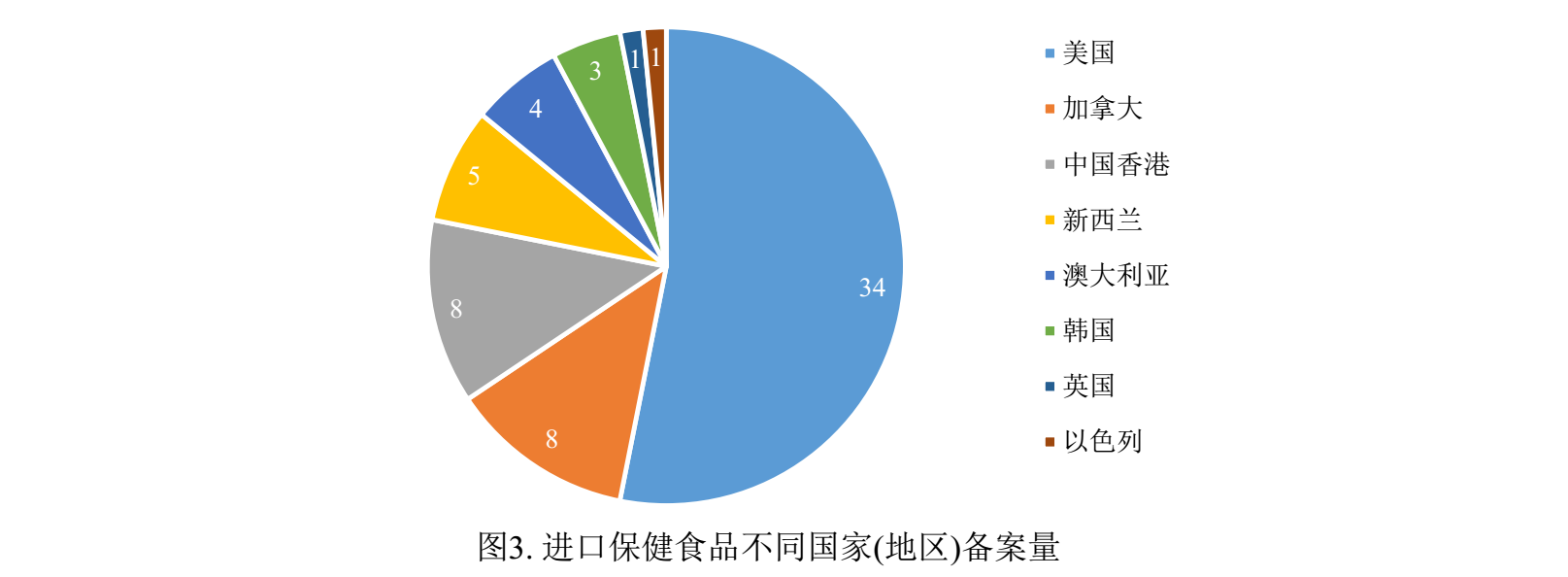
對于進口保健食品而言,獲得備案憑證的產品其備案人分別來自于美國、加拿大、中國香港、新西蘭、澳大利亞、韓國、英國和以色列8個國家/地區,并且64款已備案產品中34款產品的備案人為美國企業。而生產國為英國和以色列的保健食品均為2019年首次獲得備案憑證。
3.不同企業保健食品備案情況
3.1國產備案產品
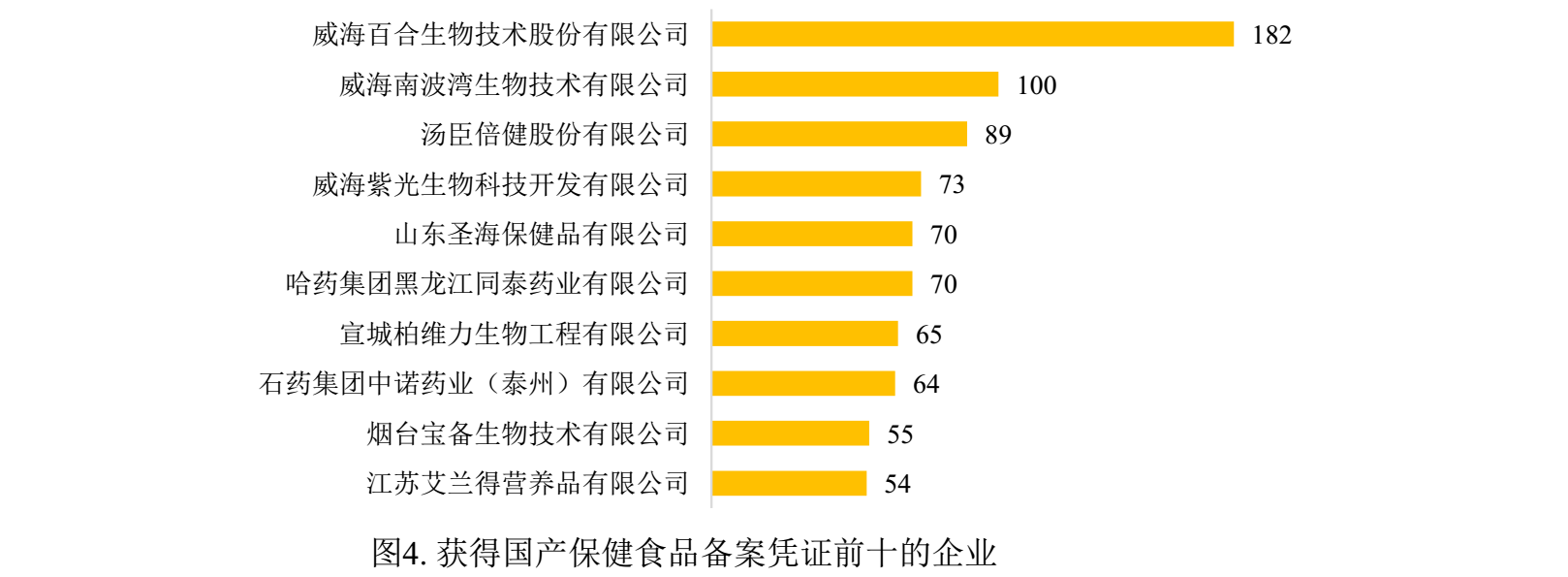
已備案的國產保健食品分別來自363家企業。其中威海百合生物技術股份有限公司共182款保健食品獲得備案憑證,備案數量最多;威海南波灣生物技術有限公司共100款保健食品獲得備案憑證,備案數量位居次席;湯臣倍健股份有限公司有89款保健食品獲得備案憑證,位居第三。
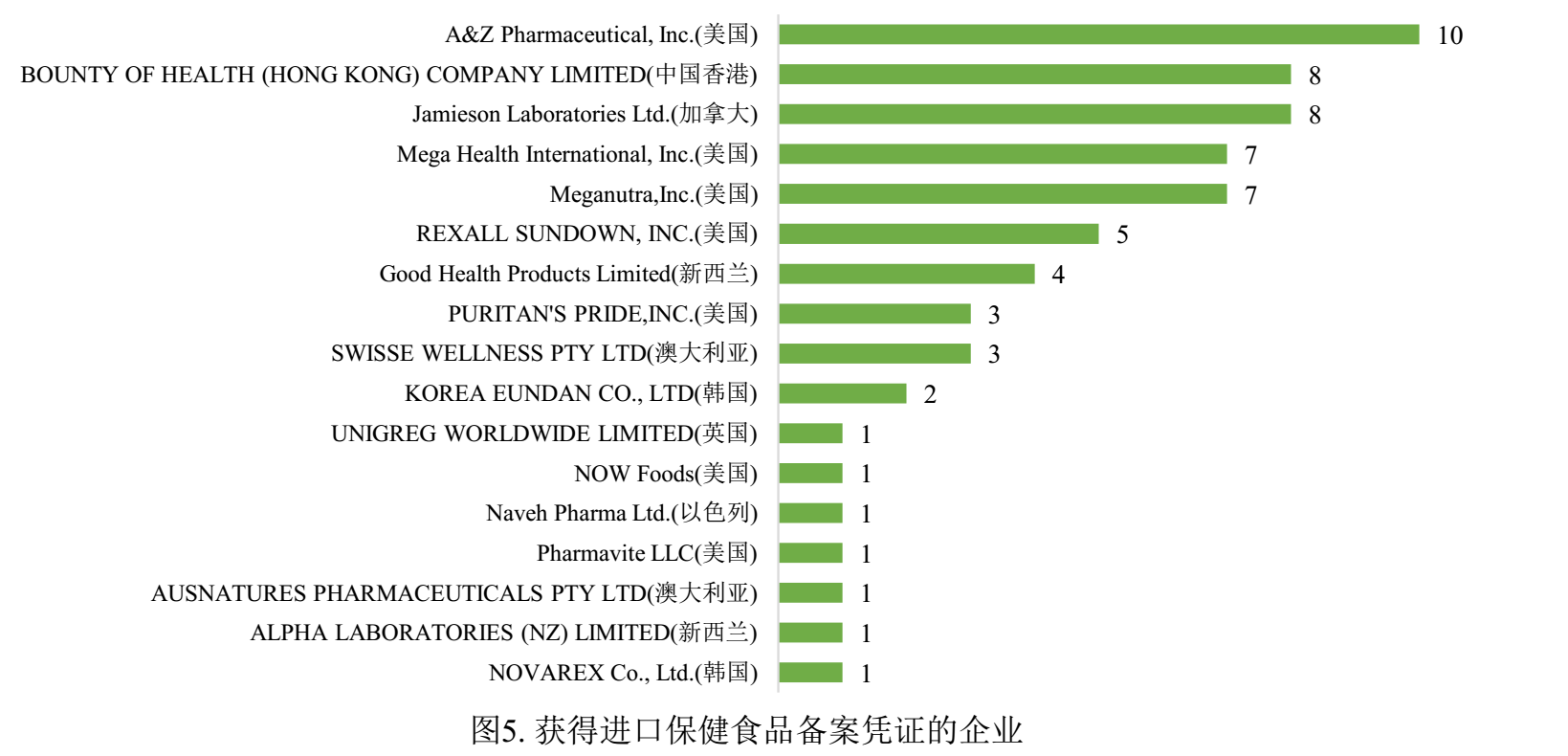
已備案的進口保健食品分別來自17家企業,其中,A&Z Pharmaceutical, Inc.(美國安士制藥有限公司)共10款保健食品獲得備案憑證,備案數量最多;BOUNTY OF HEALTH (HONG KONG) COMPANY LIMITED(健之寶(香港)有限公司)和Jamieson Laboratories Ltd.(健美生實驗室有限公司)分別獲得8款保健食品備案憑證,備案數量位居次席;Mega Health International, Inc.(美格健康國際有限公司)和Meganutra,Inc.(美國美格樂特生物有限公司)分別獲得7款保健食品備案憑證,備案數量位居第三。
4.不同劑型備案情況
4.1國產備案產品
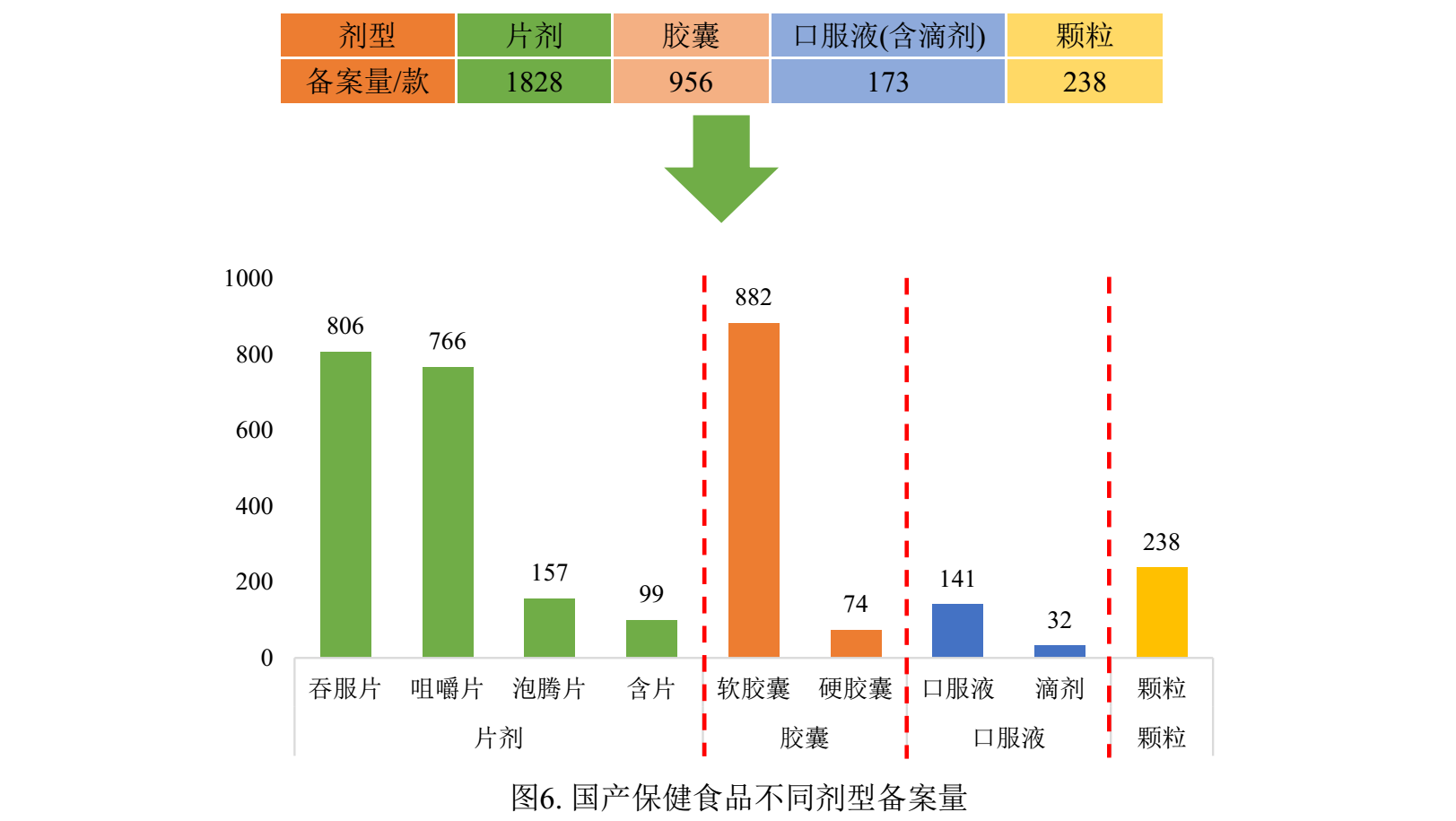
保健食品備案產品劑型目前包括片劑、膠囊、口服液和顆粒。
已備案國產保健食品的劑型主要為片劑,備案數量達1828款,占國產保健食品備案總量的57.25%。片劑產品中以吞服片和咀嚼片居多,分別為806款和766款,而泡騰片和含片備案數量僅有157款和99款。
膠囊主要包括軟膠囊和硬膠囊兩類產品,產品備案總量為956款。其中,軟膠囊產品數量遠高于硬膠囊產品,軟膠囊產品為882款,而硬膠囊產品僅有74款。
除此之外,口服液(含滴劑)和顆粒劑產品備案數量分別為173款和238款,其中口服液產品中滴劑僅有32款。
4.2進口備案產品
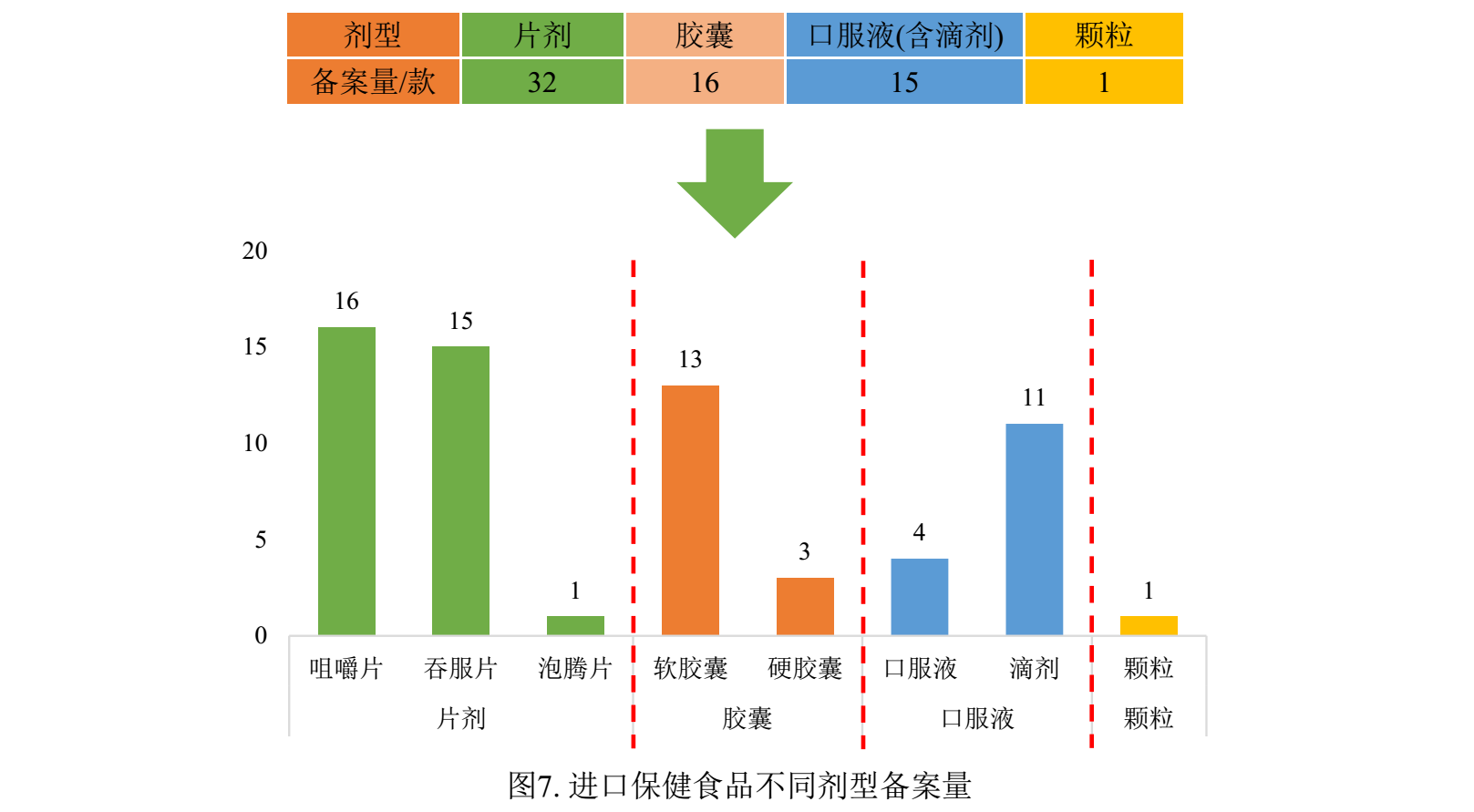
已備案進口保健食品的劑型主要為片劑,備案數量為32款,占進口保健食品備案總量的50%。片劑產品中以咀嚼片和吞服片居多,泡騰片僅有1款產品,尚未出現含片劑型的產品;膠囊和口服液(含滴劑)產品備案數量分別為16款和15款,與國產備案產品相似的是軟膠囊產品備案數量高于硬膠囊產品;與國產備案產品不同的是,進口備案產品中滴劑產品備案量高于口服液產品。顆粒劑型的產品目前僅有1款。
5.不同營養素備案量
5.1國產備案產品
已備案的國產保健食品中補充單一營養素的產品最多,備案數量為1429款,其次為補充多種營養素和補充兩種營養素的產品。
國產備案產品中補充多種維生素礦物質的產品、補充維生素C的產品和補充鈣和維生素D的產品為三大主流產品,備案數量分別為531款、486款和314款。
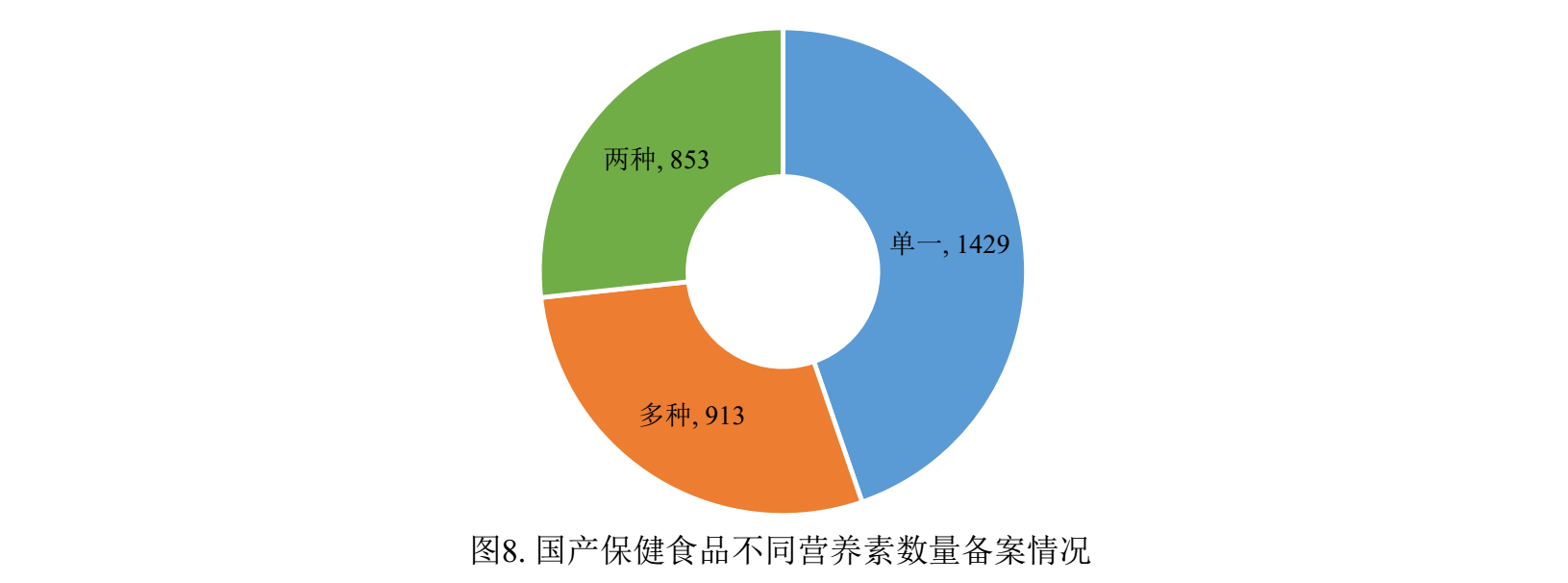
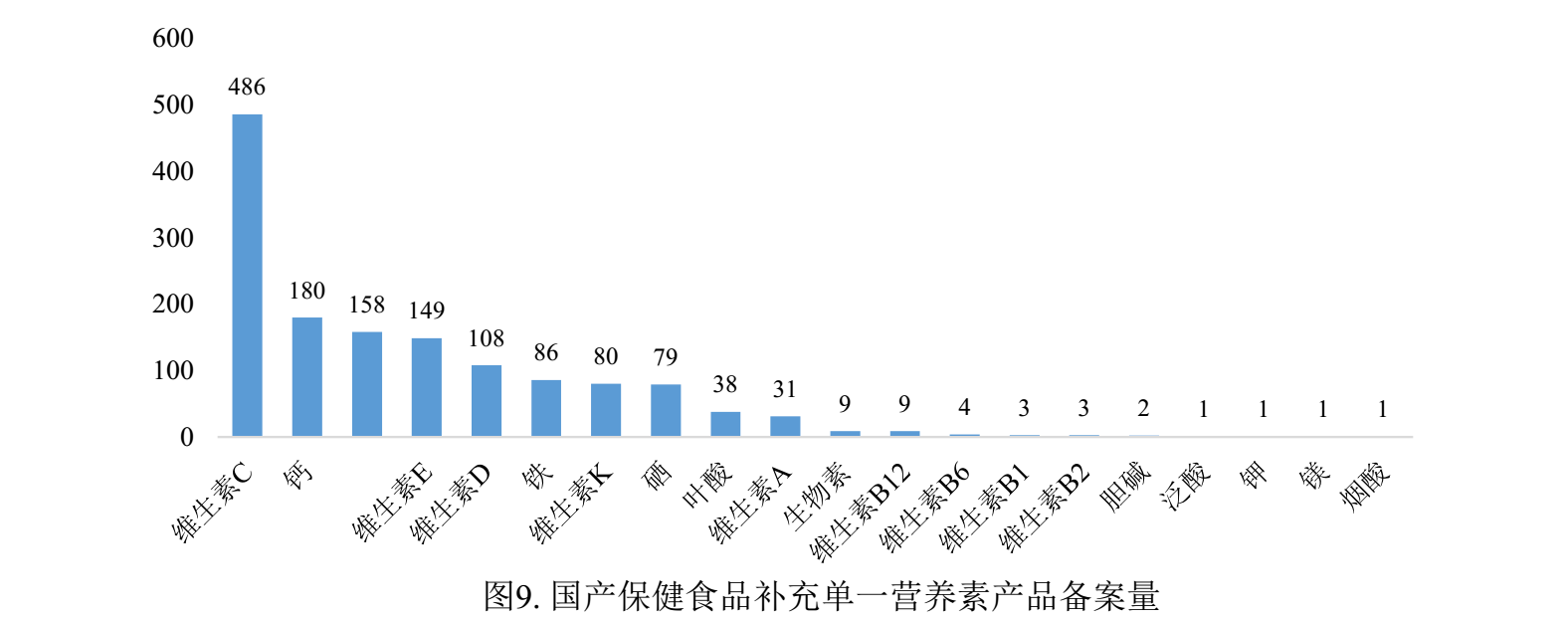
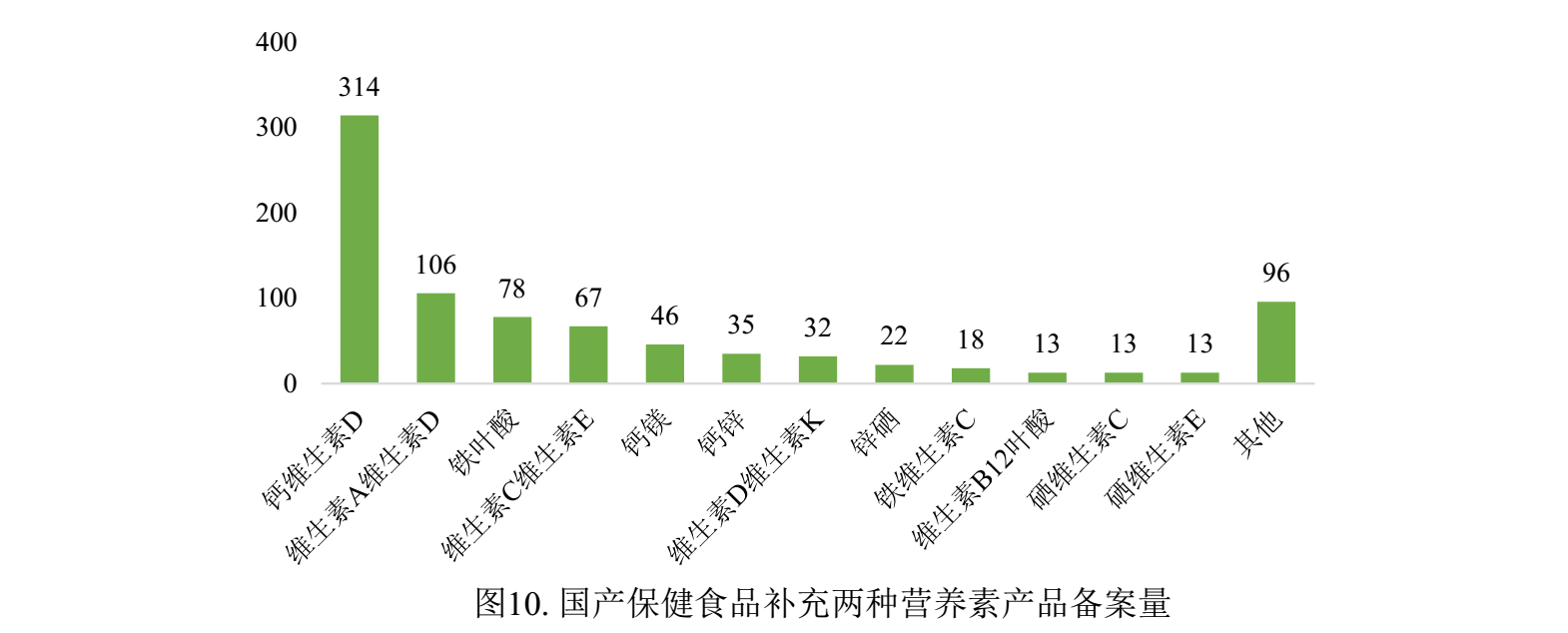
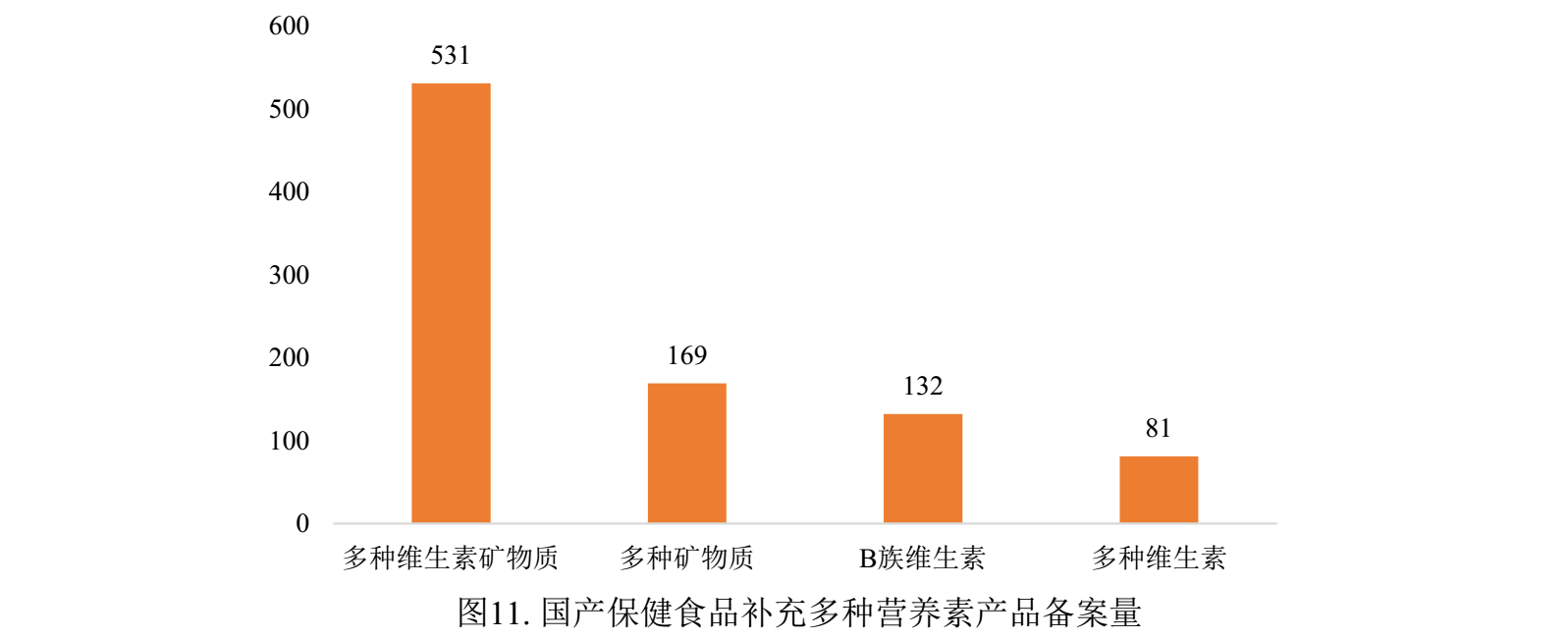
注:產品數量少于13款的保健食品歸為“其他”。
5.2 進口備案產品
已備案進口保健食品中補充多種維生素礦物質的產品、補充鈣和維生素D的產品和補充維生素D的產品為三大主流產品,備案量分別為9款、9款和7款。
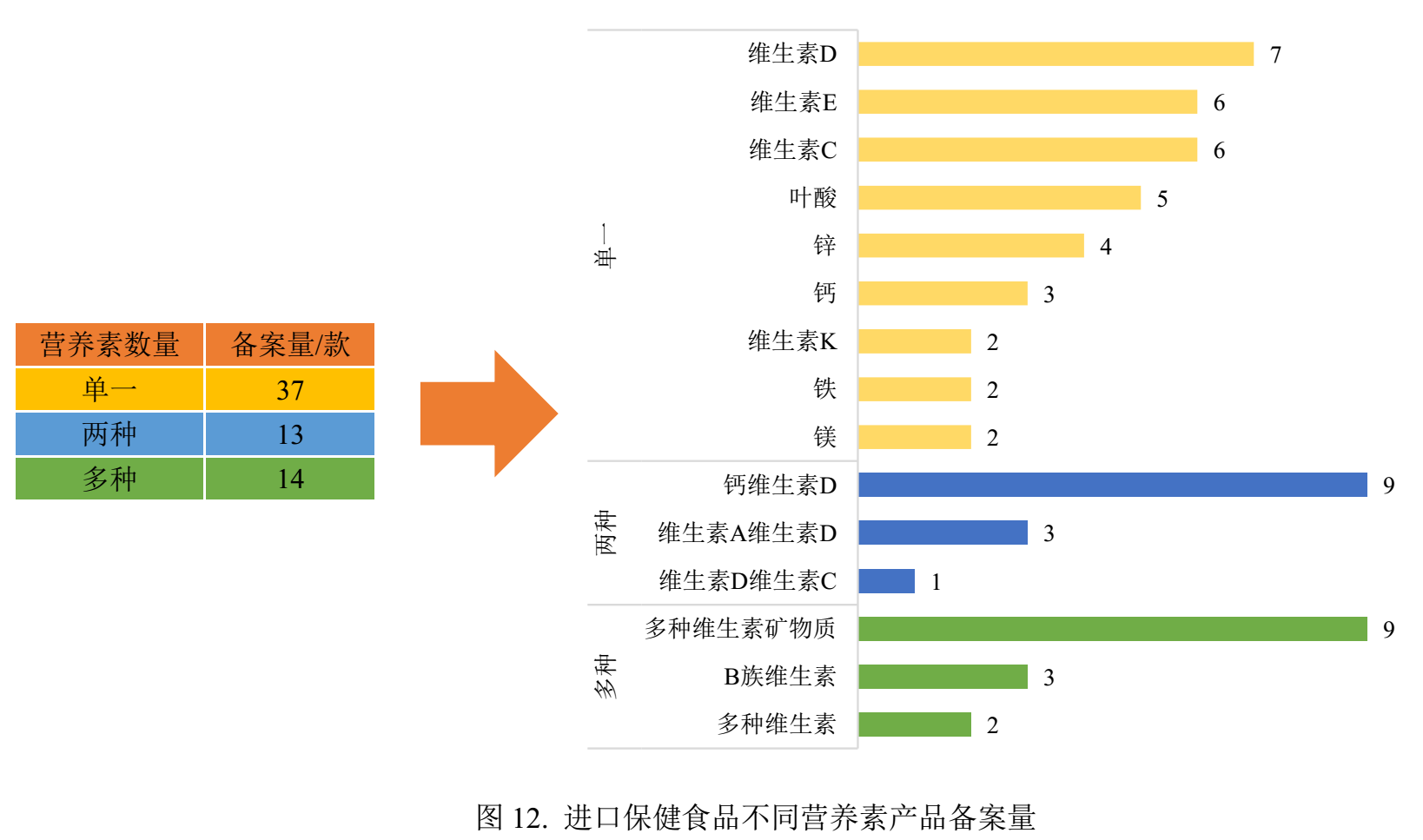
6.瑞旭觀點
保健食品備案制的實施,減少了行政審批流程,申報周期和費用均明顯低于保健食品注冊,因此倍受保健食品企業青睞。2017年至2019年,已有三千多款產品通過備案,而進口備案產品僅有64款,數量遠遠低于國產備案產品。瑞旭集團認為進口保健食品備案通過率低的主要原因在于企業對中國保健食品法規缺乏了解,相關證明文件不能滿足法規要求導致產品不能順利備案。
保健食品企業為躋身備案大軍而欣喜的同時,同質化產品競爭的壓力接踵而至。保健食品備案產品原輔料的限制,注定了產品同質化嚴重的命運,如何突顯產品優勢成為企業產品設計的關鍵點。而《保健食品備案產品可用輔料及其使用規定(2019年版)》的施行,給保健食品企業帶來了新的希望。與17版輔料目錄相比,新版輔料目錄新增了17個可用輔料,包括磷脂、辛,癸酸甘油酯等常見的食品添加劑,果蔬粉等常見的普通食品原料,都為豐富備案產品的口味,增強產品市場競爭力提供了更有利保障。此外28個輔料新增的使用標準也為企業選擇供應商提供了更大的空間。另一方面,待《輔酶Q10等5種保健食品原料目錄、技術要求(征求意見稿)》正式通過后,在備案產品的原料選擇和功能聲稱方面,企業也將獲得更多的選擇空間。
(注:國家機構改革導致各省市政府部門官方網站新舊網址更替,國產保健食品備案數據統計過程中可能有所疏漏,本文數據僅供參考,請以政府部門官方公布的信息為準。)
作者:朱琳
