為了指導企業更好地進行保健食品注冊和備案工作,國家市場監督管理總局曾多次在保健食品備案管理信息系統和食品審評中心發布保健食品常見問題與解答。瑞旭集團特對這些內容進行匯總和梳理,形成保健食品常見問題與解答系列,供企業查閱。
往期回顧:保健食品常見問題與解答——注冊篇(1):配方及原料。
保健食品常見問題與解答——注冊篇(2):功能學和毒理學評價。
本期內容:保健食品常見問題與解答——注冊篇(4):技術要求和說明書。
01 保健食品產品技術要求常見問題及注意事項(2021-10-08)
答:產品技術要求是保障保健食品質量可控的重要技術資料,也是保健食品注冊證書附件的重要組成部分。《保健食品注冊與備案管理辦法》規定了保健食品產品技術要求的主要內容,《保健食品注冊審評審批工作細則(2016年版)》《保健食品注冊申請服務指南(2016年版)》等規范性文件進一步明確了各項內容的具體要求。但是,在審評過程中,我們發現申請人提交的產品技術要求材料質量不高,問題較多,極大地影響了審評工作效率。
為進一步提高申請材料質量,提升工作效率,我們將產品技術要求常見問題和注意事項進行了匯總,供注冊申請人借鑒。
一、常見問題及注意事項
(一)注冊信息系統填報的產品技術要求與紙版資料不一致。請按照最終確定版本,認真、逐項填寫產品技術要求內容。產品技術要求電子版應為文本格式,請勿提交PDF、圖片、鏈接等格式文件。
(二)延續、變更、轉讓等注冊申請,提交的產品技術要求內容與原注冊內容不一致。請根據原批準證書及附件、注冊申請材料,按照新的規定,完善產品技術要求。
(三)擅自修改產品技術要求未發補內容。補充資料中需提交產品技術要求的,不要擅自修改審評意見未涉及內容,同時產品技術要求電子版與紙版內容保持一致。
(四)其他常見問題,主要包括:
1.【生產工藝】項
(1)除首次申報產品(受理編號為國食健申),其余申報類型產品生產工藝主要流程應與原批件保持一致,同時應當在主要關鍵工藝后以括號標注關鍵工藝參數。
(2)提取關鍵工藝參數應包括溶劑、溶劑量、溫度、次數、時間等。例如:分別加6、6、8倍量70%乙醇回流提取3次,每次2h。屬混合提取的,簡述主要提取過程。
(3)提取后干燥參數應包括方法、溫度。例如:噴霧干燥(進風溫度160~180℃,出風溫度70~80℃)、減壓干燥(50℃,-0.08MPa)等。
(4)滅菌應提供原料、方法及參數。例如:輻照滅菌(人參,60Co,5KGy)、濕熱滅菌(121℃,30min)等。
(5)發酵參數應包括培養基組成、菌種、溫度、時間、pH、終止發酵方法等。
(6)涉及精制工藝的,需要列出精制工藝過程,例如:大孔吸附樹脂型號、前處理、吸附方法、洗脫方法等。
2.【直接接觸產品包裝材料的種類、名稱及標準】
(1)應提供與原注冊資料、送檢樣品及檢驗報告一致的直接接觸產品包裝材料的種類、名稱及標準。
(2)直接接觸產品包裝材料執行標準為企業標準的,應提供企業標準全文,并以表格形式表示。
3.【感官要求】
(1)狀態項應包括雜質描述。
(2)軟膠囊應分別對囊皮及內容物的色澤、性狀進行描述,硬膠囊無需對囊殼色澤進行描述。
(3)包衣片劑應分別對包衣及片芯的色澤進行描述。
4.【理化指標】
(1)屬性名為顆粒的,參照《中華人民共和國藥典》中“顆粒劑”的規定制定粒度、溶化性指標,并檢測三批產品粒度、溶化性衛生學。屬固體飲料的,按照固體飲料國家標準執行并修改屬性名。
(2)屬性名為含片的,應按《中華人民共和國藥典》中“片劑”的規定制定溶化性指標,并檢測三批產品溶化性穩定性。屬糖果等的,按照糖果國家標準執行并修改屬性名。
(3)酒劑應按照國家標準限量要求,制定甲醇、氰化物指標(注明以100%酒精度計)。
5.【微生物指標】
應符合GB 16740-2014《食品安全國家標準保健食品》的規定。原注冊申請或批準證書內容與現行國家標準沖突的,應當進行相應調整,使之符合現行國家標準的規定。
6.【標志性成分指標】
(1)注冊申請或批準證書內容為“《保健食品檢驗與評價技術規范》(2003年版)”的,列出檢驗方法全文,并根據產品具體情況對不明確的方法內容(如樣品前處理等)進行細化并提交研究報告。無需細化明確的,提交說明。
(2)引用的國家標準有多個檢測方法的,應當明確檢測方法為第幾法。例如:應明確鈣的檢測方法為第幾法,GB 5009.92中“第二法EDTA滴定法”。
7.【裝量或重量差異指標/凈含量及允許負偏差指標】
(1)《中華人民共和國藥典》“制劑通則”項下有相應要求的產品劑型,裝量或重量差異指標應符合相應劑型的規定。例如:應符合《中華人民共和國藥典》“制劑通則”項下“膠囊劑”的規定。
(2)普通食品形態產品應檢測并制定凈含量及允許負偏差指標,應按最小銷售包裝制訂凈含量及允許負偏差指標,指標應符合《定量包裝商品凈含量計量檢驗規則》(JJF1070)規定。例如:凈含量為50g/盒,允許負偏差為9%。
(3)粉劑應制訂凈含量及允許負偏差指標。屬散劑、顆粒劑等的,應按照《中華人民共和國藥典》“制劑通則”項下相應要求制訂裝量或重量差異指標,并相應修改產品屬性名。
8.【原輔料質量要求】
(1)原輔料名稱應與【原料】【輔料】項保持一致。
(2)原輔料符合國家相關標準的,應提供正確的現行有效版本的標準號及標準名稱。
(3)無國家相關標準的,應參考《保健食品注冊申請服務指南》5.2.2.4(5)制定原輔料質量要求,包括原料名稱(動植物類包括拉丁學名)、制法(包括主要生產工序、關鍵工藝參數等)、組成、提取率(得率)、感官要求、一般質量控制指標、污染物、農藥殘留量、功效成分或標志性成分、微生物等。
(4)提取物質量要求應按《保健食品注冊申請服務指南》11.2.1制定,包括原料來源(動植物類包括拉丁名稱)、制法(提取溶劑、溶劑量、溫度、時間、次數;干燥方法、溫度;滅菌方法、參數等)、提取率(范圍)、感官要求、一般質量控制指標、污染物指標、農藥殘留量、標志性成分指標、微生物指標等。
(5)銀杏葉提取物質量要求應包括原料來源(包括拉丁名稱)、制法、性狀、水分、灰分、得率、鉛、總砷、總汞、加工助劑殘留(根據制法,如大孔吸附樹脂、乙酸乙酯殘留等)、微生物(包括菌落總數、大腸菌群、霉菌和酵母、金黃色葡萄球菌、沙門氏菌)、總銀杏酸(≤10mg/kg)、總黃酮醇苷(以范圍值標示)、萜類內酯(以范圍值標示)、游離槲皮素(≤10mg/g)、游離山柰素(≤10mg/g)、游離異鼠李素(≤4mg/g)等指標。并按銀杏葉提取物原料質量標準及《國家食品藥品監督管理總局關于發布銀杏葉藥品補充檢驗方法的公告(2015年第66號)》的要求,提供銀杏葉提取物原料自檢報告。
(6)原輔料質量要求應引用具有專屬性的質量標準,而非通用標準或使用標準。若無相關標準,應參考《保健食品注冊申請服務指南》5.2.2.4(5)制定。例如:蘋果粉不應引用GB/T 29602《固體飲料》,大豆油不應引用GB 2716《植物油》,某食品添加劑不應引用GB 2760《食品添加劑使用標準》,復配原料不應引用GB 26687《食品安全國家標準復配食品添加劑通則(含第1號修改單)》。
(7)明確空心膠囊、淀粉種類。例如:明膠空心膠囊應符合《中華人民共和國藥典》的規定,玉米淀粉應符合《中華人民共和國藥典》的規定。
(8)對于有國家相關標準和現行規定的原輔料,質量要求應不得低于國家相關標準和現行規定。例如:氯化高鐵血紅素質量要求應參照《食品安全國家相關標準營養強化劑氯化高鐵血紅素(征求意見稿)》制定。硫酸軟骨素鈉質量要求中應明確原料來源,豬軟骨來源的應符合《中華人民共和國藥典》規定;其他動物軟骨來源的,除比旋光度外應符合《中華人民共和國藥典》規定。山楂質量要求中應制定展青霉素指標。
02 以銀杏葉提取物為原料的產品,應提交的申報資料(2021-10-08)
答:根據總局要求,為進一步強化審評與監管的銜接,從2016年3月1日起評審的以銀杏葉提取物為原料的產品,包括新申報、再注冊、技術轉讓和變更產品,除符合現行法規標準外,注冊申請人還應按以下要求提供資料:
一、將銀杏葉提取物原料質量標準納入產品技術要求。
銀杏葉提取物原料質量標準應包括:來源、制法、提取率、性狀、水分、灰分、鉛(≤2.0mg/kg)、總砷(≤1.0mg/kg)、總汞(≤0.3mg/kg)、加工助劑殘留(根據制法,如大孔吸附樹脂、乙酸乙酯殘留等)、微生物(包括菌落總數、大腸菌群、霉菌和酵母、金黃色葡萄球菌、沙門氏菌)、總銀杏酸(≤10mg/kg)、總黃酮醇苷(以范圍值標示)、萜類內酯(以范圍值標示)、槲皮素(≤10mg/g)、山柰素(≤10mg/g)、異鼠李素(≤4mg/g)等。
二、按銀杏葉提取物原料質量標準及《國家食品藥品監督管理總局關于發布銀杏葉藥品補充檢驗方法的公告(2015年第66號)》的要求,提供銀杏葉提取物原料自檢報告。
03 保健食品益生菌類標志性成分檢測方法的選擇和確認(2021-10-08)
答:為進一步明確保健食品益生菌類標志性成分檢測方法的研發和審評要求,我中心組織專題研討會,對相關審評問題進行了研究。現將有關情況發布如下,供保健食品注冊申請時參考。
鑒于現行的益生菌檢測方法國家標準和國際標準基本能夠滿足保健食品益生菌檢測需要,且國家標準和國際標準檢測方法穩定、復現、適用,目前暫不將益生菌類標志性成分檢測方法學研究資料作為強制性要求,但注冊申請人選擇和確認的檢測方法應符合以下國家標準或國際標準:
(一)檢測菌種在現行《可用于保健食品益生菌菌種名單》及《可用于食品的菌種名單》內的益生菌產品,檢測方法必須采用GB 4789.34或GB 4789.35規定的方法。
(二)檢測菌種不在現行《可用于保健食品益生菌菌種名單》及《可用于食品的菌種名單》內,且檢測方法無法采用GB 4789.34或GB 4789.35規定方法的產品,可采用AOAC(Association Of Official Analytical Chemists)微生物檢驗方法體系、USDA(United States Department of Agriculture)微生物檢驗方法體系、IDF(International Dairy Federation)微生物檢驗方法體系、FDA Bacteriological Analytical Manual(BAM)及ISO 16140規定的方法。
(三)檢測菌種不在現行《可用于保健食品益生菌菌種名單》及《可用于食品的菌種名單》內,且采用自行制定的檢測方法的產品,應提供檢測方法選擇和確定的依據,與上述國際微生物檢驗方法體系相應方法的三批產品檢測結果比對。
04 保健食品含片與顆粒劑溶化性指標檢測、標志性成分或功效成分檢測方法學研究資料、按新版食品安全國家標準修改指標的產品,應提供的申報資料(2021-10-08)
答:一、含片與顆粒劑的溶化性指標
含片與顆粒劑中溶化性指標、名稱一致,但其測定方法與考察目的不同。含片的溶化性按“崩解時限檢查法”檢查,考察產品在規定時限內不得崩解,驗證物質釋放方式與劑型設計的相符性;保健食品常見的顆粒劑包括可溶性顆粒與混懸型顆粒,可溶性顆粒溶化性檢查方法為:加熱水200mL,5分鐘內應全部溶化或輕微渾濁,不得有異物或焦屑,主要目的是檢查其是否混有不溶性異物等。
鑒于檢測目的不同,保健食品技術審評中,含片的溶化性指標作為產品穩定性重點考察指標,顆粒劑的溶化性指標作為產品非穩定性考察指標,混懸型顆粒暫不要求制訂溶化性指標。
二、標志性成分或功效成分檢測方法學研究資料
根據產品檢測方法來源,應提交產品標志性成分或功效成分檢測方法學研究資料,明確檢測方法建立的研究過程,驗證檢測方法的準確性、重現性和適用性。還應按《保健食品注冊申請服務指南》(以下簡稱《指南》),提交研究人員、研究時間、研究地點等溯源性資料。屬委托研究的,還應提交委托研究合同(協議)等。
(一)引用國家相關標準方法的,考慮方法建立時已進行方法學研究,不要求提供檢測方法建立的研究資料,但應參照GB/T 5009.1《食品衛生檢驗方法 理化部分 總則》,考察檢出限、精密度、準確度、線性范圍。
(二)檢測方法對國家相關標準方法的樣品前處理、檢測條件等內容進行修訂的,重點對方法修訂部分進行方法學研究,提供研究資料,并參照GB/T 5009.1《食品衛生檢驗方法 理化部分 總則》,考察方法的檢出限、精密度、準確度、線性范圍。
(三)申請人自行制訂檢測方法的,應提供全部的方法學建立研究報告,參照GB/T 5009.1《食品衛生檢驗方法 理化部分 總則》,考察檢出限、精密度、準確度、線性范圍,并考察所建立方法的專屬性與耐用性。
三、標準執行版本更替
對于因標準執行版本更替,引起的標準名稱或標準號變化,應根據檢測方法變化情況,提交申請材料。
(一)不涉及方法原理與操作步驟變化的,可不再要求申請人進行相關項目的測定。
(二)不能確定或已確定檢測方法發生原理或操作步驟變化的,要求申請人提供三批產品新老方法檢測比對結果。
四、執行《食品安全國家標準保健食品》(GB 16740)涉及的指標檢測
對于執行GB 16740,涉及產品技術要求調整和檢測報告要求,應根據指標調整的不同,提交申請材料。
(一)因執行GB 16740,放寬指標限值或減少微生物指標要求的,考慮到原已對相關指標進行了檢測,且符合現行GB16740規定,可不再要求提供相關指標檢測報告。
(二)因執行GB 16740,需對指標限值從嚴要求的,應提供具有法定資質的檢驗機構出具的三批產品該指標檢驗報告。
(三)因執行GB 16740,需修訂大腸菌群檢測方法的,應提供三批產品大腸菌群自檢報告。
(四)因執行GB 16740,確需單獨提交污染物和微生物指標變更注冊申請的,嚴格按照《關于實施<食品安全國家標準 保健食品>有關問題的公告》(2015年第104號)和《關于實施<食品安全國家標準 保健食品>有關問題的復函》(食藥監食監三便函〔2015〕216號)規定執行。
05 功能性保健食品的產品說明書中標志性成分及含量的標示值的確定要求(2021-10-08)
答:按《保健食品注冊申請服務指南》的要求,產品說明書中標志性成分及含量的標示值以產品技術要求中指標最低值標示。如某產品的技術要求中標志性成分含量為總黃酮≥900mg/100g,說明書中應標示為“每100g含:總黃酮900mg”;如某產品的技術要求中標志性成分含量為總黃酮500-900mg/100g,說明書中應標示為“每100g含:總黃酮500mg”。
06 酒劑產品標示產品說明書的注意事項要求(2021-10-08)
答:酒劑產品應在產品說明書注意事項中標示“對酒精過敏者慎用;本品不宜超量食用,不宜與其他酒類同時食用”。
07 不同原料的保健食品,不適宜人群標注要求(2021-10-08)
答:不同原料組方的保健食品,因原料本身的限制,其不適宜人群應當且不限于以下標注內容:
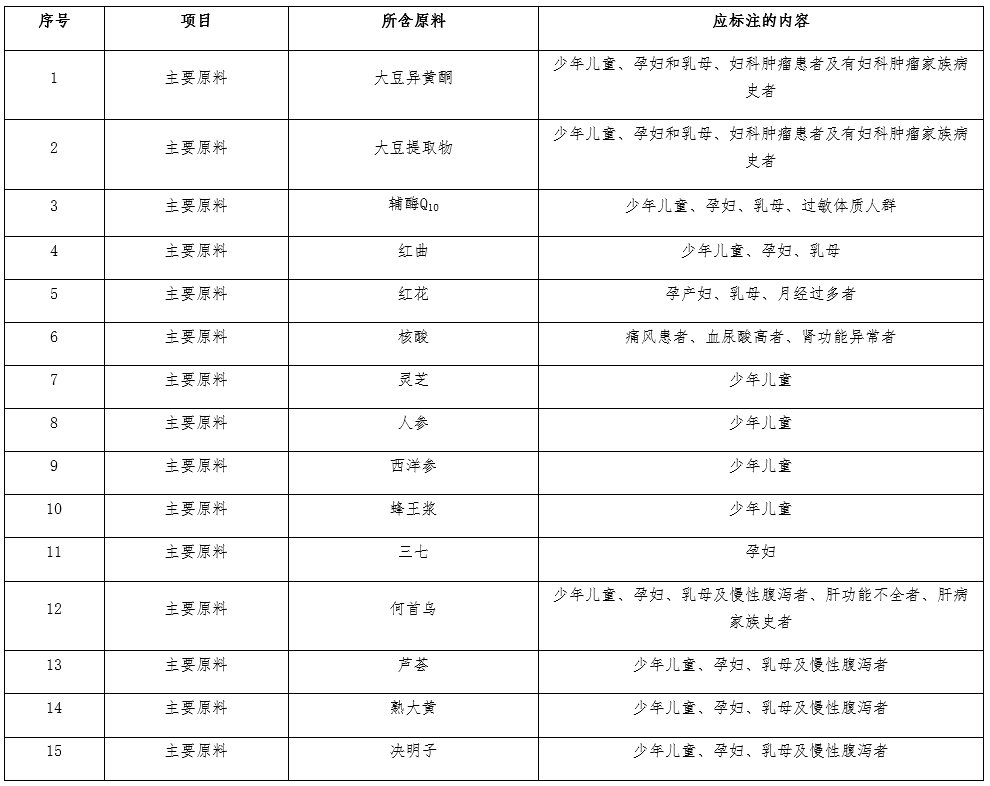
08 不同原料的保健食品,注意事項標注要求(2021-10-08)
答:不同原料組方的保健食品,因原料本身的限制,其注意事項應當且不限于以下標注內容:
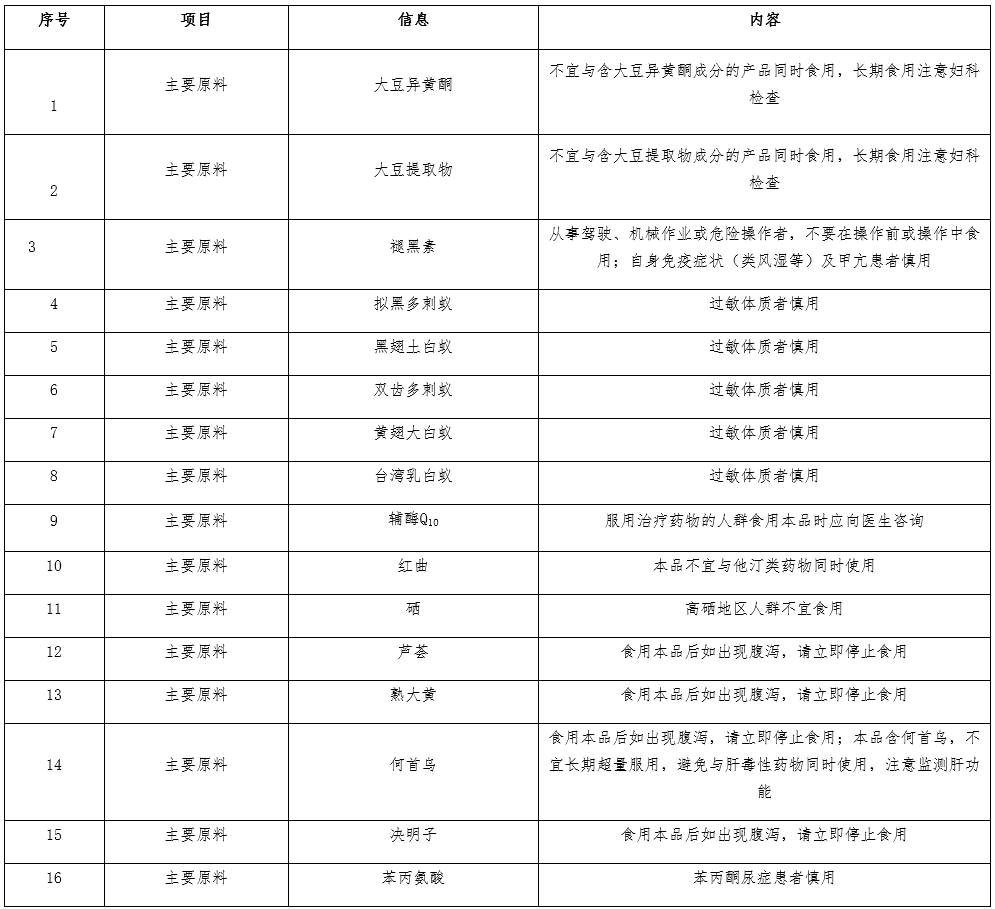
09 按審評意見需補充材料的新產品注冊和延續注冊(再注冊)申請,產品標簽說明書以及產品技術要求應補充完善哪些內容?(2021-09-23)
答:根據《關于保健食品注冊審評審批工作過渡銜接有關事項的通告》(16年第172號),已受理屬于注冊管理范圍的新產品注冊和延續注冊(再注冊)申請,申請人應按照《保健食品注冊審評審批工作細則》(2016年版)(以下簡稱《細則》)及《保健食品注冊申請服務指南》(2016年版)(以下簡稱《指南》)等相關規定完善產品標簽說明書以及產品技術要求。
一、產品標簽說明書
按照《細則》及《指南》等相關規定,補充完善產品標簽說明書內容,補充提供修訂說明以及規范的標簽說明書樣稿。
【原料】按配方材料列出全部原料。各原料順序按其在產品中的用量,由大到小排列。經輻照的原料,應在原料名稱后標注“(經輻照)”。
【輔料】按配方材料列出全部輔料。各輔料順序按其在產品中的用量,由大到小排列。經輻照的輔料,應在輔料名稱后標注“(經輻照)”。
【功效成分或標志性成分含量】應包括成分名稱及含量。應與產品技術要求中功效成分或標志性成分指標名稱一致,以產品技術要求中指標最低值為標簽說明書標示值。(營養素補充劑產品除外)
【適宜人群】應為與安全性、保健功能等科學依據相符的食用安全、有明確功能需求、適合本產品的特定人群。
【不適宜人群】應為適宜人群范圍中應當除外的特定人群、現有科學依據不足以支持該產品適宜的嬰幼兒、孕婦、乳母等特殊人群,以及現行規定明確應當標注的特定人群。暫無法確定不適宜人群的,應明確注明“限于目前科學研究水平,該產品暫未發現明確的不適宜人群,將根據收集到的食用安全信息,予以完善補充”。
【保健功能】應經研發綜合確定,符合保健功能聲稱管理的相關要求。
【食用量及食用方法】應與產品配方配伍及用量的科學依據、安全性和保健功能試驗評價材料等相符。
【規格】應為最小制劑單元的重量或者體積(不包括包裝材料;膠囊劑指內容物;糖衣片或丸指包糖衣前的片芯或者丸芯),應與產品食用量及食用方法相匹配。酒類產品應注明酒精度。
【貯藏方法】應根據產品特性、穩定性試驗等綜合確定。貯藏方法為冷藏等特殊條件的,應列出具體貯藏條件。
【保質期】應經研發綜合確定。以“××月”表示,不足月的以“××天”表示。
【注意事項】應注明“本品不能代替藥物。適宜人群外的人群不推薦食用本產品”。必要時還應根據法規規定、研發情況、科學共識以及產品特性增加相應注意事項。
備注:
1、【功效成分或標志性成分含量】項,應以重新確認提交的技術要求中相應指標的最低值標示(營養素補充劑產品除外)。
2、【適宜人群】、【不適宜人群】項內容未按《指南》要求確定的,應按《指南》要求修改完善。修訂后的內容較原確認提交的內容擴大了適宜人群范圍或縮小了不適宜人群范圍的,應說明理由并提供相應的科學證據。
3、【注意事項】內容應準確完備,需增加的內容應表述詳明。
二、產品技術要求新增內容
1、【生產工藝】項
應以文字形式描述主要生產工藝,包括主要工序、關鍵工藝參數或參數合理范圍等。非關鍵工藝的工藝參數可不提供。關鍵工藝是指產品生產過程中,對產品質量安全或保健功能有直接影響,不隨著工藝規模、生產設備等客觀變化必須進行參數調整的工藝。如:提取精制、干燥等工序的技術參數或參數合理范圍,滅菌的方法及具體參數等。
示例1:本品經提取(提取溶劑、時間、次數、溫度)、精制(D101大孔樹脂,簡述洗脫過程)、濃縮、真空干燥(××℃)、配制、過濾、熱壓滅菌(121℃,30min)、灌裝、包裝等主要工藝加工制成。
示例2:本品經混合、制粒、壓片、包裝等主要工藝加工制成。
2、【直接接觸產品包裝材料的種類、名稱及標準】項
應以文字形式描述經研發確定的直接接觸產品包裝材料的種類、名稱及標準。直接接觸產品的包裝材料的名稱、種類、標準號和標準文本應完整,選擇依據應符合現行規定。
示例:鈉鈣玻璃藥瓶應符合《鈉鈣玻璃模制藥瓶》(YBB00272002-2015);鋁防偽瓶蓋應符合《中華人民共和國包裝行業標準 鋁防偽瓶蓋》(BB/T 0034-2006)。
3、【裝量或重量差異指標/凈含量及允許負偏差指標】項
應以文字形式描述裝量或重量差異指標(凈含量及允許負偏差指標)。《中華人民共和國藥典》(以下簡稱《中國藥典》)“制劑通則”項下有相應要求的產品劑型,標注“裝量(或重量)差異指標應符合《中華人民共和國藥典》中制劑通則項下XXXX的規定。
示例1(XXX片):重量差異指標應符合《中華人民共和國藥典》中“制劑通則”項下片劑的規定。
示例2(XXX膠囊):裝量差異指標應符合《中華人民共和國藥典》中“制劑通則”項下膠囊劑的規定。
普通食品形態產品應制定凈含量及允許負偏差指標,指標應符合《定量包裝商品凈含量計量檢驗規則》(JJF 1070)規定。
示例(XXX飲料):凈含量為250mL/瓶,允許負偏差為9mL;150mL/瓶,允許負偏差為4.5%。
4、【原輔料質量要求】項
質量要求為國家標準、地方標準、行業標準的,應列出標準號;符合國家標準、地方標準、行業標準,且部分指標應同時符合企業標準的,應列出標準號或規范性文件的標題文號,同時以文字形式列出企業標準的指標項目及指標值。
為企業標準的,應以列表形式列出指標項目及指標值。無適用的國家標準、地方標準、行業標準的原料,還應列出主要生產工序和關鍵工藝參數。
對于以提取物為原料的產品,還應按《指南》完善提取物質量要求,包括原料來源(對動植物品種有明確要求的,應明確其具體品種,必要時寫明原植物拉丁學名)、制法(包括主要生產工序、關鍵工藝參數等)、提取率(得率)、感官要求、一般質量控制指標(如水分、灰分、粒度等)、污染物指標(鉛、總砷、總汞、提取溶劑殘留等)、農藥殘留量、標志性成分指標(難以定量測定的應當制定專屬性定性鑒別指標)、微生物指標(包括菌落總數、大腸菌群、霉菌和酵母、金黃色葡萄球菌、沙門氏菌)等。內容有缺項難以制定或無需制定的,原因應合理。
示例:銀杏葉提取物
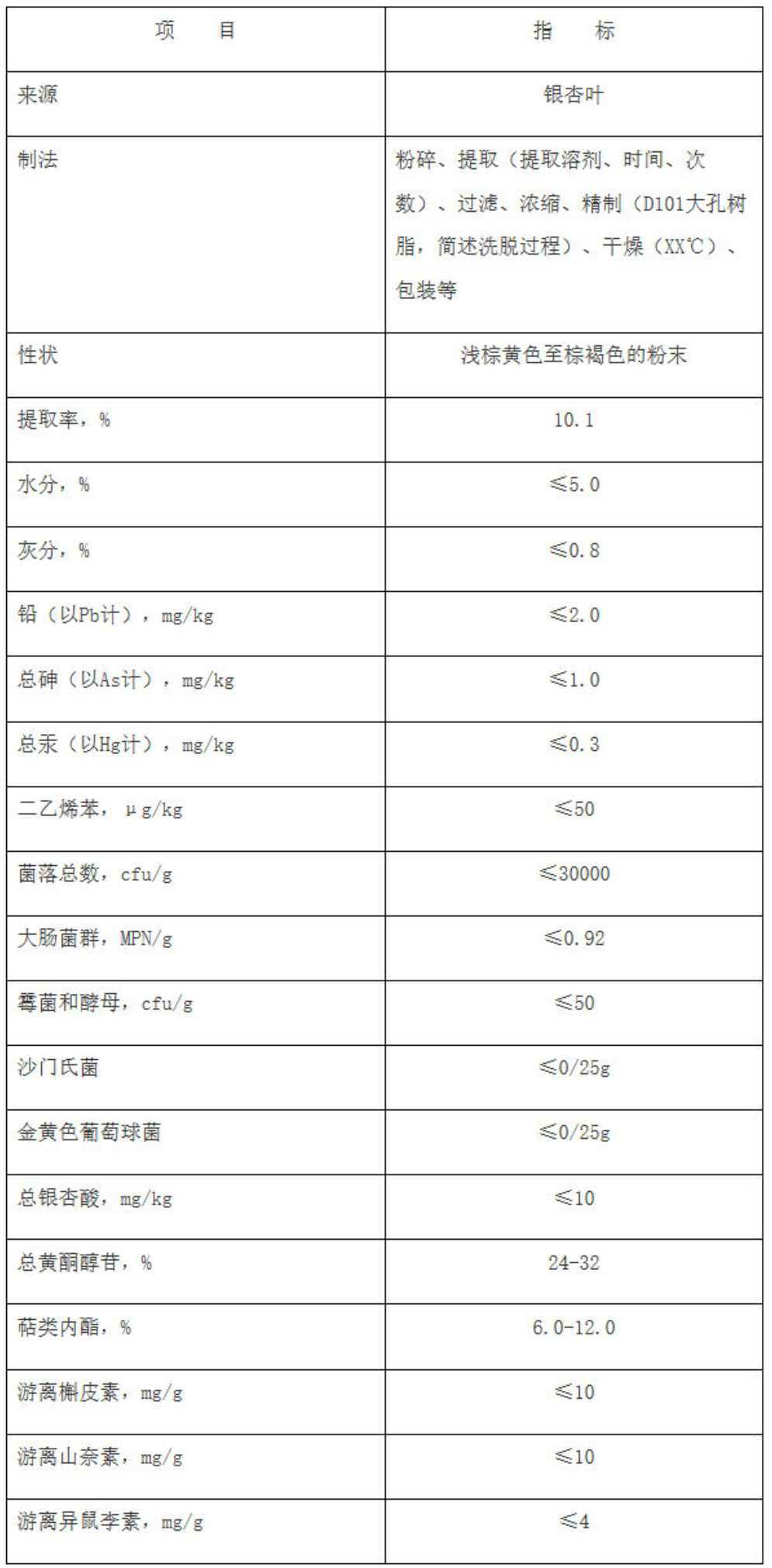
三、其它注意事項
1、補充提供的產品技術要求中原已認可內容不得更改,新增內容應與原已認可的生產工藝、企業標準、直接接觸產品的內包裝材料等相關內容保持一致。
2、產品標簽說明書電子版本提交
登錄市場監督管理總局食品審評中心網站(http://www.cfe-samr.org.cn/),上傳規范完善后的標簽說明書樣稿,同時提交加蓋申請人公章的標簽說明書樣稿、修訂說明等補充資料。
注:1.問答來源:國家市場監督管理總局食品審評中心;
2.每個問題后括號中備注的日期為食品審評中心發布該問答的具體時間,以供參考;
3.“國家食品藥品監督管理局”目前已改名為“國家市場監督管理總局”。
相關推薦:
- 2021年上半年保健食品注冊類產品批件發布情況分析
- 保健食品常見問題與解答-備案篇(1):原輔料
- 備案穩定性實驗如何執行?是否可以委托檢測?保健食品常見問題與解答——備案篇(2):理化檢驗及質量標準
- 進口保健食品備案證明文件怎么出?保健食品常見問題與解答——備案篇(3):進口保健食品備案
- 備案保健食品信息如何填報?保健食品常見問題與解答——備案篇(4):其它
- 瑞旭再傳捷報!17款進口保健食品備案產品發布,近半數由瑞旭申報成功!
我們的服務:
