

三類器械
軟性親水接觸鏡獲批上市
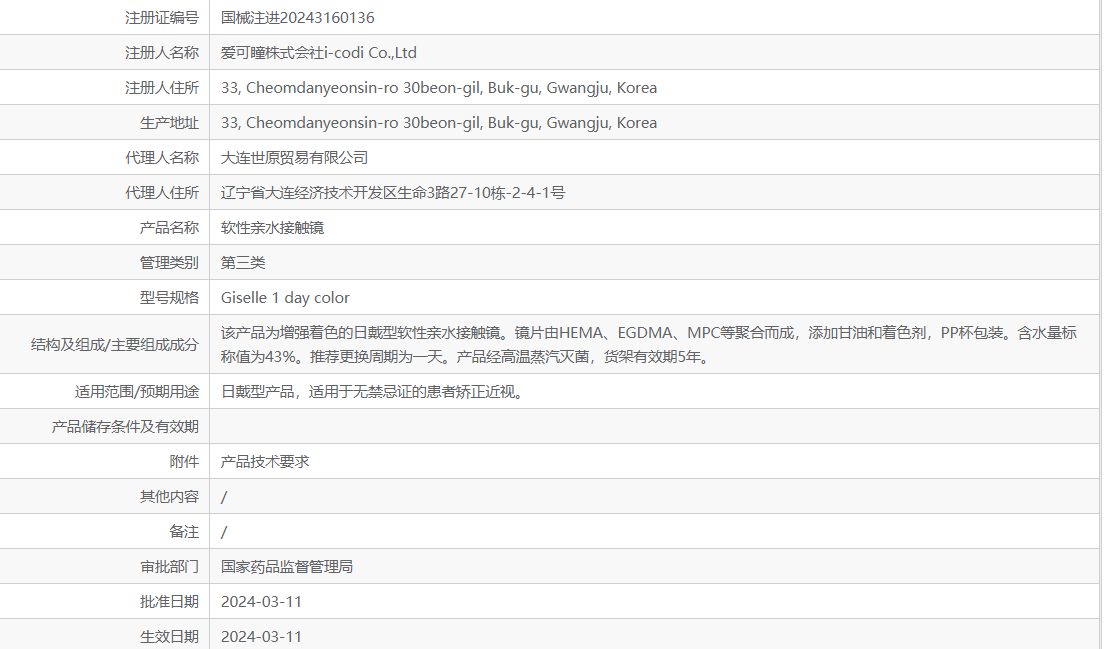
近期,CIRS協助韓國icodi.,Ltd公司順利完成了三類軟性親水接觸鏡的首次注冊。該產品是繼庫博光學后又一款采用了MPC(2-甲基丙烯酰氧乙基磷酸膽堿)的鏡片。
隱形眼鏡鏡片上的沉淀物是隱形眼鏡發生不良臨床反應的重要原因之一,針對這一問題,通過對鏡片的消毒和護理尚不能根除。而沉淀物主要是淚液中的蛋白質和脂質等,其中蛋白質最易沉淀形成蛋白質覆蓋層。細菌附著于蛋白質覆蓋層后容易滋生形成菌落,影響鏡片壽命并導致眼睛不適。而兩性離子聚合物 2-甲基丙烯酰氧乙基磷酸膽堿(MPC)可以有效阻抗非特異性蛋白的吸附,以改善隱形眼鏡的蛋白質沉淀的缺陷。
Icodi公司的該款鏡片由于其配方的特殊性屬于使用了新材料的鏡片,故而該產品在注冊過程當中需要針對新材料做出相應的研究以及進行臨床試驗。CIRS在該項目的注冊過程中充分研究了隱形眼鏡產品相關的法規政策,給出了合理的注冊策略和臨床試驗方案。
在評審環節,NMPA就該項目的臨床試驗部分未提出任何發補意見,其他非臨床研究部分未出現重大問題發補,故而該短期內該項目便提交了相關發補資料并獲得了醫療器械注冊證。
通過這一項目,CIRS團隊也完成了軟性親水接觸鏡領域技術的沉淀,對軟性親水接觸鏡的法規有了更深層次的理解和實操經驗,對未來該類項目的執行也更具把握。
瑞旭集團-北京西爾思醫療器械技術團隊由行業資深法規及醫學專業工程師領銜,技術團隊80%以上具有研究生學歷,細分于醫療器械產業中的不同技術領域,包括醫療器械注冊團隊、醫療器械質量管理體系技術團隊、臨床醫學團隊、臨床評價技術團隊、醫學統計與數據管理團隊、臨床試驗運營團隊、醫療器械評價與檢測技術團隊、醫療器械研發及生產技術團隊,可為您的項目提供專業高效的服務,保障項目順利開展。
醫療器械第Ⅱ/Ⅲ類注冊申報
依據《醫療器械監督管理條例》規定,第II、III類醫療器械施行注冊管理,在投放中國市場前,應先向藥品監督管理部門提交注冊申請并獲得醫療器械注冊證。同時確保在醫療器械生產質量管理規范體系下開展研發及生產經營活動。,全面開展文明創建工作。
醫療器械臨床評價及試驗
臨床試驗是醫療器械臨床評價過程中臨床數據的主要來源,是為評價醫療器械安全性、臨床性能或有效性而開展的系統性試驗或研究,包括可行性試驗、注冊臨床試驗及上市后臨床試驗。醫療器械臨床試驗應符合《醫療器械臨床試驗質量管理規范》(也稱為醫療器械GCP)要求,并在中國備案的醫療器械臨床研究機構開展。
醫療器械SMO服務
瑞旭集團為醫療器械臨床研究提供專業的SMO服務,包括前期臨床試驗準備、現場執行、項目全流程管理等服務,公司委任的項目經理和CRC組成的項目團隊,與申辦方、臨床試驗機構、研究者、CRO進行溝通,確保臨床試驗進程和規范化。
內容來源:NMPA/糖吉醫療公開資料收集


